- 首页 > 正文
顾兵教授:感染标志物及检测技术新进展
感染医线 发表时间:2023/11/12 21:20:53
编者按:在疾病的早期筛查、预测预警、鉴别诊断、用药指导、预后判断及疗效监测等全周期医疗决策中,绝大多数数据来源于检验,医学检验在医疗系统中具有全局性和系统性的作用。在近期召开的第六届华夏临床微生物学学术年会暨第十二届京港感染论坛中,广东省人民医院检验科顾兵教授分享了感染标志物及检测技术新进展,现整理如下,供读者参考。
1.生物标志物
《中国脓毒症早期预防与阻断急诊专家共识(2020)》推荐了5种感染生物学标志物[1],它们分别是肝素结合蛋白(heparin-binding protein,HBP)、C反应蛋白(C-reactive protein,CRP)、血清淀粉样蛋白A(serum amyloid A,SAA)、降钙素原(proealcitonin,PCT)和白细胞介素-6(Interleukin-6,IL-6)。HBP是目前唯一可以用于预测未来72小时内脓毒症发生风险的血液标志物;CRP是细菌感染早期鉴别指标;SAA升高多见于病毒感染;PCT用于脓毒症的诊断、预后评估及治疗监测;IL-6是炎症、脓毒症的早期敏感性“警示”标志物。除此之外,可溶性白细胞分化抗原14亚型(soluble cluster of differentiation antigen14 Sub-Type,sCD14-ST)也是重要的感染标志物,常用于创新脓毒症的诊疗。
1) 肝素结合蛋白(HBP)
HBP又称为天青杀素或CAP37[2],来源于中性粒细胞,主要储存于嗜天青颗粒,少部分储存于分泌小泡中,中性粒细胞活化后脱颗粒,即释放出HBP。成熟的HBP是由222个氨基酸组成的单链蛋白质,分子量29 kDa,属于丝氨酸蛋白酶家族成员,无蛋白酶活性,对脂多糖脂质A具有高亲和力。
HBP在临床感染诊疗中有多方面的应用,6~24小时定期监测HBP浓度可提前预测脓毒症风险,HBP持续升高说明脓毒症风险增加。采用HBP+SOFA/qSOFA评分可以大大提升诊断灵敏度。通过24小时定期监测,计算HBP-c,可预测生存率/评估预后。检测体液中HBP含量,可查找局部感染灶并评估感染严重程度(CSF-HBP、UHBP等)。
诱导血管渗漏是HBP与其他感染标志物最根本的差别之一,通过结合HBP、稳定细胞膜、保护糖萼选择白蛋白、肝素、激素、辛伐他汀、替唑生坦、硫酸葡聚糖等药物治疗,可预防、缓解血管渗漏过度。
2) 降钙素原(PCT)
PCT是降钙素超家族的成员,由116个氨基酸组成,分子量约为14.5 kDa。大量研究均发现PCT在抗生素感染中的指导作用和监测价值,并得到指南/专家共识认可。该指标已广泛应用于感染、脓毒症诊疗路径的早期诊断、用药指导、治疗监测、风险分层和预后评估,临床接受度高。
依据2020版专家共识[3],对于非重症下呼吸道感染患者,可基于PCT浓度水平判断细菌感染可能性,当PCT浓度>0.25 μg/L时,细菌感染可能性高,基于临床判断可启动抗感染治疗;当PCT下降至0.25 μg/L或峰值浓度80%以下,且病情稳定的情况下,建议停用抗菌药物(图1)。对于ICU重症感染患者,当PCT浓度<0.5 μg/L时,持续细菌感染可能性低,如若病情稳定可考虑停用抗菌药物;当PCT浓度≥0.5 μg/L时,极有可能存在持续细菌感染,考虑治疗无效,应及时调整治疗方案,并持续监测至PCT<0.5 μg/L或降至峰值浓度80%以下,方可停用抗菌药物(图2)。
.png)
图1. 非重症下呼吸道感染患者中PCT的临床应用(来自讲者PPT)
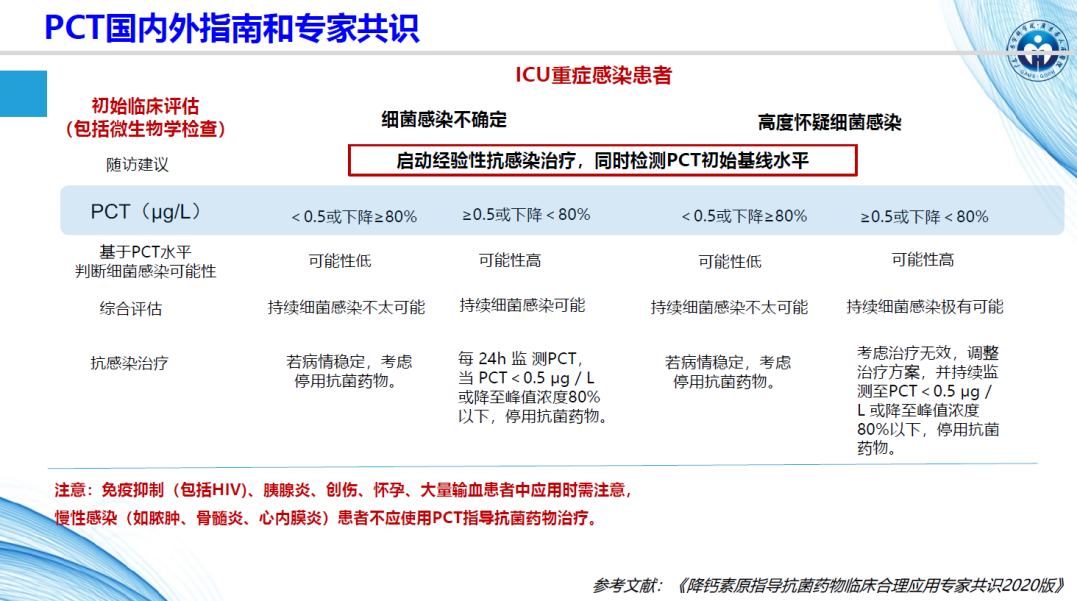
图2. ICU重症感染者中PCT的临床应用(来自讲者PPT)
3) 白细胞介素-6(Interleukin-6,IL-6)
IL-6是细胞因子网络中的重要成员,在急性炎症反应中处于中心地位,是炎症、脓毒症的早期敏感性“警示”标志物。IL-6的临床发展主要分为3个阶段,1968~2000年期间主要是IL-6的发现及基础研究,如其分泌细胞,主要作用及信号通路等。2000~2015年处于泛临床研究初期,此时应用涉及多个临床场景,如免疫调节、造血、炎症和肿瘤等。2015~2021年进入临床深入期,主要用于全身性炎症的早期诊断,脓毒症辅助诊断和风险分层等[4-7]。
脓毒症是由菌血症或其他感染引发的全身炎症反应综合征,起病急,进展迅速,病死率高。当人体的免疫系统发现外来入侵的病原时,首先要和这个病原做斗争,就会触发免疫反应来杀灭病毒,保护我们的人体;同时,免疫反应也会造成免疫损伤,所以它本身是一把双刃剑。正常状态下,人体处于免疫稳态,IL-4、IL-13、IL-10等主要的抗炎因子与TNF-α、IL-2、IL-6、IL-8、IFN-γ等主要促炎因子处于炎症反应平衡状态。当炎症反应失衡时,如果促炎介质过量,则发生全身炎症反应综合征(systemic inflammatory response syndrome,SIRS),最终导致细胞凋亡、器官功能障碍;如果抗炎介质过量,出现机体免疫功能抑制,增加感染机率。脓毒症是宿主对感染原的复杂机体反应,内源性反应导致的器官损伤可能远大于感染直接的损害。
当感染和炎症发生后,IL-6率先生成且水平迅速升高,其升高水平与炎症严重程度一致,而PCT在感染早期升高较慢,所以IL-6检测可以更早的评估脓毒症风险,有效预测脓毒症。
4) 可溶性白细胞分化抗原14亚型(soluble cluster of differentiation antigen14 SubType,sCD14-ST)
sCD14-ST由不依赖于细胞因子的细菌吞噬作用所诱导,产生机制不同于PCT、CRP和IL-6[4]。sCD14-ST是病原体直接相关的标记物,较PCT可以更直接、更早的反应机体感染,在细菌感染及脓毒症早期诊断、危险分层和预后评估等方面有着独特的优势。2019年以来,sCD14-ST在NICU、中心ICU的脓毒症和创伤临床研究中广泛应用,涌现出大量在新生儿脓毒血症诊断、发热性中性粒细胞减少症、感染等相关领域的医学研究。
Masson[8]等的一项临床研究表明,患者从进入ICU第一天起,其sCD14-ST含量在生存组和死亡组之间就存在显著差异,而PCT在第7天才会表现出显著差异。Endo等[9]的研究表明在ICU患者疗效监测中,sCD14-ST在疗效显著(好转)组呈降低趋势,疗效不显著组其含量保持不变或上升。但无论病情是否好转,疗效是否显著,PCT水平均呈明显下降趋势。一项sCD14-ST在创伤和手术的应用研究表明[10],创伤后的前3天内,感染组血浆sCD14-ST显著升高,而非感染组未见升高;然而,感染和非感染创伤患者的血浆PCT、CRP和WBC均显著升高。
Carlo等[11]关于新生儿脓毒症sCD14-ST的研究表明,sCD14-ST水平在T0期及抗生素治疗过程中,新生儿感染、脓毒症、脓毒症休克组间存在显著差异。Yusuke等将sCD14-ST应用到中性粒伴发热临床诊断中[12],患者化疗后在第10天感染肺炎克雷伯菌,第9天sCD14-ST即出现显著升高,比CRP的变化提前一天,所以sCD14-ST可用于化疗后细菌感染的早期诊断。
5) 血清淀粉样蛋白A(serum amyloid A,SAA):
SAA是淀粉样沉积的前体物质,是一种急性时相反应蛋白,属于载脂蛋白家族中的异质类蛋白质,是Rosenthal等人在研究淀粉样变性的过程中发现的一种蛋白质。SAA基因家族有4个成员,包括SAA1、SAA2、SAA3和SAA4,其中SAA1和SAA2基因表达的蛋白即为“acute phase SAA”。作为一种急性时相反应蛋白,其增高幅度反映病情严重程度,广泛应用于感染、炎症、外伤、肿瘤等诊断。
在急性时相反应中,经白细胞介素IL-6和肿瘤坏死因子刺激,肝细胞可迅速合成SAA,在感染的5~6 小时内达到峰值,半衰期一般为50 min。临床上主要用于小儿感染性疾病的早期诊断,如新生儿败血症、脓毒症,可有效评估细菌或病毒感染的严重程度和治疗效果,也常与CRP联用,鉴别细菌与病毒感染。
6) C反应蛋白(C-reactive protein,CRP)
CRP是一种急性时相反应蛋白,大多数感染可引发其浓度迅速上升,通常于感染后2 小时开始升高,24~48 小时达高峰。细菌感染时CRP升高显著,而病毒感染时大都正常或轻微升高。因此CRP通常作为鉴别细菌或病毒感染的参考指标之一。
7) IPS感染标志物新组合
高灵敏度多元炎症标志物的联合检测可以辨别细菌与病毒感染,有利于抗菌药物的合理使用和感染疾病的早期快速筛查,是即时检测领域的一个重要需求,也为细菌感染及脓毒症早期诊断、预后评估提供解决方案。
IL-6和sCD14-ST分别为机体反应和病原体情况的直接指标,对反映病情和预后评估均有重要临床价值;PCT为机体反应和病原体情况的间接指标,IPS联合应用,能更真实的反映感染状态(图3),更及时准确反映病情进展(图4)。
.png)
图3. IPS联合应用案例(来自讲者PPT)
.png)
图4. IPS联合应用案例(来自讲者PPT)
在“IPS联合应用在脓毒症28天生存组和死亡组差异比较”研究中,回顾生存组与死亡组前、6、7天,四个感染标志物(IL-6,PCT,CRP及sCD14-ST)的中位数,均只有sCD14-ST具有显著性差异;前5、6、7天的中位数差异效应量差别不大,提示sCD14-ST可提前至5天进行预测,说明IPS联合应用能有效加强标记物在脓毒症预后评估的预警作用(图5)。从首日测值结果来看,仅sCD14-ST在病重组与病危组中仍具有显著性差异,具有区分两种病情严重程度的能力(图6),也体现了IPS联合应用在加强标记物早期测值对脓毒症病情分层的价值。
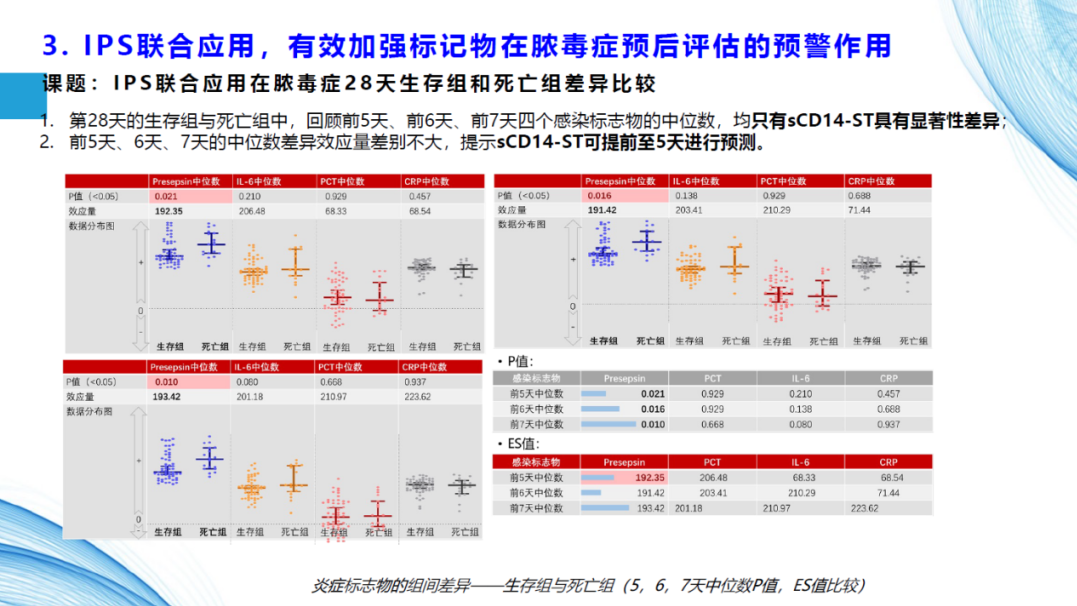
图5. IPS联合应用有效加强标记物在脓毒症预后评估的预警作用(来自讲者PPT)

图6. IPS联合应用在加强标记物早期测值对脓毒症病情分层的价值(来自讲者PPT)
2. 检测技术新进展
1) 微生物质谱检测新技术
病原微生物的鉴定是临床检验的重要组成板块。通过表型、生化反应等传统方法来进行微生物鉴定,操作繁琐、耗时长、鉴定微生物种类十分有限。微生物质谱技术平台成本低、速度快,准确率极高,对常见病原细菌或酵母菌的鉴定准确率高达95%,在临床得到了高度认可。微生物质谱是基于定性检测的基质辅助激光解吸电离飞行时间质谱仪(MALDI-TOF MS),仪器技术原理简单,操作便捷。
SCI期刊Journal of Thoracic Disease于2014年2月设立VITEK MS质谱专栏,刊登关于VITEK MS质谱综述、论著和病例报道等文章,让国际同行了解本领域的学术进展。顾兵教授团队在该刊中发表1篇综述和7篇论文。
2) 宏基因组测序(metagenomics Next Generation Sequencing,mNGS)
mNGS是基于宏基因组学的新一代测序技术,不依赖于传统的微生物培养、无需预设,直接提取临床样本中的DNA/RNA,进行高通量测序,经过专用病原数据库比对与生信分析,可一次性完成1万多种细菌、真菌、病毒和寄生虫等病原体的检测。
mNGS联合传统检测,可提高病原体检出率。2016年,北京协和医院入组来自ICU患者的78份血液样本[13],同时进行血培养与mNGS,并通过PCR扩增/Sanger测序验证,评估mNGS在ICU患者的感染诊断价值。结果表明,mNGS可显著提高细菌/真菌/病毒整体阳性率(31% vs. 13%)。2019年,美国mNGS测序公司Karius基于cfDNA进行mNGS确认试验[14],筛选13种代表微生物对mNGS进行性能评估。评估纳入350例脓毒症患者,结果表明mNGS与血培养的阳性符合率为93.7%。mNGS与血培养和其它方法联合可以显著提高病原体检出率(52%)。
复旦大学附属华山医院张文宏教授团队纳入108名接受激素治疗的免疫抑制疑似患者[15],对所有患者同时进行常规微生物检测(CMT)和mNGS检测。对于多重感染病原体的诊断,相比于CMT,mNGS缩短检测时间近半。基于mNGS检测结果调整抗生素方案的患者治疗成功率(81.8%)显著高于经验性使用抗生素的患者(52.6%)。
对于临床不明原因发热及新发罕见病原体、混合感染的疑难问题,重症肺炎、脑膜炎、脓毒症等危重病例、器官移植、免疫缺陷或低下等特殊人群,mNGS检测提供了解决方案。如一名新生隐球菌肺炎患者(图7),经过分析各项检查结果,取消肺部穿刺,先行肺泡灌洗液送检mNGS并确诊,有效减少了有创检查。
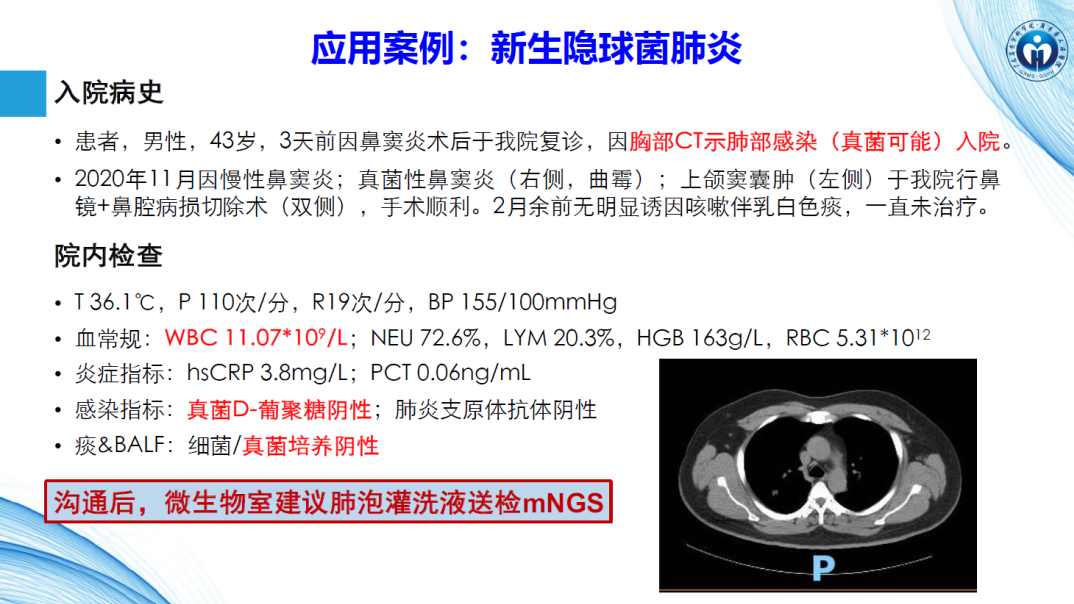
图7. 新生隐球菌肺炎病例(来自讲者PPT)
3) LDT产品研发
LDT(Laboratory Developed Test)项目,指针对尚未获得产品注册、仅在实验室内部研发、验证与使用的体外诊断项目,最早由美国提出并实践,主要是为了缓和医疗器械监管与实际临床需求之间的矛盾,允许满足特定条件的医学实验室自研并使用未经注册的体外诊断试剂产品用于临床诊断。目前基于临床检验需求,很多临床实验室自建项目也在开展,由医学检验部门自行开发的检测方法介绍如下。
基于适配体和凝集素双识别的SERS新技术[16]:采用凝集素修饰的金壳磁珠作为高效的细菌捕获工具,同时利用适配体修饰的胶体金作为稳定的SERS信号来源,成功构建了一种双识别SERS生物传感器。首次使用基于麦胚凝集素和适配体的双识别生物传感器同时检测两种病原菌。首次使用基于麦胚凝集素和适配体的双识别生物传感器同时检测两种病原菌。
单线检多种目标分析物的SERS免疫层析技术:将拉曼报告分子修饰在标签表面,赋予材料特征性的拉曼峰值,可以通过不同拉曼位移处的信号峰值来判断和定量多种目标分析物的含量。实现单条检测线检测两种抗生素,结合磁性材料的富集增强能力,有效增强免疫层析体系的灵敏度和检测通量。30分钟内实现卡那霉素/氯霉素高敏检测,检测限分别达到0.54 pg/mL和0.47 pg/mL(未发表数据)。
研发基于氧化石墨烯的三维荧光量子点免疫层析技术[17]:开发新型二维柔性膜状多层量子点材料,建立了一种同时筛选新冠、甲流和腺病毒的超灵敏免疫层析方法。实现唾液样品中三种呼吸道病毒的同步快速、高敏检测。
研发新冠变异株快速分型的等温扩增技术[18]:实现新冠病毒Delta突变株及野生株的快速检测及区分,1小时左右实现新冠病毒及其Delta变异株的特异性区分,分型准确率达到100%。
构建基于宏基因测序的云端毒力因子分析体系:性能全面优于现有基于组装的毒力预测软件(灵敏度和特异度均>97%),包含24种临床重要病原菌最广泛最全面的毒力基因参考序列(株水平)。在前瞻性队列中验证发现,该云端体系能实现高毒力肺克的快速和准确预测(kappa=0.94)(未发表数据)。
真菌tNGS技术的建立、验证与临床转化:开发了临床常见的60种真菌的靶向测序panel,以增加真菌检出性能、降低检测成本。
感染性心内膜炎的数字PCR定量检测panel:合作研发基于ddPCR的感染性心内膜炎(IE)12种病原体定量检测试剂盒,旨在3 小时内实现IE常见病原体的灵敏特异、快速、多靶检测。
参考文献
[1] 中国医疗保健国际交流促进会急诊医学分会,中华医学会急诊医学分会,中国医师协会急诊医师分会,中国人民解放军急救医学专业委员会.中国脓毒症早期预防与阻断急诊专家共识[J].临床急诊杂志,2020,21(7):517-529.DOI:10.13201/j.issn.1009-5918.2020.07.001.
[2] Tapper H, Karlsson A, M?rgelin M, Flodgaard H, Herwald H. Secretion of heparin-binding protein from human neutrophils is determined by its localization in azurophilic granules and secretory vesicles. Blood. 2002;99(5):1785-1793. doi:10.1182/blood.v99.5.1785
[3] 中国医药教育协会感染疾病专业委员会.降钙素原指导抗菌药物临床合理应用专家共识[J].中华医学杂志,2020,100(36):2813-2821.DOI:10.3760/cma.j.cn112137-20200714-02112.
[4] Teggert A, Datta H, Ali Z. Biomarkers for Point-of-Care Diagnosis of Sepsis. Micromachines (Basel). 2020;11(3):286. Published 2020 Mar 10. doi:10.3390/mi11030286
[5] Tanaka T, Narazaki M, Kishimoto T. Immunotherapeutic implications of IL-6 blockade for cytokine storm. Immunotherapy. 2016;8(8):959-970. doi:10.2217/imt-2016-0020
[6] Ma L, Zhang H, Yin YL, et al. Role of interleukin-6 to differentiate sepsis from non-infectious systemic inflammatory response syndrome. Cytokine. 2016;88:126-135. doi:10.1016/j.cyto.2016.08.033
[7] Harbarth S, Holeckova K, Froidevaux C, et al. Diagnostic value of procalcitonin, interleukin-6, and interleukin-8 in critically ill patients admitted with suspected sepsis. Am J Respir Crit Care Med. 2001;164(3):396-402. doi:10.1164/ajrccm.164.3.2009052
[8] Masson S, Caironi P, Spanuth E, et al. Presepsin (soluble CD14 subtype) and procalcitonin levels for mortality prediction in sepsis: data from the Albumin Italian Outcome Sepsis trial. Crit Care. 2014;18(1):R6. Published 2014 Jan 7. doi:10.1186/cc13183
[9] Endo S, Suzuki Y, Takahashi G, et al. Presepsin as a powerful monitoring tool for the prognosis and treatment of sepsis: a multicenter prospective study. J Infect Chemother. 2014;20(1):30-34. doi:10.1016/j.jiac.2013.07.005
[10] Kang J, Gong P, Zhang XD, Wang WJ, Li CS. Early Differential Value of Plasma Presepsin on Infection of Trauma Patients. Shock. 2019;52(3):362-369. doi:10.1097/SHK.0000000000001269
[11] Pietrasanta C, Ronchi A, Vener C, et al. Presepsin (Soluble CD14 Subtype) as an Early Marker of Neonatal Sepsis and Septic Shock: A Prospective Diagnostic Trial. Antibiotics (Basel). 2021;10(5):580. Published 2021 May 14. doi:10.3390/antibiotics10050580
[12] Koizumi Y, Shimizu K, Shigeta M, et al. Plasma presepsin level is an early diagnostic marker of severe febrile neutropenia in hematologic malignancy patients. BMC Infect Dis. 2017;17(1):27. Published 2017 Jan 5. doi:10.1186/s12879-016-2116-8
[13] Long Y, Zhang Y, Gong Y, et al. Diagnosis of Sepsis with Cell-free DNA by Next-Generation Sequencing Technology in ICU Patients. Arch Med Res. 2016;47(5):365-371. doi:10.1016/j.arcmed.2016.08.004
[14] Blauwkamp TA, Thair S, Rosen MJ, et al. Analytical and clinical validation of a microbial cell-free DNA sequencing test for infectious disease. Nat Microbiol. 2019;4(4):663-674. doi:10.1038/s41564-018-0349-6
[15] Wang S, Ai J, Cui P, Zhu Y, Wu H, Zhang W. Diagnostic value and clinical application of next-generation sequencing for infections in immunosuppressed patients with corticosteroid therapy. Ann Transl Med. 2020;8(5):227. doi:10.21037/atm.2020.01.30
[16] Cheng S, Tu Z, Zheng S, et al. An efficient SERS platform for the ultrasensitive detection of Staphylococcus aureus and Listeria monocytogenes via wheat germ agglutinin-modified magnetic SERS substrate and streptavidin/aptamer co-functionalized SERS tags. Anal Chim Acta. 2021;1187:339155. doi:10.1016/j.aca.2021.339155
[17] Wang W, Yang X, Rong Z, et al. Introduction of graphene oxide-supported multilayer-quantum dots nanofilm into multiplex lateral flow immunoassay: A rapid and ultrasensitive point-of-care testing technique for multiple respiratory viruses. Nano Res. 2023;16(2):3063-3073. doi:10.1007/s12274-022-5043-6
[18] Yang J, Hu X, Wang W, et al. RT-LAMP assay for rapid detection of the R203M mutation in SARS-CoV-2 Delta variant. Emerg Microbes Infect. 2022;11(1):978-987. doi:10.1080/22221751.2022.2054368

顾兵 教授
医学博士、教授、博士研究生导师,广东省人民医院检验科主任、学科带头人
美国普渡大学及UCLA访问学者,国家重点研发计划首席科学家、广东省“珠江人才计划项目”人才、江苏省“科教强卫”医学重点人才、“333工程”人才、“六大人才高峰”人才、“六个一工程”高层次卫生人才。现担任中国人体科技健康促进会临床微生物与感染精准检验专委会主委、中国医学装备协会检验医学分会副会长兼秘书长、中华医学会检验分会青委会委员、广东省临床基因检测质控中心主任、广东省医院协会微生物与临床感染专委会主委、广东省卫生经济学会检验经济分会会长、第三届国家人间传染的病原微生物实验室生物安全评审专家委员会委员、国家自然科学基金一审专家、AME学术沙龙总负责人。J Lab Precis Med执行主编,SCI期刊Ann Transl Med和J Thorac Dis编委,Annals of Infection主编。
从事重大传染病快速检测新技术与耐药菌感染防控研究,主持国家科技部重点研发计划2项、国家自然科学基金5项、省部级课题8项。以第一或通迅作者发表论文190篇,其中在Nano Research、Emerg Infect Dis、Biosens Bioelectron、Gut Microbes、PLoS Pathog、Emerg Microbes Infect、J Antimicrob Chemother、J Clin Microbiol等本领域权威期刊发表SCI论文119篇,其中JCR1区论文59篇,JCR2区论文32篇,10分以上12篇,累计影响因子652.936分,在中华级期刊发表论文17篇,H-index为35,被引频次总计5340余次;编写学术专著与教材40部,其中主编及副主编18部;获授权专利10项;获江苏省科学技术奖二等奖1项、江苏省医学科技奖三等奖1项、江苏省医学新技术引进奖6项。
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
.png)
责任编辑:彭伟彬
相关搜索: 感染标志物