- 首页 > 正文
黄曼教授:铜绿假单胞菌感染的诊治要点分析
感染医线 发表时间:2023/5/16 14:02:21
编者按:铜绿假单胞菌(PA)是临床常见的革兰阴性杆菌,在自然界广泛分布,可在人体皮肤表面分离到,还可污染医疗器械甚至消毒液,具有易定植、易变异和多耐药的特点。近年来,PA的流行病学、耐药情况不断发生变化,相关临床研究不断深入,新型抗菌药物研发上市,临床需要重新认识PA感染。本文中,浙江大学附属第二医院黄曼教授将为我们解析当前铜绿假单胞菌感染的诊治进展。
01
流行病学
铜绿假单胞菌(Pseudomonas aeruginosa,PA)是一种革兰阴性杆菌,也是临床最常见的非发酵菌,在自然界广泛分布,喜好潮湿环境。PA可作为正常菌群在人体皮肤表面分离到,还可污染医疗器械甚至消毒液,从而导致医源性感染,是医院获得性感染重要的条件致病菌,具有易定植、易变异和多耐药的特点。
PA是医院获得性肺炎(HAP)、呼吸机相关性肺炎(VAP)、社区获得性肺炎(CAP)的重要病原体。在我国HAP病原谱中,PA占16.9%~22.0%,居第2位,其中在≥65岁的患者中,PA比例更高,居第1位[1]。在我国呼吸机相关性肺炎病原谱中,PA占12.5%~27.5%,居第2位,其中在≥65岁的患者中,PA感染比例更高[2]。近期发表于《柳叶刀微生物》的一项研究[3]分析了2009年至2020年期间我国30个省的监测数据,结果显示PA是严重CAP患者最常见病原体之一,在18~60岁成年人中居第2位,在>60岁老年人中居首位。另一项前瞻性观察研究[4]显示,PA是与CAP死亡率相关的个体危险因素(单因素分析OR 3.78,95%CI:2.05~6.79,P<0.001;多因素分析OR 2.39,95%CI:1.02~5.59,P=0.045)。
随着抗生素的大量使用,PA的耐药菌株逐渐增多,给临床治疗带来了极大的难度。目前,世界卫生组织(WHO)已将碳青霉烯类耐药铜绿假单胞菌(CRPA)列为迫切需要研究和开发新抗生素的关键病原体;美国疾病控制中心(CDC)也将多重耐药铜绿假单胞菌(MDR-PA)列为严重威胁;同时,PA也被列为导致全球医院感染的ESKAPE(屎肠球菌、金黄色葡萄球菌、肺炎克雷伯菌、鲍曼不动杆菌、铜绿假单胞菌和肠杆菌)病原体之一。一项针对CRPA和相关碳青霉烯酶(KPC)的前瞻性队列研究[5]发现,KPC-2(23%)是我国最常见的KPC基因;在CRPA感染患者中,产KPC患者的30天死亡率高于非产KPC患者(22% vs 12%,校正差异7%,95%CI:1~14);与其他地区相比,中国患者获得有利DOOR结局(无临床应答、无出院或有再入院、肾功能衰竭或艰难梭菌感染)的概率更大。
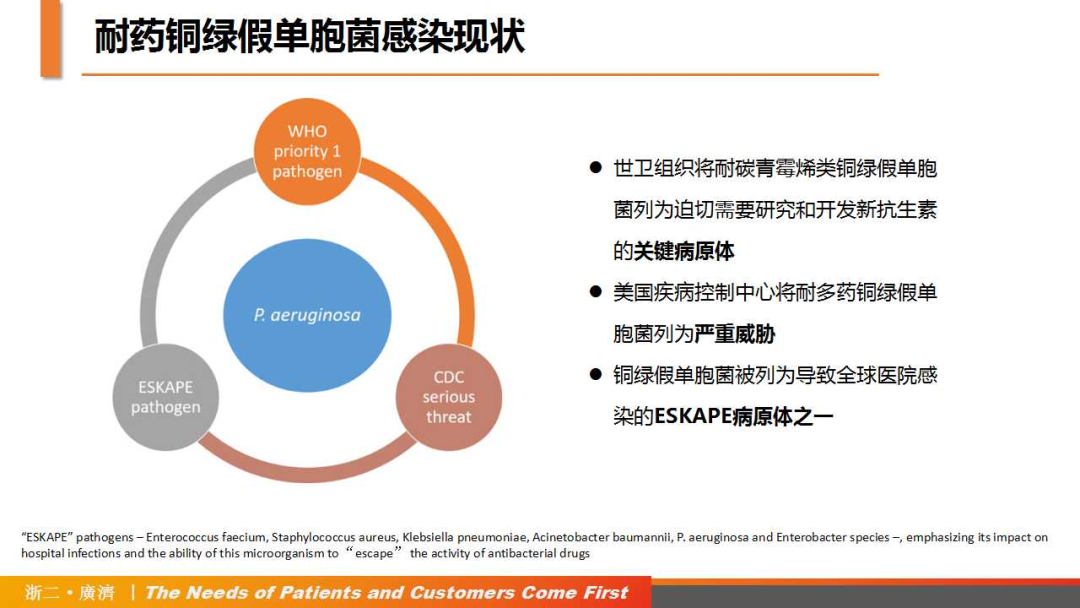
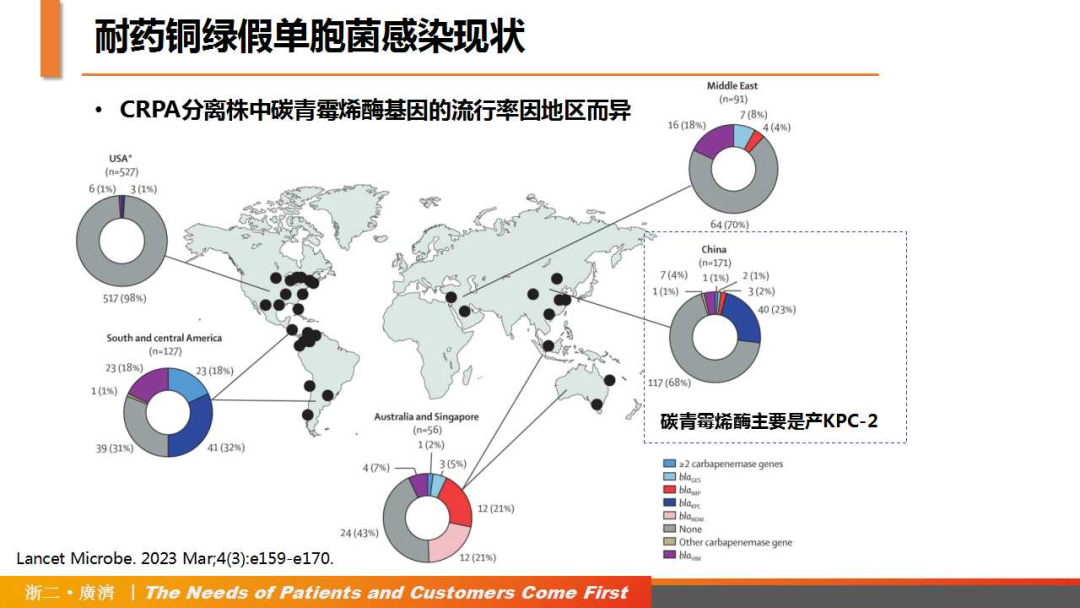
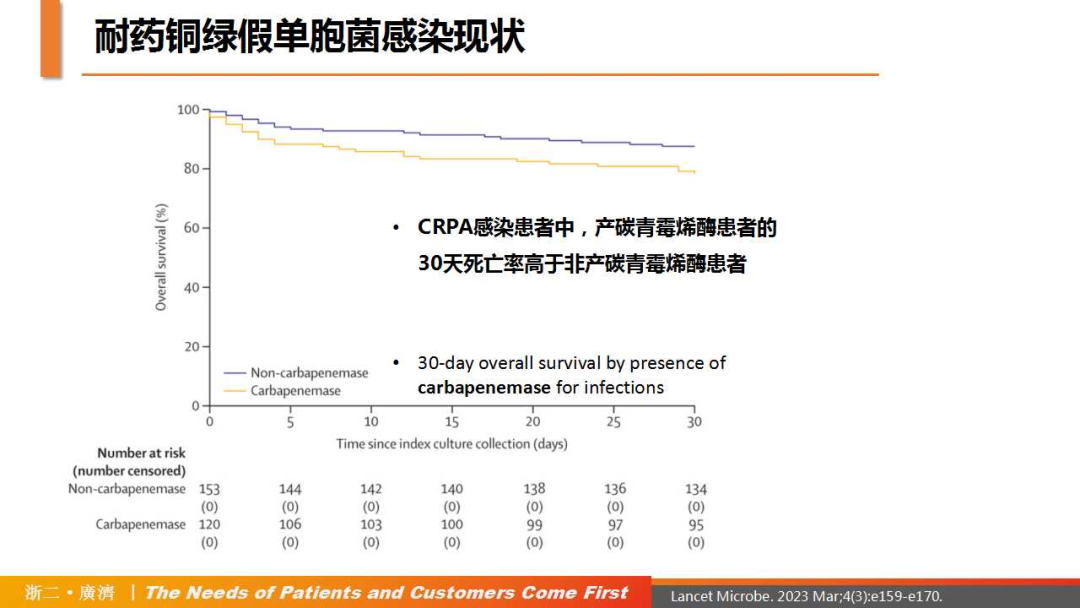
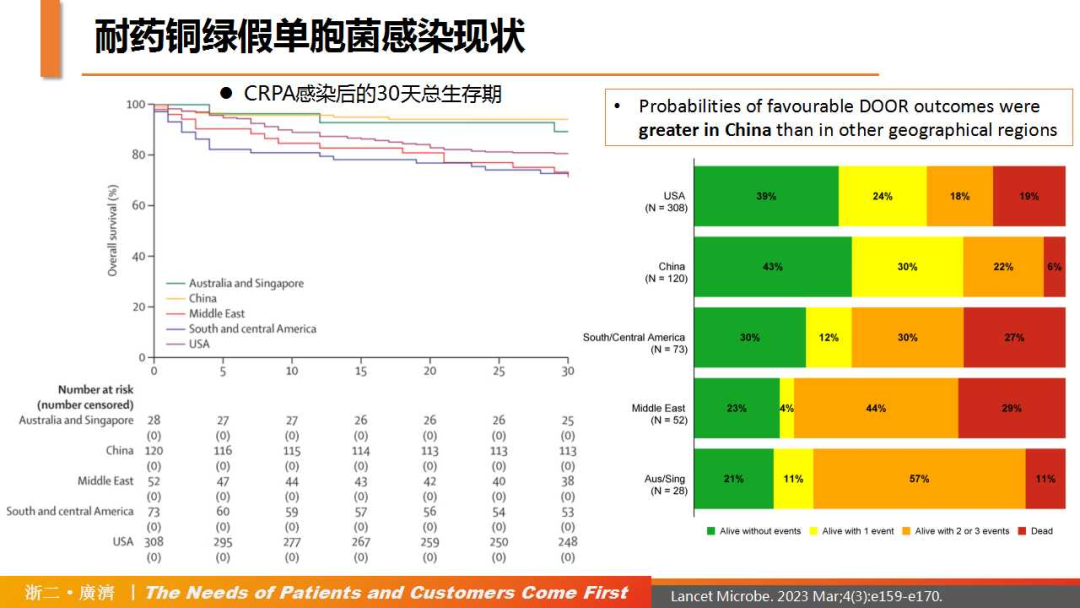
△耐药铜绿假单胞菌感染现状
(引自讲者幻灯)
02
病理机制
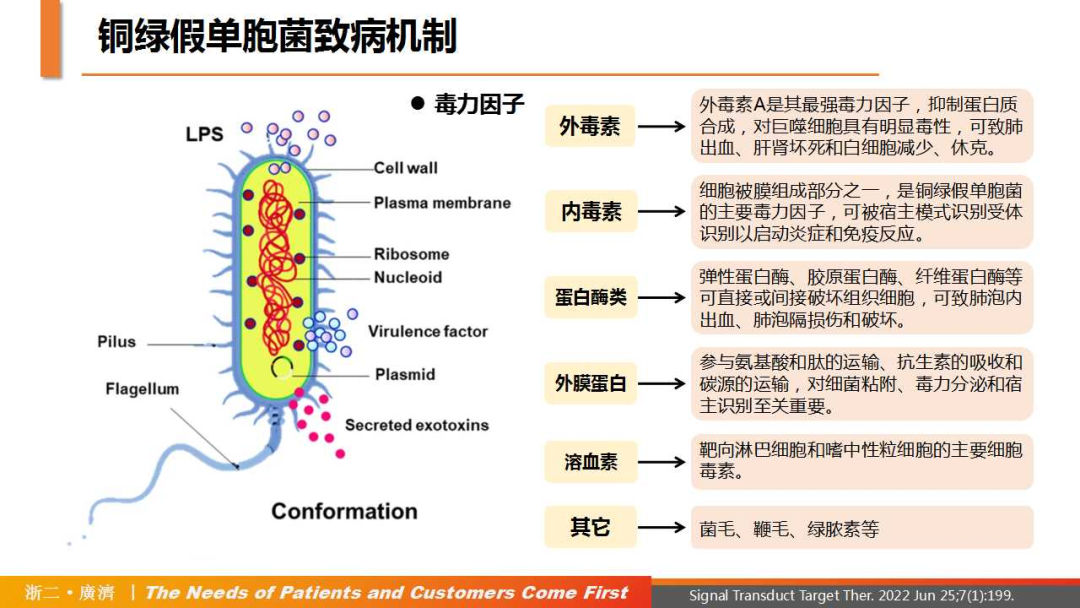
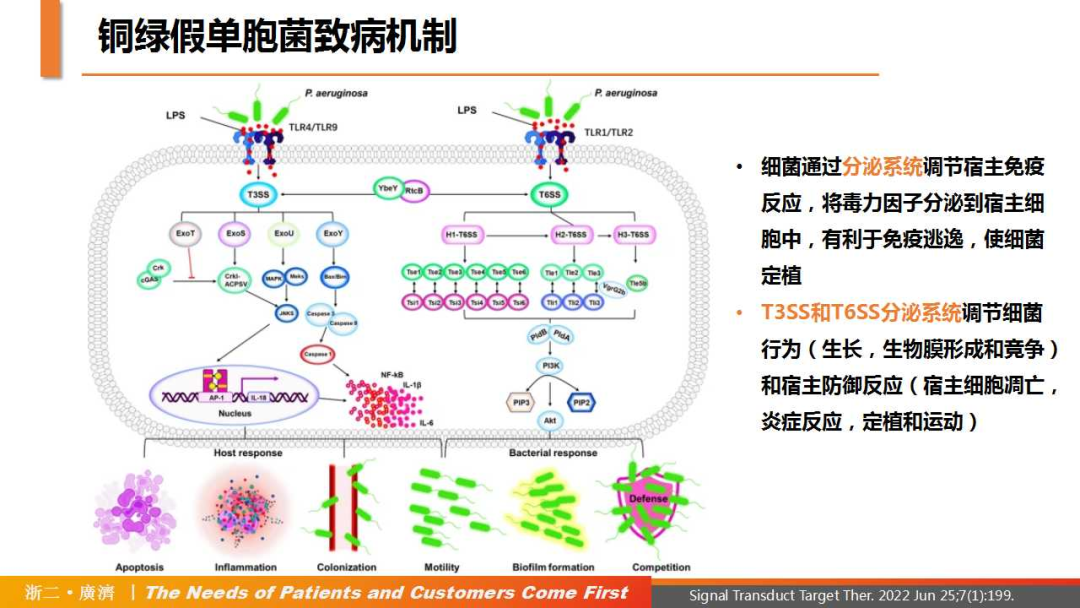
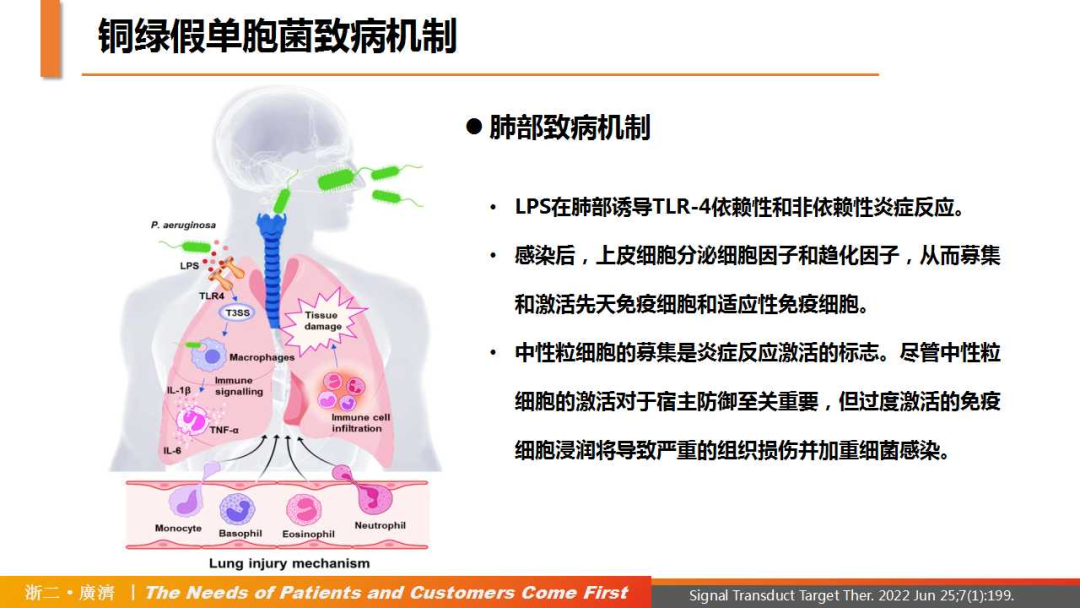
PA能够通过分泌多种毒力因子来适应宿主的不利环境[6],从而使宿主成功感染并致病,包括外毒素、内毒素、蛋白酶类、外膜蛋白、溶血素等。细菌通过分泌系统调节宿主免疫反应,将毒力因子分泌到宿主细胞中,有利于免疫逃逸,使细菌定植。T3SS和T6SS分泌系统调节细菌行为(生长、生物膜形成和竞争)和宿主防御反应(宿主细胞凋亡、炎症反应、定植和运动)。
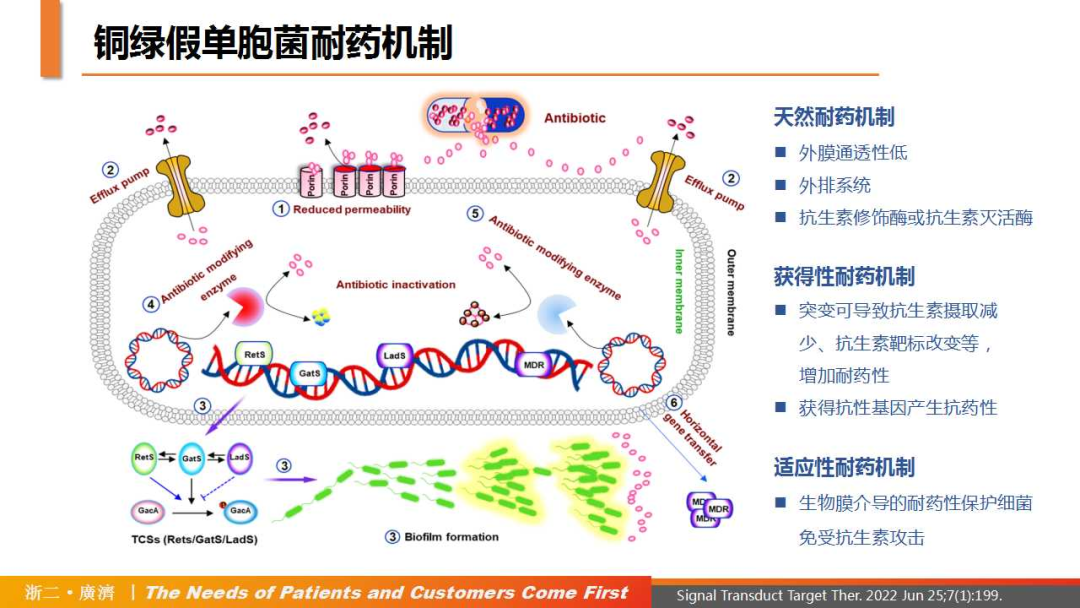
PA产生耐药性主要取决于多种抗生素耐药机制,主要包括天然耐药机制、获得性耐药机制和适应性耐药机制。因此,PA可以迅速对各种抗生素产生耐药性,如氨基糖苷类、喹诺酮类和β-内酰胺类。
△铜绿假单胞菌致病及耐药机制
(引自讲者幻灯)
03
临床表现与诊断
PA可感染机体许多部位,包括眼部、耳部、肺部、心脏、腹腔、泌尿系统、骨关节、皮肤与软组织等,感染部位与进入途径及患者的易感性有关。PA诊断的重点和难点在于区分感染与定植,临床工作中区别定植和感染非常困难,需根据患者的临床症状、体征、实验室检查、影像学改变等进行综合判断是否为感染,以下几点有助于鉴别:
- 阳性结果是否来自于合格的呼吸道标本;
- 是否具有PA感染的高危因素;
- 是否存在明确的下呼吸道感染诊断;
- PA出现的时间是否与下呼吸道感染发生或病情加重的时间相符合;
- 病情加重是否能够排除其他原因;
- 是否下呼吸道标本多次分离到PA,且未被经验性治疗所覆盖;
- 使用敏感药物抗PA治疗是否有效。
.png)
.png)
.png)
△铜绿假单胞菌感染诊断及高危因素
(引自讲者幻灯)
04
治疗与挑战
治疗原则
(1)选择有抗PA活性的抗菌药物,通常需要联合治疗;
(2)根据药代动力学(PK)/药效学(PD)理论选择正确的给药剂量和用药方式;
(3)充分的疗程;
(4)消除危险因素;
(5)重视抗感染外的综合治疗。
治疗目标
对于PA下呼吸道感染,急性和慢性患者的治疗目标是不同的:

治疗疗程
对于PA引起的VAP(PA-VAP)的最佳抗生素治疗时间尚无共识,有研究者开展了一项随机、对照、开放标签研究[7],旨在评估短程抗生素(8天)与长程抗生素治疗(15天)对PA-VAP的非劣效性,但该研究最终未能证明短程抗生素治疗PA-VAP的非劣效性。另一项关于PA菌血症治疗时间的回顾性多中心研究[8]结果显示,在存活率和复发率方面,短疗程(6~10天)和长疗程(11~15天)抗生素治疗PA菌血症一样有效,短疗程与住院时间短和停药次数少有关。一项来自韩国的回顾性研究[9]也得出了类似的结论,对于单纯性PA引起的菌血症,短疗程(7~11天)与长疗程(12~21天)一样有效。
.png)
.png)
.png)
△铜绿假单胞菌感染治疗疗程
(引自讲者幻灯)
抗菌药物及联合用药方案选择
PA感染的可选抗菌药物包括抗铜绿假单胞菌β-内酰胺类、喹诺酮类、氨基糖苷类和多粘菌素等。临床需根据患者自身状态、既往抗菌药物用药史、药敏试验结果等谨慎选择合理的治疗方案。
.png)
.png)
.png)
.png)
△抗菌药物及联合用药方案选择
(引自讲者幻灯)
头孢他啶/阿维巴坦
头孢他啶/阿维巴坦是由头孢他啶和阿维巴坦组成的新型酶抑制剂合剂,其中,头孢他啶是第三代头孢菌素(β-内酰胺类),通过与细菌细胞中的青霉素结合蛋白相结合抑制细胞壁合成从而杀灭细菌,阿维巴坦是一种新型β-内酰胺酶抑制剂,通过酰胺键与亲核进攻的β-内酰胺酶丝氨酸开环形成共价结合物,得到稳定的酶-抑制剂复合体,能有效阻止头孢他啶被β-内酰胺酶水解失活,保护头孢他啶对多种产KPC肠杆菌科菌株的抗菌活性[10]。
一项回顾性队列研究[11]评估了头孢他啶/阿维巴坦治疗多重耐药/广泛耐药(MDR/XDR)PA感染的有效性和安全性,结果显示第14天的临床治愈率为54.1%(aOR 0.84,95%CI:0.72~0.98,P=0.024),30天全因死亡率为13.1%,90天复发率为12.5%,未发现对头孢他啶/阿维巴坦的耐药性,治疗相关不良事件(TRAE)发生率为4.9%,头孢他啶/阿维巴坦是治疗MDR/XDR-PA感染的有效替代方案。
另一项研究[12]比较了头孢他啶/阿维巴坦与多黏菌素B对CRPA感染治疗的有效性,结果表明头孢他啶/阿维巴坦组的14天死亡率(5.9% vs 27.1%,P=0.002)、30天死亡率(13.7% vs 47.1%,P<0.001)和院内死亡率(29.4% vs 60.0%,P=0.001)均显著低于多黏菌素B组,细菌清除率(45.1% vs 12.9%,P<0.001)高于多黏菌素B组,头孢他啶/阿维巴坦治疗CRPA感染优于多黏菌素B,并提供了明显的生存优势。
.png)
.png)
.png)
.png)
△头孢他啶/阿维巴坦相关研究结果
(引自讲者幻灯)
预防与挑战
细菌耐药问题是全球面临的重大公共健康威胁,由耐药PA引起的感染在近几年逐渐增多,临床急切需要新的药物作为治疗选择。针对PA的新疗法主要从以下几个方向进行探索:噬菌体、免疫、基因编辑、抗菌肽以及疫苗。除了开发新疗法以外,还需要做好PA感染的预防工作,主要措施包括严格执行手卫生操作、接触预防、患者隔离、环境清洁消毒、器械物品的清洁消毒以及呼吸道去定植。
在PA耐药菌株全球播散、耐药机制复杂、新药研发需要充足时间等多种因素影响下,临床抗PA之路仍然任重道远。在新型药物问世前,我们要谨慎选择合理的治疗药物,避免出现无药可用的窘境。
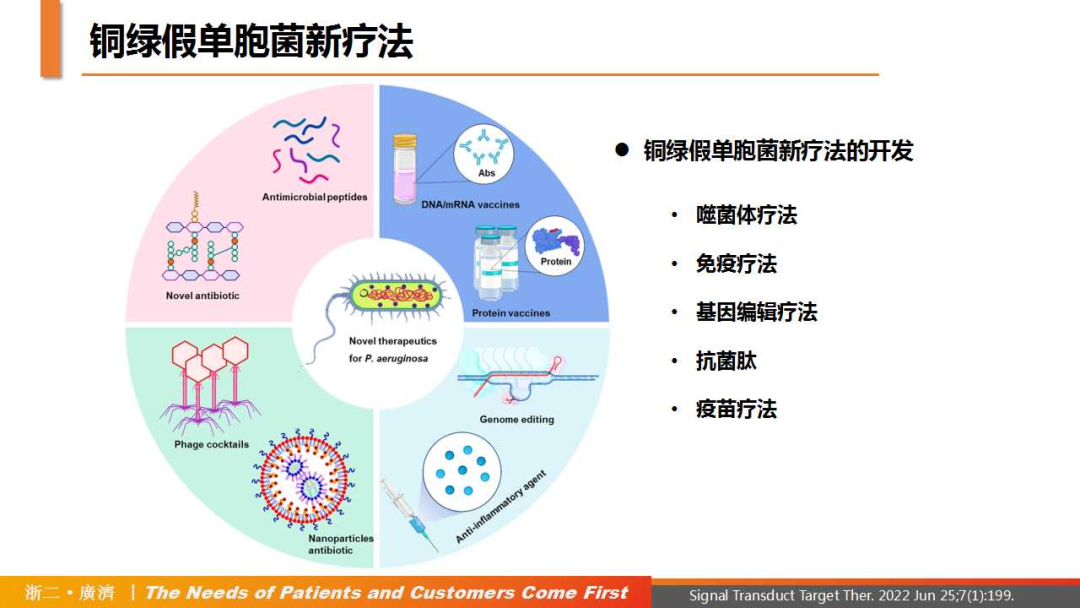
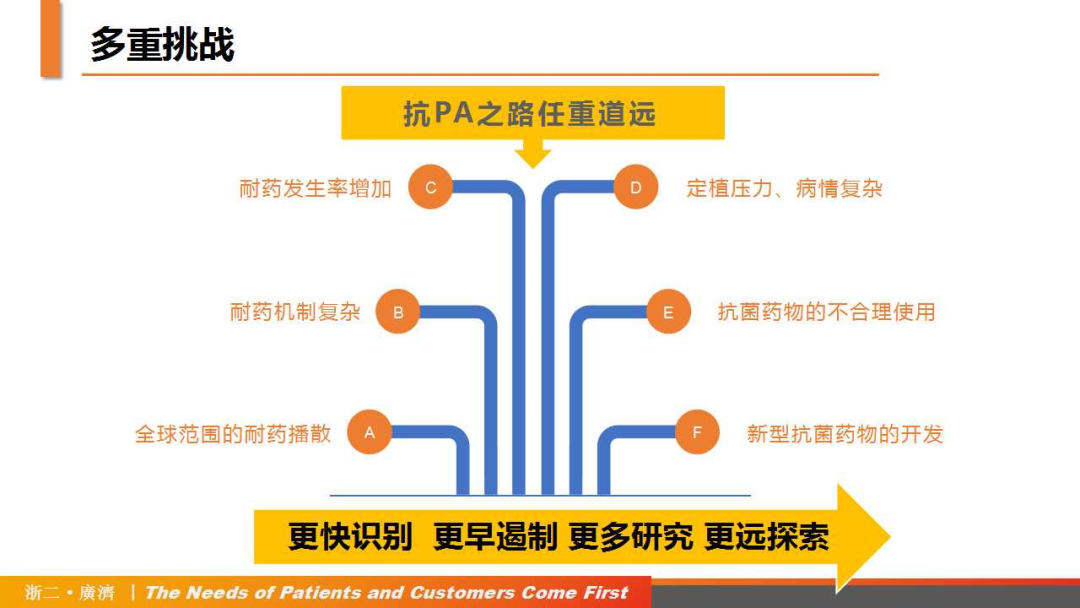
△铜绿假单胞菌新疗法的开发与挑战
(引自讲者幻灯)
参考文献
[1]中华医学会呼吸病学分会感染学组.中国成人医院获得性肺炎与呼吸机相关性肺炎诊断和治疗指南(2018年版)[J].中华结核和呼吸杂志,2018,41(4):255-280.
[2]瞿介明,施毅.中国成人医院获得性肺炎与呼吸机相关性肺炎诊断和治疗指南(2018年版)的更新与解读[J].中华结核和呼吸杂志,2018,41(4):244-246.
[3]Liu YN, Zhang YF, Xu Q, Qiu Y, Lu QB, Wang T, Zhang XA, Lin SH, Lv CL, Jiang BG, Li H, Li ZJ, Gao GF, Yang WZ, Hay SI, Wang LP, Fang LQ, Liu W; Chinese Center for Disease Control and Prevention Etiology Surveillance Study Team of Acute Respiratory Infections. Infection and co-infection patterns of community-acquired pneumonia in patients of different ages in China from 2009 to 2020: a national surveillance study. Lancet Microbe. 2023 Mar 28:S2666-5247(23)00031-9.
[4]Cillóniz C, Gabarrús A, Ferrer M, Puig de la Bellacasa J, Rinaudo M, Mensa J, Niederman MS, Torres A. Community-Acquired Pneumonia Due to Multidrug- and Non-Multidrug-Resistant Pseudomonas aeruginosa. Chest. 2016 Aug;150(2):415-25.
[5]Reyes J, Komarow L, Chen L, Ge L, Hanson BM, Cober E, Herc E, Alenazi T, Kaye KS, Garcia-Diaz J, Li L, Kanj SS, Liu Z, O?ate JM, Salata RA, Marimuthu K, Gao H, Zong Z, Valderrama-Beltrán SL, Yu Y, Tambyah P, Weston G, Salcedo S, Abbo LM, Xie Q, Ordo?ez K, Wang M, Stryjewski ME, Munita JM, Paterson DL, Evans S, Hill C, Baum K, Bonomo RA, Kreiswirth BN, Villegas MV, Patel R, Arias CA, Chambers HF, Fowler VG Jr, Doi Y, van Duin D, Satlin MJ; Antibacterial Resistance Leadership Group and Multi-Drug Resistant Organism Network Investigators. Global epidemiology and clinical outcomes of carbapenem-resistant Pseudomonas aeruginosa and associated carbapenemases (POP): a prospective cohort study. Lancet Microbe. 2023 Mar;4(3):e159-e170.
[6]Qin S, Xiao W, Zhou C, Pu Q, Deng X, Lan L, Liang H, Song X, Wu M. Pseudomonas aeruginosa: pathogenesis, virulence factors, antibiotic resistance, interaction with host, technology advances and emerging therapeutics. Signal Transduct Target Ther. 2022 Jun 25;7(1):199.
[7]Bouglé A, Tuffet S, Federici L, Leone M, Monsel A, Dessalle T, Amour J, Dahyot-Fizelier C, Barbier F, Luyt CE, Langeron O, Cholley B, Pottecher J, Hissem T, Lefrant JY, Veber B, Legrand M, Demoule A, Kalfon P, Constantin JM, Rousseau A, Simon T, Foucrier A; iDIAPASON Trial Investigators. Comparison of 8 versus 15 days of antibiotic therapy for Pseudomonas aeruginosa ventilator-associated pneumonia in adults: a randomized, controlled, open-label trial. Intensive Care Med. 2022 Jul;48(7):841-849.
[8]Babich T, Naucler P, Valik JK, Giske CG, Benito N, Cardona R, Rivera A, Pulcini C, Fattah MA, Haquin J, Macgowan A, Grier S, Chazan B, Yanovskay A, Ami RB, Landes M, Nesher L, Zaidman-Shimshovitz A, McCarthy K, Paterson DL, Tacconelli E, Buhl M, Mauer S, Rodríguez-Ba?o J, de Cueto M, Oliver A, de Gopegui ER, Cano A, Machuca I, Gozalo-Marguello M, Martinez-Martinez L, Gonzalez-Barbera EM, Alfaro IG, Salavert M, Beovic B, Saje A, Mueller-Premru M, Pagani L, Vitrat V, Kofteridis D, Zacharioudaki M, Maraki S, Weissman Y, Paul M, Dickstein Y, Leibovici L, Yahav D. Duration of Treatment for Pseudomonas aeruginosa Bacteremia: a Retrospective Study. Infect Dis Ther. 2022 Aug;11(4):1505-1519.
[9]Bae M, Jung J. Short versus prolonged courses of antimicrobial therapy for patients with uncomplicated Pseudomonas aeruginosa bloodstream infection: a retrospective study-authors' response. J Antimicrob Chemother. 2022 Feb 23;77(3):859-860.
[10]Shirley M. Ceftazidime-Avibactam: A Review in the Treatment of Serious Gram-Negative Bacterial Infections. Drugs. 2018 Apr;78(6):675-692.
[11]Corbella L, Boán J, San-Juan R, Fernández-Ruiz M, Carretero O, Lora D, Hernández-Jiménez P, Ruiz-Ruigómez M, Rodríguez-Goncer I, Silva JT, López-Medrano F, Lizasoain M, Villa J, Caro-Teller JM, Aguado JM. Effectiveness of ceftazidime-avibactam for the treatment of infections due to Pseudomonas aeruginosa. Int J Antimicrob Agents. 2022 Feb;59(2):106517.
[12]Chen J, Liang Q, Chen X, Wu J, Wu Y, Teng G, Huang M. Ceftazidime/Avibactam versus Polymyxin B in the Challenge of Carbapenem-Resistant Pseudomonas aeruginosa Infection. Infect Drug Resist. 2022 Feb 25;15:655-667.

黄曼 教授
现任浙江大学医学院附属第二医院综合ICU主任医师,肺移植科常务副主任(主持工作),烧创伤党总支书记,综合ICU党支部书记
目前是浙江大学医学院博士生导师,浙江大学医学院附属第二医院综合ICU科室主任,同时担任浙江《中华急诊医学杂志》编委、中国研究型医院休克脓毒症学会委员、中国医促会急诊急救分会委员、浙江省重症医学分会委员。重症感染、多脏器功能衰竭的诊治及脓毒症脑病、脓毒症肾病的发病机制,关注危重病人评估及监测,在重症患者的血液净化治疗(人工肝、人工肾)领域有深入研究,具备良好的科研能力及医疗质量管理背景
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。

责任编辑:彭伟彬
相关搜索: 铜绿假单胞菌