- 首页 > 正文
谷丽教授:优中选优,解锁COVID-19防治困局
感染医线 发表时间:2023/6/20 16:31:08
编者按:
COVID-19是由SARS-CoV-2引起的一种传染病,至今仍在全球范围内不断蔓延,对人类健康和生命造成了严重威胁。为降低COVID-19的重症转化率和病死率,各国紧急批准了多种COVID-19疫苗和新型抗病毒药物。在治疗药物方面,一些药物存在明显的局限性,还有一些药物的临床疗效尚未得到充分验证,这为我们的临床实践带来了一定的困扰。在近期举办的第十六届北京感染病和肝病论坛中,首都医科大学附属北京朝阳医院谷丽教授带来了“卓眼未来实力无限-从RCT到RWE双重印证新冠防治优选方案”的精彩演讲,《感染医线》整理如下。
解锁COVID-19防治困局
2019冠状病毒病(COVID-19)是由SARS-CoV-2病毒引起的一种传染病,任何年龄人群均有可能患病。保持社交距离、佩戴口罩、勤洗手等是保护自己和他人免受感染的重要防护措施。基于RT-PCR的诊断工具在COVID-19大流行早期就被开发出来,并紧急用于病例检测、追踪和隔离[1]。目前,全球已有多款mRNA疫苗、灭活疫苗和病毒载体疫苗问世[1]。与此同时,针对COVID-19的治疗药物也在以多种方式进行研发,包括“老药新用”、恢复期血浆疗法、单克隆抗体和小分子创新药物开发等[1]。
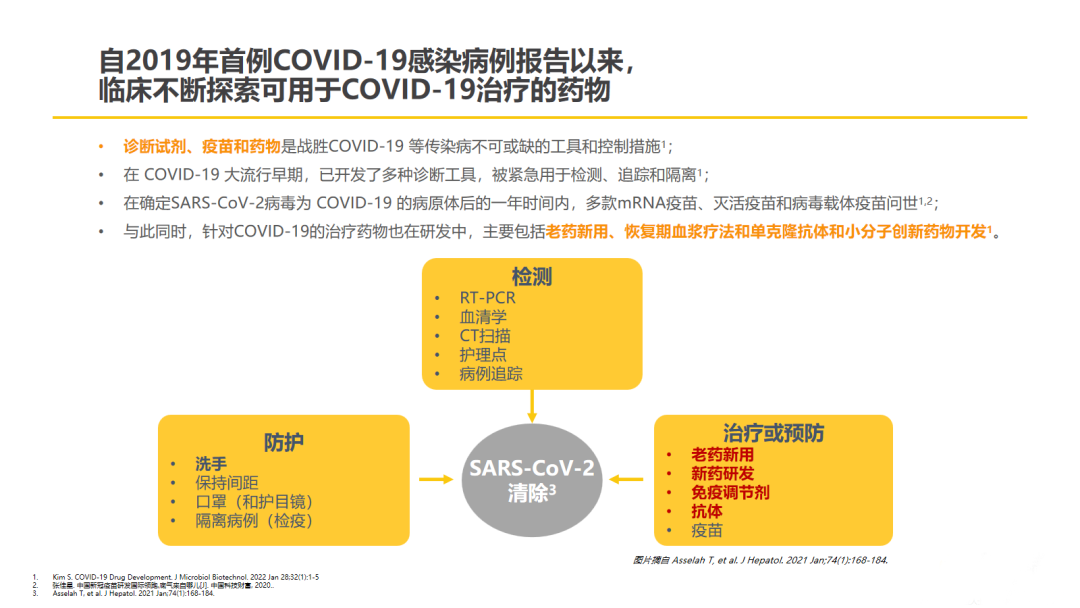
△SARS-CoV-2的防控措施
(引自讲者幻灯)
目前COVID-19治疗策略主要有“靶向病毒”和“靶向宿主”两大类。“靶向病毒”的药物主要以单克隆抗体和小分子抗病毒治疗药物为主。单克隆抗体的开发速度比小分子抑制剂更快,其抗病毒机制是通过中和感染性病毒颗粒来阻断病毒进入,如Bamlanivimab、Bamlanivima/etesevimab、Casirivimab/imdevimab等。由于中和能力依赖于抗体和病毒刺突蛋白之间的相互作用,因此病毒变异株的出现可能会削弱单克隆抗体的中和能力[1],这也限制了单克隆抗体的开发与应用。小分子抗病毒治疗药物主要通过抑制SARS-CoV-2病毒复制来发挥治疗作用,如瑞德西韦、法匹拉韦、利巴韦林等。但考虑到部分药物存在药物相互作用,为保证患者用药的安全性,还需要进一步分析药物的药代动力学特性、代谢途径和药效学等[2]。

△现有COVID-19治疗药物的局限性
(引自讲者幻灯)
莫诺拉韦是全球首个用于COVID-19的小分子口服药物,目前已在40多个国家获批或获得紧急使用授权。莫诺拉韦是核糖核苷类似物EIDD-1931的口服生物可利用的异丙酯前药,莫诺拉韦作为RNA依赖的RNA聚合酶(RdRp)的底物,参与病毒RNA的合成,通过与RdRp活性中心的G或A形成稳定的碱基对,导致病毒RNA复制错误,从而阻断新冠病毒复制[3]。
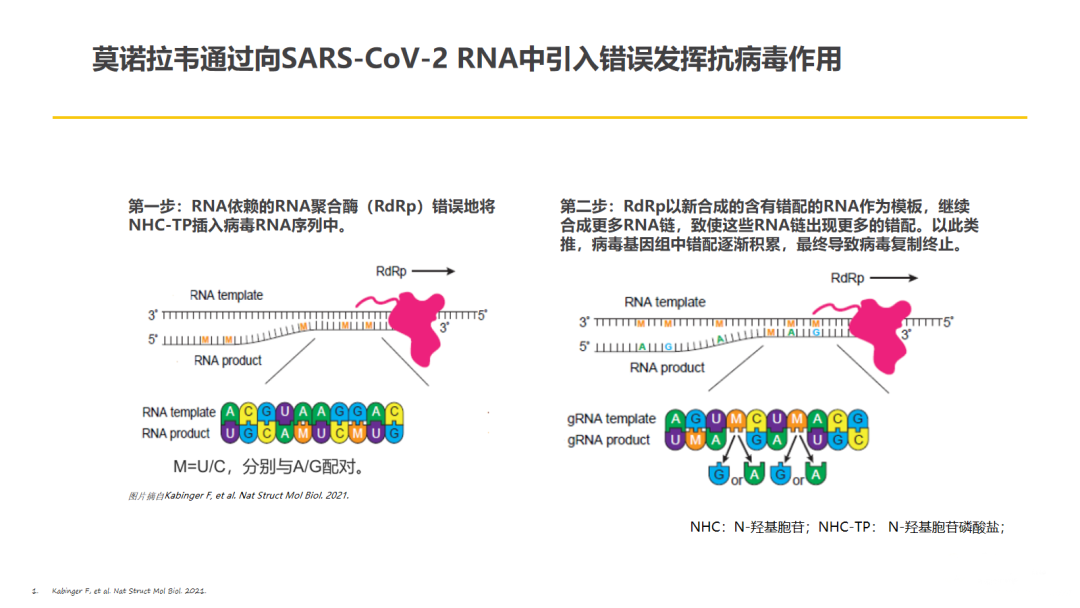
△莫诺拉韦抗病毒作用机制
(引自讲者幻灯)
随机对照试验证据
2020年4月,美国批准莫诺拉韦新药临床试验申请,Ⅰ期研究随即启动;2021年11月,莫诺拉韦已在美国、日本、欧盟、英国等多国获批[4];2022年12月29日,我国国家药品监督管理局附条件批准莫诺拉韦进口注册[5]。关于药物的有效性和安全性,MOVe-OUT研究[6]已为我们提供较为详实的临床数据。
MOVe-OUT研究是一项随机、安慰剂对照、双盲的Ⅲ期临床试验,旨在评估莫诺拉韦治疗轻至中度COVID-19非住院患者的疗效和安全性。纳入标准:非住院、未接种疫苗、轻度至中度实验室确诊的COVID-19、伴有至少一个潜在重症高风险因素、随机分组前5天内出现症状的成年患者。研究对象为来自20个国家的107家中心的1433例患者,患者随机接受莫诺拉韦(800 mg)或安慰剂治疗(每天两次,为期5天),随访至第29天。主要终点为至第29天的全因住院率/死亡率以及不良事件的发生率。次要终点包括至第29天COVID-19症状和体征的改善情况、症状和体征持续缓解或减轻的时间、症状和体征进展的时间。探索性终点为SARS-CoV-2病毒载量自基线的平均变化。
研究结果显示,与安慰剂组相比,接受莫诺拉韦治疗的患者住院或死亡的比例更低(6.8% vs 9.7%,差异3%,95%CI:-5.9~-0.1)。莫诺拉韦组29天全因死亡率低于安慰剂组(0.1% vs 1.3%),死亡风险比安慰剂组低89%(95%CI:14~99)。此外,MOVe-OUT研究事后病毒学分析[7]显示,在基线及治疗期间留有病毒学检测记录的193例(莫诺拉韦组96例,安慰剂组97例)患者中,接受莫诺拉韦治疗的患者,无论其是否伴有免疫缺陷,均可在治疗第3天“清除”传染性病毒颗粒,在后续的随访中也均未检测到传染性病毒颗粒。不良事件方面,莫诺拉韦组(n=216,30.4%)与安慰剂组(n=231,33.0%)相当。被判定为与试验方案相关的常见不良事件包括腹泻、恶心和头晕。
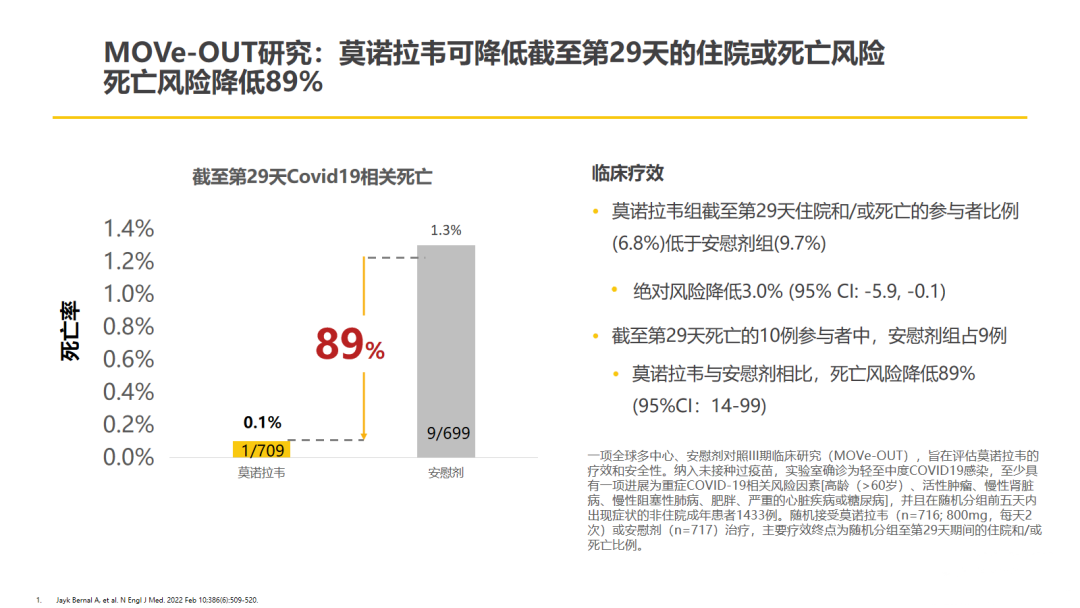
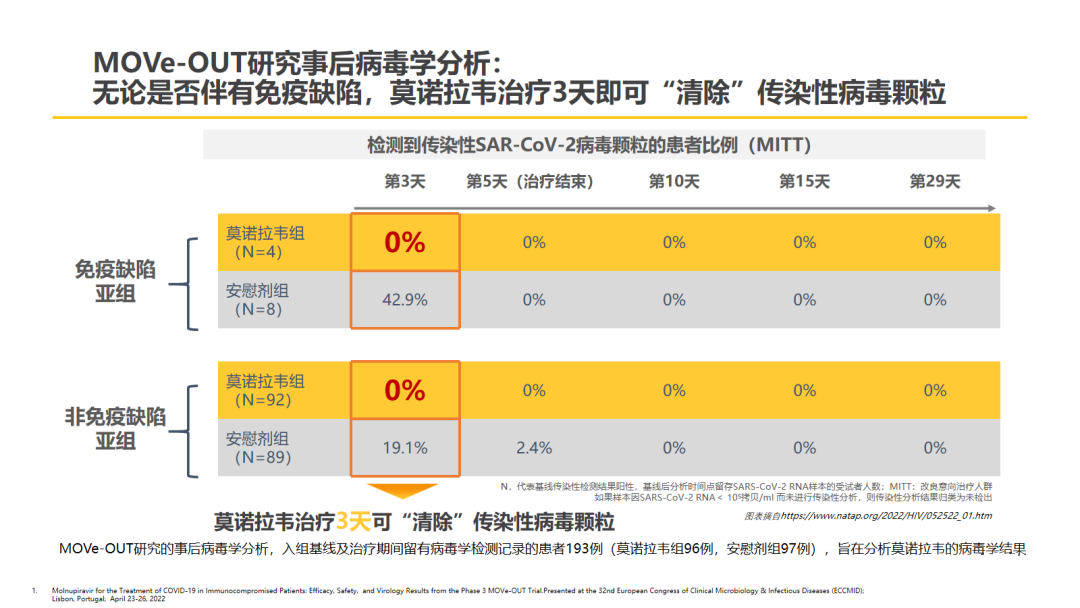
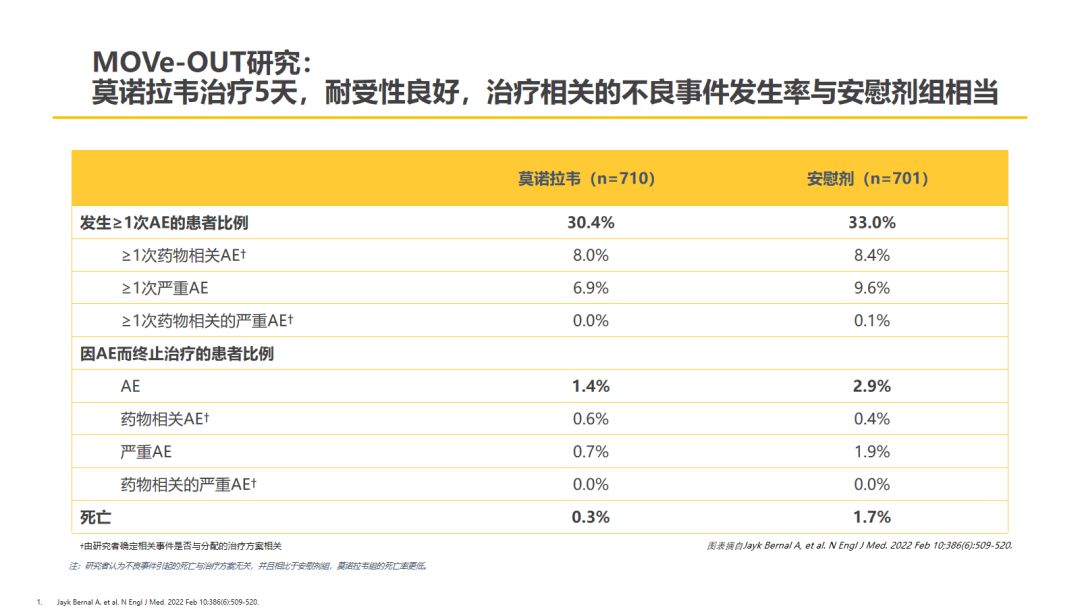
△MOVe-OUT研究结果
(引自讲者幻灯)
多国真实世界证据
为进一步了解莫诺拉韦对于奥密克戎变异株的疗效,多国开展了真实世界研究。中国香港一项回顾性队列研究[8]分析了2022年2月26日至4月26日(奥密克戎流行期间)因确诊COVID-19感染而住院的40776例患者,所有纳入研究的患者入院时均未接受氧疗,将患者分为莫诺拉韦队列(n=2551)、奈玛特韦/利托那韦队列(n=1096)以及未接受莫诺拉韦或奈玛特韦/利托那韦治疗的对照队列(n=37129),进行1:1倾向评分匹配后,分析各队列的全因死亡率、疾病进展的复合结局、个体疾病进展结局、达到低病毒载量的时间(RT-PCR 循环阈值≥30)。结果显示,与对照组相比,使用莫诺拉韦治疗可降低全因死亡(HR 0.48,95%CI:0.40~0.59,P<0.0001)和疾病进展复合结局终点风险(HR 0.60,95%CI:0.52~0.69,P<0.0001)。
一项在日本进行的真实世界、回顾性队列研究[9]评估了日本福岛县奥密克戎流行期间莫诺拉韦治疗COVID-19的疗效。研究纳入了2022年1月至4月期间入院的轻度至中度COVID-19患者。经过1:3倾向评分匹配后,比较了莫诺拉韦使用者(n=230)与非使用者(n=690)入院后的临床恶化情况。结果显示,与非使用者相比,使用莫诺拉韦治疗的患者临床恶化率明显更低(3.90% vs 8.40%,P=0.034)。多变量logistic回归分析表明,接受莫诺拉韦治疗是防止病情恶化的因素之一(OR 0.448,95%CI:0.206~0.973,P=0.042),且不受其他协变量影响。
以色列的一项真实世界研究[10]探讨了奥密克戎流行期间莫诺拉韦在重症高危患者中的有效性。研究纳入了在2022年1月至2月期间确诊COVID-19的成年患者(无论是否接种疫苗),患者伴有至少1种进展为重症COVID-19的高危因素。将莫诺拉韦组患者与非莫诺拉韦组(对照组)患者以1:1的比例进行倾向评分匹配,最终两组各匹配2661例患者。对患者进行为期28天的随访,观察两组患者重症COVID-19或COVID-19特异性死亡的情况以及二者组成的复合终点。结果显示,对于总体人群,莫诺拉韦治疗未显著降低复合终点、COVID-19重症和COVID-19特异性死亡风险。但亚组分析显示,在高龄(HR 0.54,95%CI:0.34~0.86,P=0.018)、女性(HR 0.41,95%CI:0.22~0.77,P=0.003)和疫苗接种不足(HR 0.45,95%CI:0.25~0.82,P=0.006)的亚组人群中,莫诺拉韦与复合终点风险显著降低有关。
另一项来自波兰的研究[11]旨在评估在奥密克戎流行期间莫诺拉韦在COVID-19住院患者(特别是老年人)中的疗效。从SARSTer国家数据库纳入了590例在2022年1月1日至4月30日期间住院的COVID-19确诊患者。其中203例接受莫诺拉韦治疗,387例未接受任何抗病毒治疗(对照组)。疗效终点为28天死亡率和需要机械通气的患者比例。结果显示,与对照组相比,莫诺拉韦可显著降低死亡率(9.9% vs 16.3%,P=0.03),在80岁以上(症状出现5天内)的患者中尤为显著(14.6% vs 35.2%,P=0.016)。莫诺拉韦治疗并不影响需要机械通气的频率,但接受莫诺拉韦治疗的患者需要氧气补充的频率明显低于对照组患者(31.7% vs 49.2%,P=0.00005)。
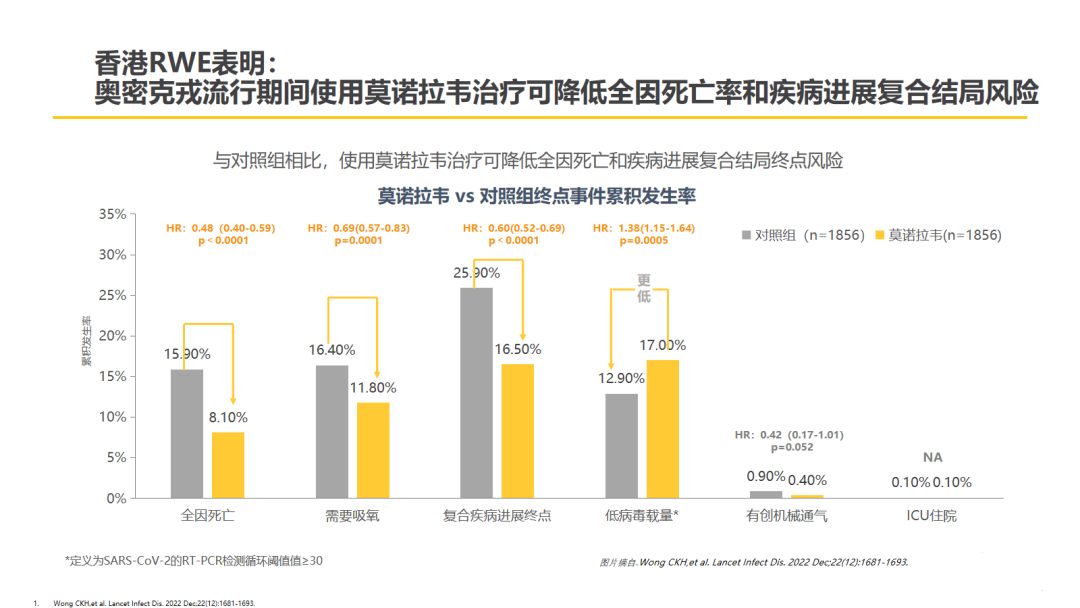
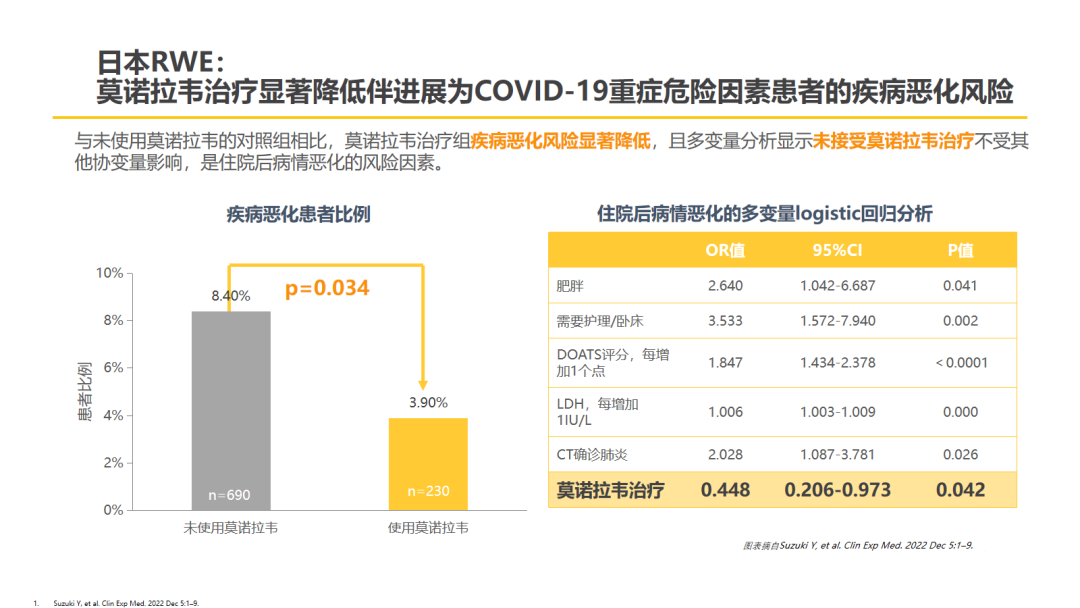
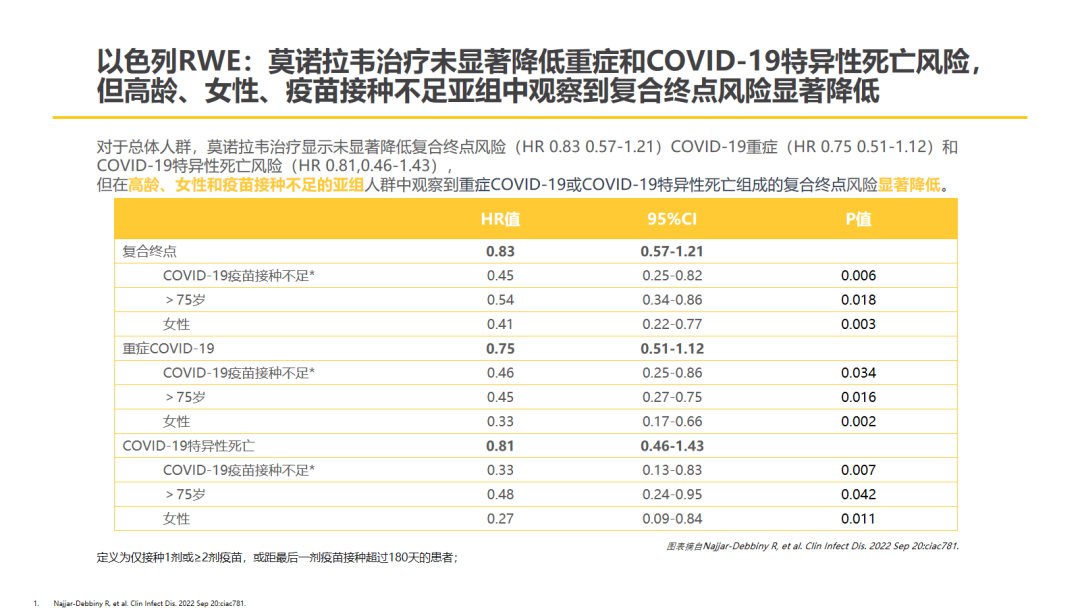
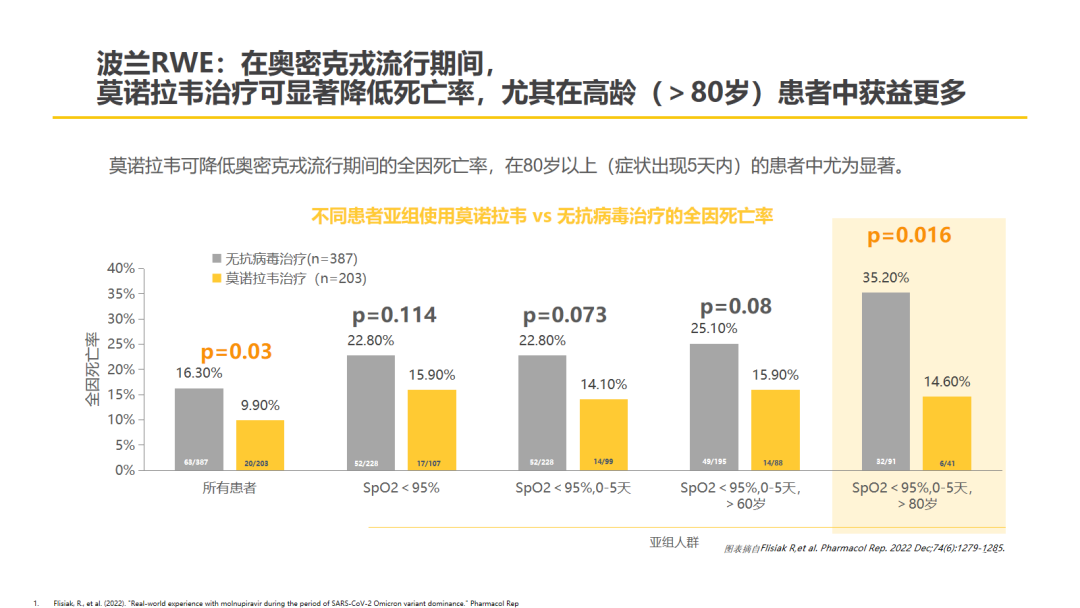
△中国香港、日本、以色列、波兰真实世界研究
(引自讲者幻灯)
总结
MOVe-OUT研究为我们提供了莫诺拉韦可降低COVID-19患者死亡风险的循证依据,来自多国的真实世界研究进一步探索了其在奥密克戎变异株中的应用效果,良好的疗效和安全性为我们今后的临床实践带来了更强的信心,我们也期待获得更多真实世界的应用数据。莫诺拉韦具有给药方式便捷、可降低重症和死亡风险、对变异株有效等优点,是治疗COVID-19较为理想的药物,希望这一药物能惠及更多的患者。

谷丽 教授
主任医师
首都医科大学附属北京朝阳医院
感染和临床微生物科主任
中国医疗保健国际交流促进会临床微生物与感染分会委员
北京医学会感染分会委员
参考文献
上下滑动查看更多内容
[1] Kim S. COVID-19 Drug Development. J Microbiol Biotechnol. 2022;32(1):1-5.
[2] Jeong E, Nelson SD, Su Y, Malin B, Li L, Chen Y. Detecting drug-drug interactions between therapies for COVID-19 and concomitant medications through the FDA adverse event reporting system. Front Pharmacol. 2022;13:938552.
[3] 张福杰,王卓,王全红,等.新型冠状病毒感染者抗病毒治疗专家共识[J].中华临床感染病杂志,2023,16(1):10-20.
[4] Syed YY. Molnupiravir: First Approval. Drugs. 2022;82(4):455-460.
[5] 国家药品监督管理局.国家药监局应急附条件批准默沙东公司新冠病毒治疗药物莫诺拉韦胶囊进口注册[EB/OL]. (2022-12-30). https://www.nmpa.gov.cn/yaowen/ypjgyw/20221230152354151.html
[6] Jayk Bernal A, Gomes da Silva MM, Musungaie DB, et al. Molnupiravir for Oral Treatment of Covid-19 in Nonhospitalized Patients. N Engl J Med. 2022;386(6):509-520.
[7] Johnson MG, Strizki JM, Brown ML, et al. Molnupiravir for the treatment of COVID-19 in immunocompromised participants: efficacy, safety, and virology results from the phase 3 randomized, placebo-controlled MOVe-OUT trial [published online ahead of print, 2023 Jan 17]. Infection. 2023;1-12.
[8] Wong CKH, Au ICH, Lau KTK, Lau EHY, Cowling BJ, Leung GM. Real-world effectiveness of early molnupiravir or nirmatrelvir-ritonavir in hospitalised patients with COVID-19 without supplemental oxygen requirement on admission during Hong Kong's omicron BA.2 wave: a retrospective cohort study. Lancet Infect Dis. 2022;22(12):1681-1693.
[9] Suzuki Y, Shibata Y, Minemura H, et al. Real-world clinical outcomes of treatment with molnupiravir for patients with mild-to-moderate coronavirus disease 2019 during the Omicron variant pandemic [published online ahead of print, 2022 Dec 5]. Clin Exp Med. 2022;1-9.
[10] Najjar-Debbiny R, Gronich N, Weber G, et al. Effectiveness of Molnupiravir in High-Risk Patients: A Propensity Score Matched Analysis. Clin Infect Dis. 2023;76(3):453-460.
[11] Flisiak R, Zar?bska-Michaluk D, Rogalska M, et al. Real-world experience with molnupiravir during the period of SARS-CoV-2 Omicron variant dominance [published correction appears in Pharmacol Rep. 2022 Oct 3;:]. Pharmacol Rep. 2022;74(6):1279-1285.
《感染医线》整理/谷丽教授校审
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。

责任编辑:彭伟彬
相关搜索: COVID-19