- 首页 > 正文
小小氟原子 抗菌大不同丨首个氟环素类抗菌药依拉环素登陆中国,抗感染治疗增添新利器
感染医线 发表时间:2023/7/20 15:36:52
随着抗菌药物的广泛应用,细菌耐药问题也愈演愈烈,即使是在严重感染和多重耐药菌感染中大展身手的碳青霉烯类药物,也面临耐药问题日趋严重的尴尬境地。研发新型抗菌药物,是当前临床应对耐药问题迫在眉睫的“刚需”。2023年3月16日,新型抗菌药依拉环素(依嘉®)通过国家药品监督管理局(NMPA)附条件批准上市。作为全球首个氟环素类抗菌药,依拉环素以其广谱、抗菌活性强、组织浓度高、联合用药有协同相加作用等药物优势,将成为临床医生抗感染治疗“兵器谱”中的“重器”。在依拉环素即将走进我国临床实践之际,《感染医线》特邀中山大学附属第一医院罗益锋教授介绍依拉环素的药物特征,总结当前国内外的循证医学证据。
细菌耐药:
悬在头顶的达摩克利斯之剑
抗菌药耐药(AMR)已经成为悬在人类头顶的“达摩克利斯之剑”,对生命健康带来巨大的威胁。相关数据显示,2019年全球约有93万例死亡归因于AMR,357万例死亡与AMR相关[1];到2050年,AMR相关死亡病例将达1000万[2]。值得注意的是,在致死的前6位耐药细菌中,有4个是革兰阴性耐药菌(大肠埃希菌、肺炎克雷伯菌、鲍曼不动杆菌、铜绿假单胞菌)[1]。也有学者认为,多重耐药或广泛耐药(MDR/ XDR)的革兰阴性菌呼吸道感染,有可能成为另一场大流行(Another pandemic)[3]。
碳青霉烯耐药革兰阴性菌(CRO)感染的形势尤其不容乐观,CHINET监测数据显示碳青霉烯耐药肺炎克雷伯菌(CRKP)、碳青霉烯耐药鲍曼不动杆菌(CRAB)的检出率分别高达25%和70%以上[4]。美国CDC和世卫组织则将CRAB、碳青霉烯耐药肠杆菌(CRE)分别列为急迫威胁(Urgent threats)和关键病原体(Critical pathogens),强调开发新型抗菌药物的紧迫性。
然而,当前我国临床实践中用于MDR或CRO治疗的药物选择十分有限,且治疗限制较多。例如,《碳青霉烯耐药肠杆菌科细菌感染诊治与防控专家共识》[5]指出:多黏菌素易发生异质性耐药,且有明显的肾脏和神经系统毒性,肺组织渗透性低;替加环素的血药浓度较低,且对肝功能和凝血影响大,有黑框警示;头孢他啶-阿维巴坦对产金属酶菌株感染无效;氨基糖苷类的治疗效果欠佳,且耳、肾毒性较大。
应对细菌耐药,是一场没有硝烟的战役。在治疗选择有限的窘境下,我们亟需更多新型药物作为有力“武器”。
横空出世:
首个氟环素类抗菌药依拉环素
细数MDR/CRO抗感染治疗的“兵器谱”,第三代四环素仍是重要选择,但也存在各种各样的不足。数十年来,科学家一直致力于四环素的结构改造。然而,传统的生物合成和半合成法因难度大、结构变化受限等因素,极大限制了对四环素类抗菌药改造的发展空间。2005年,一种新的四环素类抗菌药物的合成方法——全合成法发布,该方法允许在四环素D环上的更多位点(包括C7、C8和C9)引入更多样化的取代基,可将杂环和多环引入到四环素的基本结构中,为新型药物的研发带来了更多可能[6]。
与此同时,喹诺酮类药物诺氟沙星成功在分子中引入氟,这种新的药物优化改构策略受到重视。系列研究发现,氟原子的引入可显著改变分子构象、药物解离常数(PKa)、活性、渗透性、代谢途径和药代动力学特性[7]。研究人员陆续发现,氟原子的引入:(1)可调节药物的酸碱性,提高药物的生物利用度;(2)通过调节亲脂性、与氢键结合或降低胺的碱性,影响药物的渗透性,进而改善组织分布;(3)改善药物在体内的代谢稳定性,从而降低临床使用剂量[7-8]。
全合成及氟改构的药物工艺发展成熟,促使全球首个氟环素类抗菌药物——依拉环素的横空出世。依拉环素通过对核心D环的独特修饰[9],包括氟原子取代C-7处的二甲胺部分、吡咯烷乙酰氨基取代C-9处的2-叔丁基甘氨酰胺基[10],使其具有更强的抗菌活性,并有效改善药物的渗透性、组织分布以及代谢稳定性。

△四环素的发展历程及首个氟环素类药物依拉环素的化学结构式
脱胎换骨:
依拉环素药物性能的全面提升
对核心D环引入氟原子修饰,犹如神来之笔,使得依拉环素的药物性能得到全面提升。
抗菌谱广,可覆盖不同类型耐药细菌
体外研究显示,依拉环素对不同类型的细菌病原体几乎“通杀”,可以覆盖革兰阴性菌(铜绿假单胞菌除外)、革兰阳性菌、厌氧菌和非典型病原体。
更重要的是,依拉环素对多种耐药细菌也“毫不示弱”,其抗菌活性不受或极少受常见四环素类外排泵(tetA,tetB,tetK)和核糖体保护蛋白(tetM)耐药基因的影响[11];对大多数CRO、万古霉素耐药肠球菌(VRE)、甲氧西林耐药金葡菌(MRSA)等耐药菌均有活性;在治疗革兰阴性菌中,依拉环素不受到β-内酰胺酶(ESBL,KPC,AmpC,OXA-48/23,VIM,NDM,IMP)存在或类型的影响[12]。
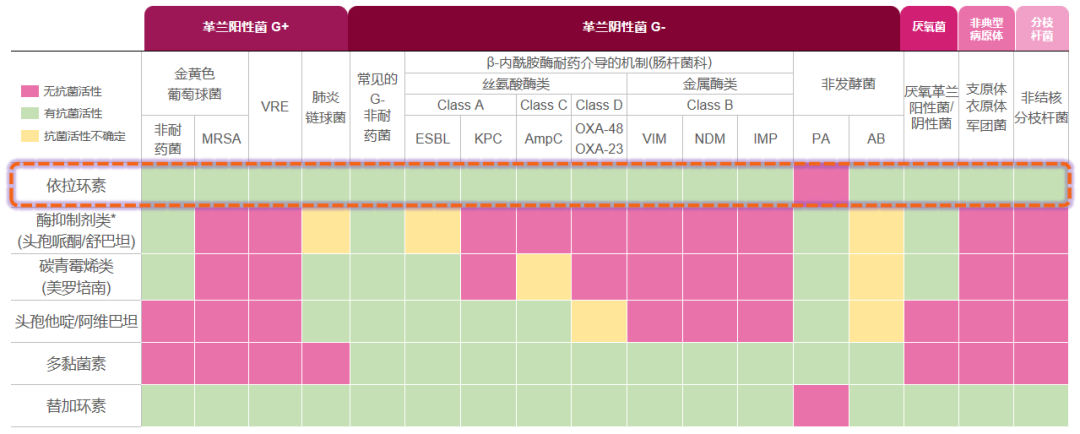
△依拉环素抗菌谱广,可覆盖不同类型细菌及耐药细菌
抗菌活性强,维持较低的最小抑菌浓度值
最小抑菌浓度值(MIC)维持较低水平,意味着标准剂量的抗菌药即可发挥强大抗菌作用,而无需通过增加药物剂量才能达到临床治疗效果,避免药物不良反应和细菌耐药的风险增加。
国内外的体外药敏试验显示,依拉环素对碳青霉烯耐药大肠埃希菌(CREC)、CRKP(包括产KPC、NDM)、CRAB、MRSA、VRE的MIC90仅为0.032~2μg/mL,相比其他抗菌药低1~2倍以上[13-14]。依拉环素在欧洲上市大约5年以来,MDR、产ESBL肠杆菌或产碳青霉烯酶肠杆菌(carbapenemase-producing Enterobacteriaceae,CPE)的MIC50仍维持在0.5~1μg/mL[15-16]。
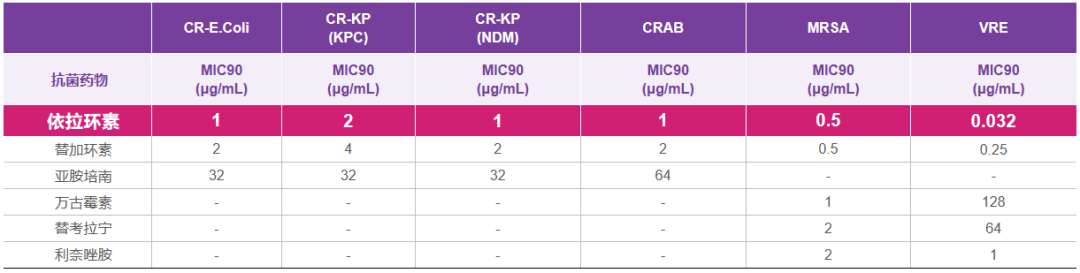
△体外药敏试验显示依拉环素对CREC、CRKP、CRAB、MRSA、VRE保持较低的MIC90
组织浓度高,推荐剂量可达较高成功率
从药代动力学/药效学(PK/PD)特征来看,依拉环素在体内分布广泛、组织中浓度高,蛋白结合率约为79%~90%;主要通过CYP3A4/5和FMO酶介导的氧化作用进行代谢,给药剂量的近半数经粪便、约1/3经尿液排泄,肾功能受损者无需调整剂量。
值得关注的是,良好的组织穿透性是依拉环素在各种复杂感染中大显身手的秘诀所在。一项基于Ⅱ期临床试验的评估数据显示,使用推荐剂量的依拉环素,在f AUC:MIC≥1.87的情况下,临床成功率即可达到100%[17]。这同样表明依拉环素可以避免“以加量增毒换取疗效”的不合理用药。

△依拉环素的组织穿透性强,且fAUC/MIC可作为预测疗效的PK/PD参数
与多种药物联合应用具有协同相加作用
CRE诊治和防控专家共识指出,联合用药可以更快速控制感染,遏制耐药发生;并适当降低毒性较高的药物的剂量,减少不良反应;对于严重感染患者,联合治疗病死率明显低于单药治疗[5]。
那么,谁是MDR/CRO联合治疗的理想选择?已有针对CREC、CRKP、CRAB的联合药敏研究显示,依拉环素与多种药物显示出良好的协同相加作用,而无拮抗作用[18];此外,抗菌谱广、耐药率低、强效安全等药物特征,也支持依拉环素作为联合治疗的基础方案。
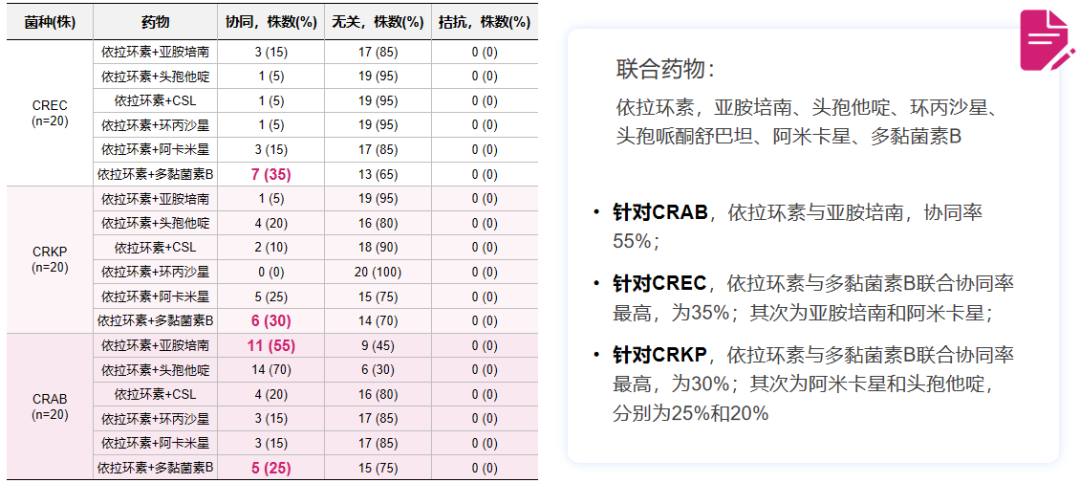
△体外药敏试验显示依拉环素与多种药物联合可对CRAB、CREC、CRKP产生协同相加的抗菌作用
强大的证据背书和权威的
国内外指南推荐
继在美国、欧洲、新加坡上市后,今年3月,依拉环素获批在中国上市。
依拉环素的国内外获批,主要基于国际IGNITE 1/4试验以及国内桥接试验的积极结果(见下表),证实依拉环素治疗复杂腹腔内感染(cIAI)的疗效不劣于碳青霉烯类药物,而且腹泻等胃肠道反应的发生率更低。在真实世界研究中,依拉环素的疗效和安全性再次得到印证,而且拓展了抗感染治疗的应用场景,包括肺炎、骨关节和皮肤软组织感染、糖尿病足、脓胸、血流感染、导管相关感染等(见下表)。
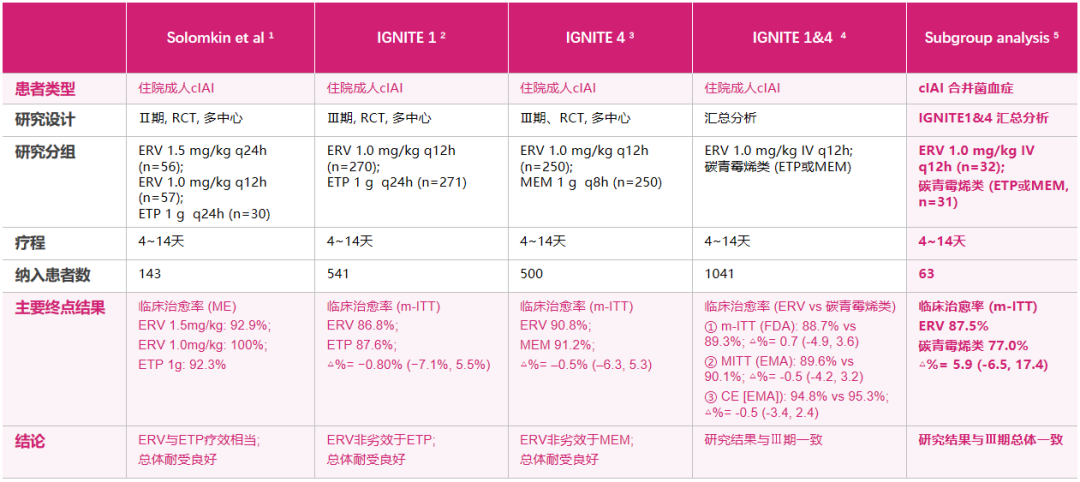
△依拉环素的临床试验及汇总分析
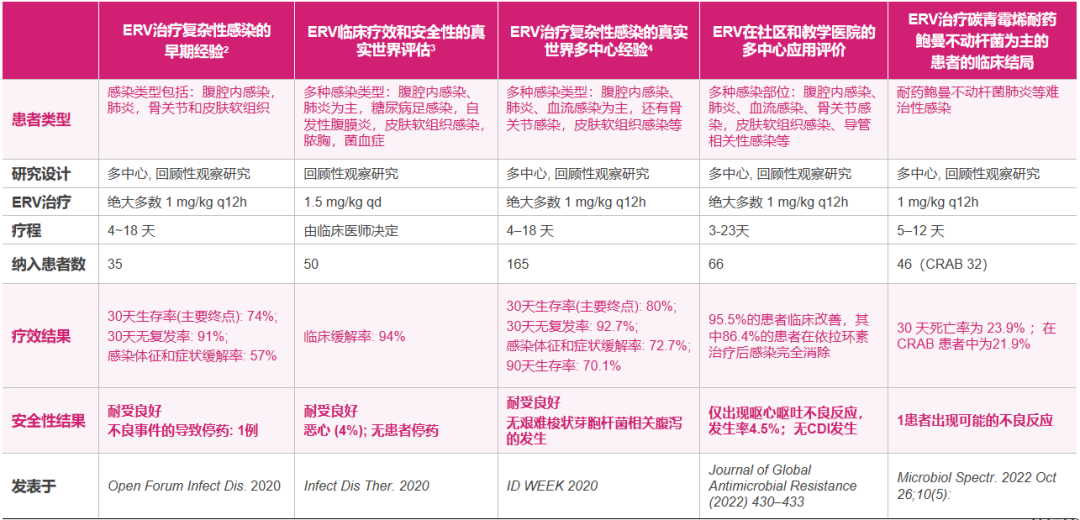
△依拉环素的真实世界研究
在丰富的循证医学证据基础上,依拉环素已被国内外多部权威指南或专家共识所推荐。美国感染病学会(IDSA)的耐药革兰阴性菌感染治疗指南,欧洲临床微生物与感染病学会(ESCMID)的MDR革兰阴性菌感染指南,中国CRO感染诊断、治疗与防控指南,中国台湾MDR菌感染治疗指南均推荐依拉环素作为经验性治疗。此外,还有多个指南共识推荐依拉环素用于血流感染、腹腔感染以及各种耐药细菌感染的治疗(见下图)。
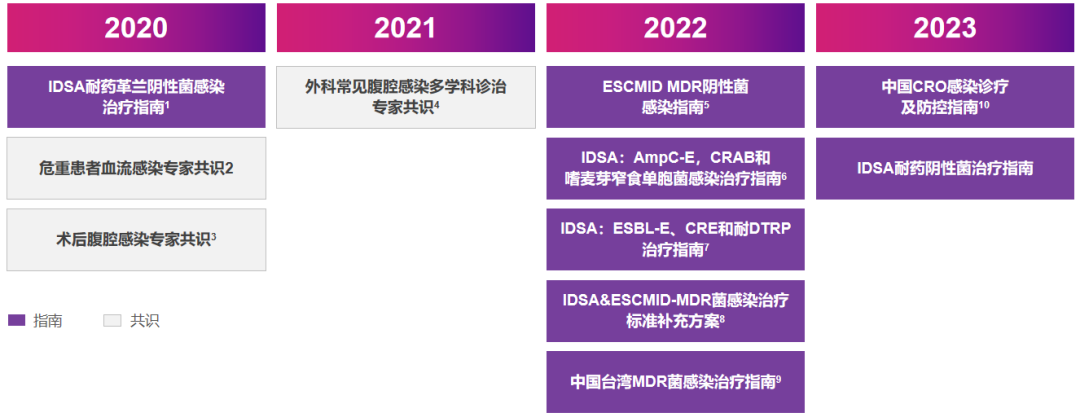
△多部国内外权威指南共识推荐依拉环素治疗MDR/CRO感染
拓展临床应用场景:
来自不同学科的声音
如前所述,依拉环素具有抗菌谱广、抗菌活性强、分布广泛、组织穿透性强、联合用药协同作用等药物特征,临床试验和真实世界研究也证实其在不同感染类型患者中的疗效和安全性。因此,依拉环素上市可及之后的临床应用场景还将得到大大拓展。
呼吸科
肺部感染是呼吸科重要的一大类疾病,以社区获得性肺炎(CAP)、医院获得性肺炎(HAP)及呼吸机相关性肺炎(VAP)为主,常见致病菌包括肺炎链球菌、流感嗜血杆菌、 肺炎克雷伯菌等。随着抗菌药物耐药现象越来越严重,既往长期经验使用的青霉素类、碳青霉烯类等药物似乎越来越难满足临床的需求。
多项数据提示依拉环素用于治疗肺部感染,包括多重耐药肺部感染的可行性。依拉环素肺组织中浓度高,其在肺泡上皮衬液(ELF)中的浓度明显高于替加环素[19],且肺组织穿透率高,ELF和肺泡巨噬细胞(AM)中浓度是血浆浓度的6.44倍和51.63倍[20]。
在已报道的依拉环素真实世界研究中纳入了部分肺部感染患者,虽然病例数较少,但已初步显示出依拉环素在肺部感染中的应用潜能。可喜的是,依拉环素已在我国上市。相信随着临床研究和真实世界应用经验的积累,我们会对依拉环素在肺部感染中的表现有更多直接认识,也期待依拉环素为肺部感染临床治疗实践掀开新的篇章。
重症医学科
重症医学科(ICU)患者因原发疾病的关系大多免疫力低下,是重症感染的好发人群,同时也是医院感染的高发区域,因此,重症感染引起的脓毒症以及多重耐药等现象在ICU尤为严重。研究显示,耐药克雷伯菌、不动杆菌和肠球菌感染是ICU内感染导致死亡的独立危险因素[21]。
碳青霉烯类是ICU抗击重症感染的中坚力量,但随着碳青霉烯类的使用增加,与其他抗菌药物一样,耐药形势也日趋严峻。CRKP检出率接近25%,CRAB的检出率已超70%[22]。而碳青霉烯类耐药后的选择十分有限,临床亟需新的强大的抗菌药物。
依拉环素的问世为解决这一难题提供了方案。该药抗菌谱广,对包括ESBLs、CRE、CRAB等在内的多重耐药菌均有强大的抗菌活性,且不易发生四环素类常见的耐药。其III期临床试验(IGNITE 1和IGNITE 4研究)证明,依拉环素与厄他培南/美罗培南在治疗cIAI中疗效相当且安全性好。依拉环素对于革兰阳性菌感染包括MRSA等也表现出了较高的抗菌作用。
值得一提的是,一份意大利和法国专家发布的《危重患者血流感染专家共识》推荐依拉环素联合其他药物用于治疗血流感染,而血流感染在ICU常见感染中排名第三,也是ICU最常见的混合感染[23]。相信依拉环素在中国上市可为ICU抗感染治疗的严峻形势带来新的希望,未来我们还需要积累更多的依拉环素单用或联合应用于ICU重症感染的经验。
血液科
由于疾病本身或抗血液病治疗对造血系统和免疫系统的损伤,以及造血干细胞移植受者需要免疫抑制等因素,血液病患者和造血干细胞移植受者的感染风险较高。
粒细胞缺乏伴发热患者是一类最主要的感染高风险人群,感染的部位以呼吸道感染和血流感染为主。中国《中性粒细胞缺乏伴发热患者抗菌药物应用指南(2020版)》指出,我国粒缺伴发热其病原学资料显示以革兰阴性杆菌为主,包括大肠埃希菌、肺炎克雷伯菌、铜绿假单胞菌、嗜麦芽窄食单胞菌和鲍曼不动杆菌,耐药菌主要包括产ESBL-EC、产ESBL肺炎克雷伯菌、CRKP、耐碳青霉烯铜绿假单胞菌(CRPA)、CRAB等。初始选择抗菌药物时要求能覆盖最常见和毒力较强的病原菌、并具有抗假单胞菌活性和安全性良好[24]。
依拉环素抗菌谱广,可覆盖CRE、CRAB等耐药菌株,且抗菌活性强,具有更快退热的潜在优势[25],同时还提高了组织分布尤其在血流和肺部的浓度,并减少了不良反应,其诸多PK/PD特征符合血液科患者抗感染治疗的需求,临床应用前景值得期待。
参考文献
[1]Antimicrobial Resistance Collaborators. Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis [published correction appears in Lancet. 2022 Oct 1;400(10358):1102]. Lancet. 2022;399(10325):629-655
[2]The Review on Antimicrobial Resistance, Chaired by Jim O’Neill, December 2014. available from:https://amr-review.org/#:~:text=%E2%80%9CThe%20Review%20on%20Antimicrobial%20Resistance%20%28AMR%29%2C%20was%20commissioned,and%20propose%20concrete%20actions%20to%20tackle%20it%20internationally
[3]Reynolds D, Burnham JP, Vazquez Guillamet C, et al. The threat of multidrug-resistant/extensively drug-resistant Gram-negative respiratory infections: another pandemic. Eur Respir Rev. 2022;31(166):220068.
[4]CHINET中国细菌耐药监测结果(2022年1-12月).available from: www.chinets.com
[5]中国碳青霉烯耐药肠杆菌科细菌感染诊治与防控专家共识[J]. 中华医学杂志,2021,101(36):2850-2860.
[6]张雪峥等.结构修饰性四环素类抗生素研究进展[J].中国抗生素杂志,2016,41(6):411
[7]Gillis EP, Eastman KJ, Hill MD, Donnelly DJ, Meanwell NA. Applications of Fluorine in Medicinal Chemistry. J Med Chem. 2015;58(21):8315-8359
[8]Purser S, Moore PR, Swallow S, Gouverneur V. Fluorine in medicinal chemistry. Chem Soc Rev. 2008;37(2):320-330
[9]Sutcliffe JA, O'Brien W, Fyfe C, Grossman TH. Antibacterial activity of eravacycline (TP-434), a novel fluorocycline, against hospital and community pathogens. Antimicrob Agents Chemother. 2013;57(11):5548-5558
[10]Zhanel GG, Cheung D, Adam H, et al. Review of Eravacycline, a Novel Fluorocycline Antibacterial Agent. Drugs. 2016;76(5):567-588.
Grossman TH, Starosta AL, Fyfe C, et al. Target- and resistance-based mechanistic studies with [11]TP-434, a novel fluorocycline antibiotic [published correction appears in Antimicrob Agents Chemother. 2015 Sep;59(9):5870]. Antimicrob Agents Chemother. 2012;56(5):2559-2564
[12]Alosaimy S, Abdul-Mutakabbir JC, Kebriaei R, Jorgensen SCJ, Rybak MJ. Evaluation of Eravacycline: A Novel Fluorocycline. Pharmacotherapy. 2020;40(3):221-238
[13]Zhao C, Wang X, Zhang Y, et al. In vitro activities of Eravacycline against 336 isolates collected from 2012 to 2016 from 11 teaching hospitals in China. BMC Infect Dis. 2019;19(1):508. Published 2019 Jun 10
[14]Seifert H, Stefanik D, Sutcliffe JA, Higgins PG. In-vitro activity of the novel fluorocycline eravacycline against carbapenem non-susceptible Acinetobacter baumannii. Int J Antimicrob Agents. 2018;51(1):62-64
[15]O. Jomat, et al.In vitro activity of cefiderocol, eravacycline and β-lactam-β-lactamase inhibitor combinations against carbapenemase-producing Enterobacterales isolated in western Normandy, France, during a 5 years period.ECCMID 2023;abstract P0158
[16]S. Hawser, et al.In vitro surveillance of eravacycline against Enterobacterales and non-fermentor clinical isolates, including resistant isolates, collected in Europe during 2021.ECCMID 2023;abstract P0139
[17]Bhavnani SM, Trang M, Griffith DC, et al. Pharmacokinetic-Pharmacodynamic Target Attainment Analyses as Support for Meropenem-Vaborbactam Dosing Regimens and Susceptibility Breakpoints. Antimicrob Agents Chemother. 2022;66(12):e0213021
[18]Li Y, Cui L, Xue F, Wang Q, Zheng B. Synergism of eravacycline combined with other antimicrobial agents against carbapenem-resistant Enterobacteriaceae and Acinetobacter baumannii. J Glob Antimicrob Resist. 2022;30:56-59
[19]Gotfried MH, et al. Comparison of Omadacycline and Tigecycline Pharmacokinetics in the Plasma, Epithelial Lining Fluid, and Alveolar Cells of Healthy Adult Subjects. Antimicrob Agents Chemother. 2017;61(9):e01135-17.
[20]Connors KP, et al. Phase I, open-label, safety and pharmacokinetic study to assess bronchopulmonary disposition of intravenous eravacycline in healthy men and women. Antimicrob Agents Chemother. 2014;58(4):2113.
[21]Jean-Louis Vincent JL,et al. Prevalence and Outcomes of Infection Among Patients in Intensive Care Units in 2017. JAMA. 2020;323(15):1478-1487.
[22]CHINET 2022年全年细菌耐药检测结果 http://www.chinets.com/Document
[23]Timsit JF, et al. Bloodstream infections in critically ill patients: an expert statement. Intensive Care Med. 2020;46(2):266
[24]中华医学会血液学分会, 中国医师协会血液科医师分会. 中国中性粒细胞缺乏伴发热患者抗菌药物临床应用指南(2020年版). 中华血液学杂志, 2020, 41(12):10.
[25]Solomkin JS, et al. Phase 2, randomized, double-blind study of the efficacy and safety of two dose regimens of eravacycline versus ertapenem for adult community-acquired complicated intra-abdominal infections. Antimicrob Agents Chemother. 2014;58(4):1847-54.
.png)
罗益锋 教授
中山大学附属第一医院医务处副处长
内科副主任、呼吸与危重症医学科副主任、内科ICU主任
临床医学博士,主任医师,硕士研究生导师,博士后合作导师
全国卫生健康系统抗击新冠肺炎疫情防控工作先进个人
中国医师协会呼吸医师分会第一届中青委常委
IDSC全国青年委员
中国医学救援协会重症医学分会常务理事
广东省医学会呼吸病学分会青委副主委
广东省医学会内科学分会青委副主委
广东省胸部肿瘤协会肿瘤慢病管理专业委员会副主委
广东省临床医学学会感染性疾病精准诊疗专委会副主委
广东省药学会重症医学用药专业委员会常委
广东省健康管理学会第一、二届理事会理事
美国Vanderbilt(范德堡)大学医学中心访问学者
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。

责任编辑:彭伟彬
相关搜索: 依拉环素