- 首页 > 正文
张丽教授:念珠菌耐药性及机制解读
感染医线 发表时间:2023/7/21 20:42:48
念珠菌广泛存在于自然界,为条件致病真菌。临床以白念珠菌(Candida albicans)最常见,非白念珠菌近十年分离比例在增加,其中以热带念珠菌(C. tropicalis)、光滑念珠菌(C. glabrata)、近平滑念珠菌(C. parapsilosis)和克柔念珠菌(C. krusei)较常见。全球念珠菌耐药问题日益引起关注。2019年美国CDC耐药报告中将耳念珠菌(C. auris)列入紧急威胁名单。在近期举行的中国医药教育协会感染疾病专业委员会第九届学术大会(IDSC 2023)上,北京协和医院检验科张丽教授分享了全球念珠菌耐药性评估及药敏解读。
01
真菌耐药流行病学
全球SENTRY监测项目近20年数据(2006~2016)分析显示,常见念珠菌如白念珠菌、近平滑念珠菌和热带念珠菌的氟康唑耐药率均低于10%,其中非白念珠菌氟康唑耐药率高于非白念珠菌;棘白菌素类耐药率方面,光滑念珠菌高于白念珠菌和其他非白念珠菌:阿尼芬净1.7%、卡泊芬净3.5%、米卡芬净1.7%[1]。杜克医学中心对2001~2010年收集的313例光滑念珠菌进行了棘白菌素药敏检测,阿尼芬净耐药率从4.9%增至12.3%[2]。
中国医院侵袭性真菌病监测网(CHIF-NET)(2015~2017)数据[3]显示,热带念珠菌对氟康唑的敏感率仅60%左右(图1),而白念珠菌和近平滑念珠菌氟康唑耐药率均低于10%。另外,CHIF-NET已监测到棘白菌素耐药的光滑念珠菌、热带念珠菌、季也蒙念珠菌和克柔念珠菌,但两性霉素B耐药少见(图1)。
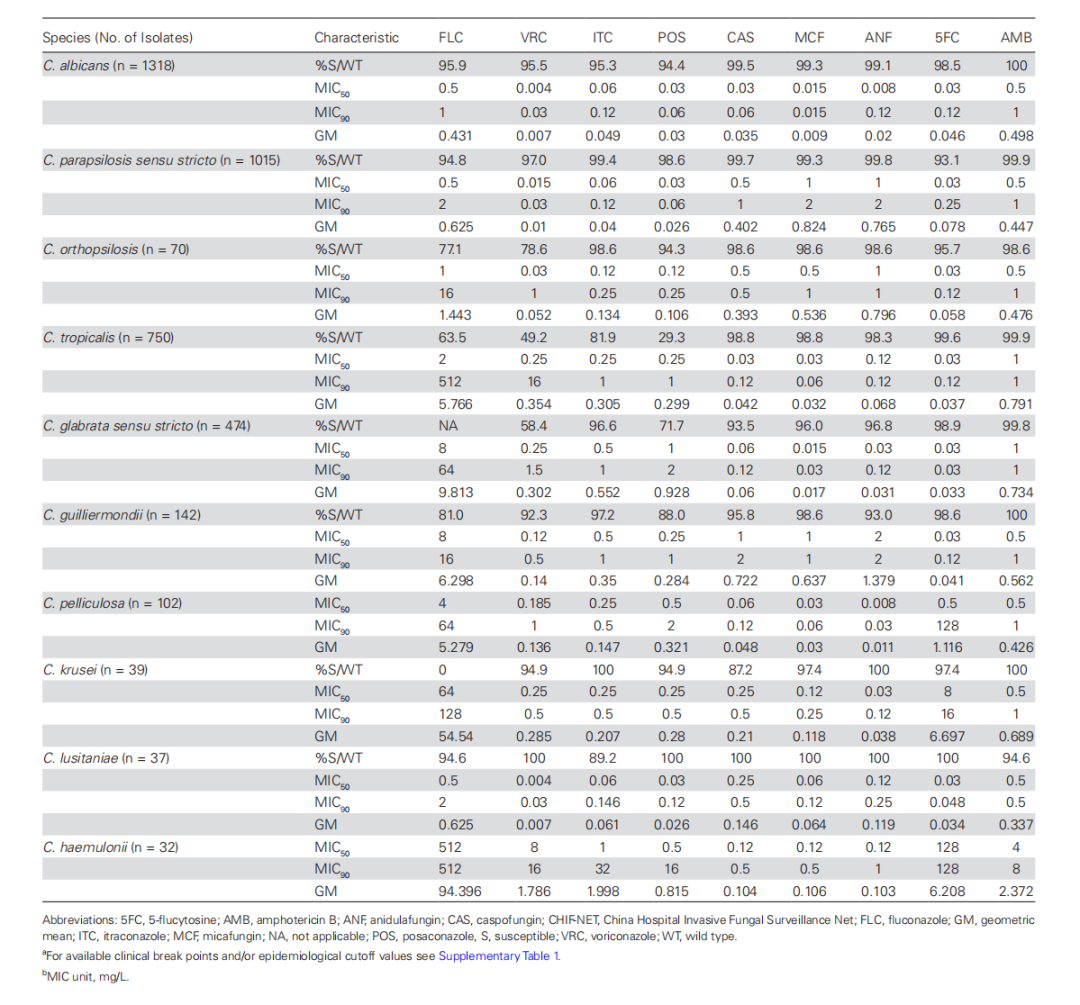
图1. CHIF-NET15-17监测念珠菌氟康唑和伏立康唑药物敏感性
02
真菌耐药机制与研究进展
唑类药物耐药机制主要包括药物外排泵(ATP依赖的转运蛋白超家族ABC和易化扩散载体蛋白超家族MFS)过表达、编码14-a羊毛甾醇去甲基化酶的ERG11改变和ERG11表达升高等。棘白菌素类药物耐药机制主要是编码1,3-β-D-葡聚糖合成酶的基因FKS1/FKS2发生突变,导致对该类药物的亲和力降低。氟胞嘧啶耐药机制主要包括胞嘧啶通透酶(FCY2编码)改变;去氨基酶(FCY1)突变。两性霉素B耐药机制相关研究较少,主要机制是作用靶点麦角固醇其合成通路中基因(如ERG2、ERG3、ERG5等)改变后导致细胞膜上主要甾醇成分改变。
热带念珠菌
国内热带念珠菌对唑类药物耐药率持续升高。一项中国全国性多中心研究(87家医院收集3702株热带念珠菌)[4]报告了热带念珠菌抗真菌药物敏感性变化,在9年的监测中,氟康唑耐药率从5.7%上升到31.8%,伏立康唑的耐药率从5.7%上升到29.1%(图2)。靶位点编码基因ERG11的错义突变与热带念珠菌唑类耐药相关;药物外排泵高表达对我国侵袭性热带念珠菌唑类耐药作用不十分重要[5]。
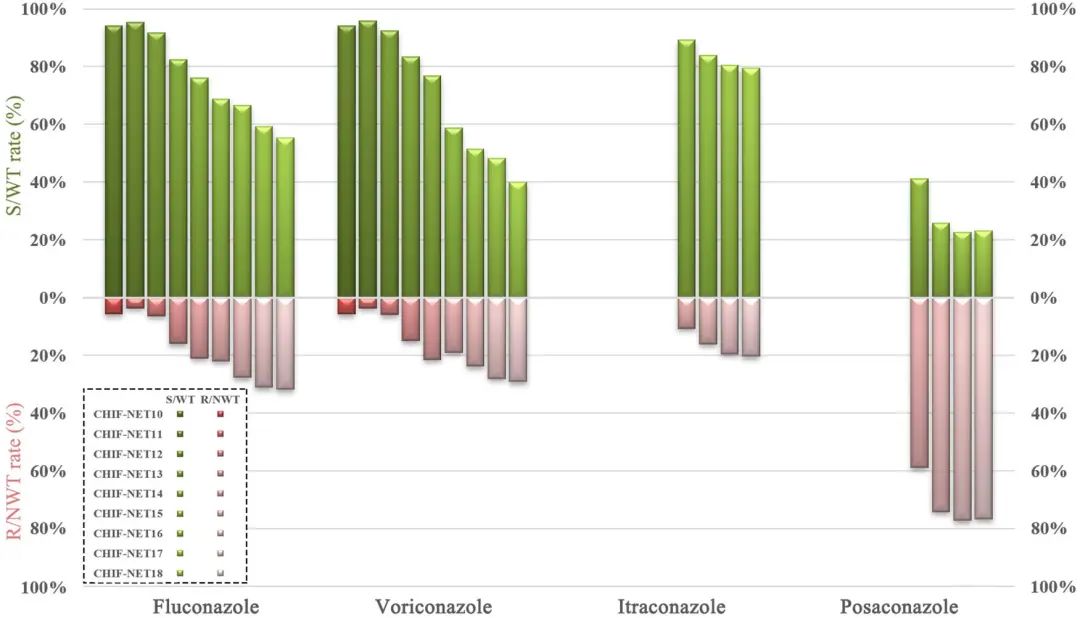
图2. 热带念珠菌耐药情况
光滑念珠菌
光滑念珠菌对唑类药物敏感性低。IDSA指南中推荐棘白菌素是侵袭性光滑念珠菌感染的首选药物。2018年北京协和医院报道我国首例棘白菌素耐药菌,为高耐株(MIC≥8 μg/ml),患者为46岁免疫功能正常男性,腹水,腹腔手术史,无抗真菌药物暴露史[6]。FKS1/FKS2发生突变是导致耐药的主要机制,FKS2 E655K突变(Fks2 HS1)是导致棘白菌素耐药的新发现位点[7]。
近平滑念珠菌
中国CHIF-NET(2015~2017)数据显示,近平滑念珠菌对氟康唑和伏立康唑耐药率低于10%[3](图1)。但在近3年中,全球近平滑念珠菌氟康唑耐药株在医疗机构的分布范围逐渐扩张,耐药率攀升;土耳其、美国、韩国、印度等国连续出现耐药株克隆性暴发[8-9]。2019年印度某医院报道199株菌中氟康唑耐药率32%,耐药机制为Erg11突变(K143R 92%、Y132F 8%)[10]。2020年CHIF-NET多中心研究发现,319株近平滑念珠菌氟康唑耐药率5%,但3家医院内存在耐药株克隆传播,其中一家医院存在7株耐药菌克隆传播,耐药机制为Erg11突变(Y132F)[11]。此外CHIF-NET报道了国内首例Fks1突变(S656P)导致棘白菌素类药物泛耐药株。
耳念珠菌
耳念珠菌是近年来引起全球广泛关注的多重耐药念珠菌,多个国家已报道了耳念珠菌感染病例[12](图3)。中国北京报道的首例耳念珠菌对主要抗真菌药物均敏感,包括两性霉素B、氟康唑和卡泊芬净,沈阳报道的15例耳念珠菌主要表现为对氟康唑耐药,但对其他抗真菌药物敏感[13-14]。已报道的耳念珠菌耐药机制包括:Erg11突变(Y132F、K143R)导致唑类药物耐药;Fks1突变(HS1区,S639F)导致棘白菌素类药物耐药[15]。
.png)
图3. 截至2019年6月15日报告耳念珠菌病例的国家
希木龙念珠菌(C. haemulonii)
CHIF-NET监测数据显示,2009~2014年希木龙念珠菌分离率为0.3%(24/3965)[16],2015~2017年已升至0.8%(32/4010)[3],且国内和国际已报道出现克隆传播。CHIF-NET项目监测到希木龙念珠菌的多重耐药情况[3](图4)。
.png)
图4. 念珠菌多重耐药情况
角膜念珠菌(C. pelliculosa)
中国CHIF-NET项目数据显示,在2009~2014年全国65家三甲医院鉴定到123株角膜念珠菌,总分离率为1.4%[16],2015年至2017年其分离率增长至2.5%[3]。角膜念珠菌对唑类药物敏感性近年来呈现下降趋势,且存在潜在的交叉耐药和多重耐药菌株,2015~2017年有近1/3的角膜念珠菌对唑类和5-氟胞嘧啶共耐药[3]。
Candida vulturna
2023年6月复旦大学黄广华教授团队研究并报道了中国北方某家医院2019年1月至2022年10月期间19例Candida vulturna引起的感染,该菌种表现为对多种抗真菌药物耐药,需要引起警惕。
03
小结
真菌耐药情况亟待关注。热带念珠菌唑类药物耐药率升高,唑类交叉耐药现象明显。光滑念珠菌应警惕棘白菌素类药物耐药株的出现。近平滑念珠菌具有耐药株传播流行风险。多重耐药念珠菌中,希木龙念珠菌和角膜念珠菌亟需关注其传播流行,也需持续监测新的多重耐药株的出现。
参考文献
[1] Pfaller MA, Diekema DJ, Turnidge JD, Castanheira M, Jones RN. Twenty Years of the SENTRY Antifungal Surveillance Program: Results for Candida Species From 1997-2016. Open Forum Infect Dis. 2019;6(Suppl 1):S79-S94. Published 2019 Mar 15. doi:10.1093/ofid/ofy358
[2] Alexander BD, Johnson MD, Pfeiffer CD, et al. Increasing echinocandin resistance in Candida glabrata: clinical failure correlates with presence of FKS mutations and elevated minimum inhibitory concentrations [published correction appears in Clin Infect Dis. 2014 Mar;58(5):754]. Clin Infect Dis. 2013;56(12):1724-1732. doi:10.1093/cid/cit136
[3] Xiao M, Chen SC, Kong F, et al. Distribution and Antifungal Susceptibility of Candida Species Causing Candidemia in China: An Update From the CHIF-NET Study. J Infect Dis. 2020;221(Suppl 2):S139-S147. doi:10.1093/infdis/jiz573
[4] Wang Y, Fan X, Wang H, et al. Continual Decline in Azole Susceptibility Rates in Candida tropicalis Over a 9-Year Period in China. Front Microbiol. 2021;12:702839. Published 2021 Jul 9. doi:10.3389/fmicb.2021.702839
[5] Fan X, Xiao M, Liao K, et al. Notable Increasing Trend in Azole Non-susceptible Candida tropicalis Causing Invasive Candidiasis in China (August 2009 to July 2014): Molecular Epidemiology and Clinical Azole Consumption. Front Microbiol. 2017;8:464. Published 2017 Mar 22. doi:10.3389/fmicb.2017.00464
[6] Xiao M, Fan X, Hou X, et al. Clinical characteristics of the first cases of invasive candidiasis in China due to pan-echinocandin-resistant Candida tropicalis and Candida glabrata isolates with delineation of their resistance mechanisms. Infect Drug Resist. 2018;11:155-161. Published 2018 Jan 23. doi:10.2147/IDR.S152785
[7] Perlin DS, Wiederhold NP. Culture-Independent Molecular Methods for Detection of Antifungal Resistance Mechanisms and Fungal Identification. J Infect Dis. 2017;216(suppl_3):S458-S465. doi:10.1093/infdis/jix121
[8] Daneshnia F, de Almeida Júnior JN, Ilkit M, et al. Worldwide emergence of fluconazole-resistant Candida parapsilosis: current framework and future research roadmap [published correction appears in Lancet Microbe. 2023 Jun 15;:]. Lancet Microbe. 2023;4(6):e470-e480. doi:10.1016/S2666-5247(23)00067-8
[9] Alcoceba E, Gómez A, Lara-Esbrí P, et al. Fluconazole-resistant Candida parapsilosis clonally related genotypes: first report proving the presence of endemic isolates harbouring the Y132F ERG11 gene substitution in Spain. Clin Microbiol Infect. 2022;28(8):1113-1119. doi:10.1016/j.cmi.2022.02.025
[10] Singh A, Singh PK, de Groot T, et al. Emergence of clonal fluconazole-resistant Candida parapsilosis clinical isolates in a multicentre laboratory-based surveillance study in India. J Antimicrob Chemother. 2019;74(5):1260-1268. doi:10.1093/jac/dkz029
[11] Zhang L, Yu SY, Chen SC, et al. Molecular Characterization of Candida parapsilosis by Microsatellite Typing and Emergence of Clonal Antifungal Drug Resistant Strains in a Multicenter Surveillance in China. Front Microbiol. 2020;11:1320. Published 2020 Jun 16. doi:10.3389/fmicb.2020.01320
[12] Friedman DZP, Schwartz IS. Emerging Fungal Infections: New Patients, New Patterns, and New Pathogens. J Fungi (Basel). 2019;5(3):67. Published 2019 Jul 20. doi:10.3390/jof5030067
[13] Wang X, Bing J, Zheng Q, et al. The first isolate of Candida auris in China: clinical and biological aspects. Emerg Microbes Infect. 2018;7(1):93. Published 2018 May 18. doi:10.1038/s41426-018-0095-0
[14] Tian S, Rong C, Nian H, et al. First cases and risk factors of super yeast Candida auris infection or colonization from Shenyang, China. Emerg Microbes Infect. 2018;7(1):128. Published 2018 Jul 11. doi:10.1038/s41426-018-0131-0
[15] Chowdhary A, Prakash A, Sharma C, et al. A multicentre study of antifungal susceptibility patterns among 350 Candida auris isolates (2009-17) in India: role of the ERG11 and FKS1 genes in azole and echinocandin resistance. J Antimicrob Chemother. 2018;73(4):891-899. doi:10.1093/jac/dkx480
[16] Xiao M, Sun ZY, Kang M, et al. Five-Year National Surveillance of Invasive Candidiasis: Species Distribution and Azole Susceptibility from the China Hospital Invasive Fungal Surveillance Net (CHIF-NET) Study. J Clin Microbiol. 2018;56(7):e00577-18. Published 2018 Jun 25. doi:10.1128/JCM.00577-18
.jpg)
张丽 教授
北京协和医院检验科
微生物检验专业组副组长
副主任技师
社会兼职
全国真菌病监测网质量管理中心质量主管
中国医学装备协会检验医学分会团标学组委员兼秘书
医学参考报微生物与感染专刊青年编委会副主任委员
华人抗菌药物敏感性试验委员会(ChiCAST) 秘书
学术成就
主持国自然青年项目1项、中央高校科研基金项目1项、科技部重大专项子课题1项;发表SCI和核心期刊文章10余篇;参加卫生行业标准制定4项,参与著书、专家共识10余部;获得中华预防医学会科技奖三等奖、华夏医学科技奖三等奖等科技奖励。
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
.png)
责任编辑:彭伟彬
相关搜索: IDSC 2023