- 首页 > 正文
沈宁教授:新冠和流感合并细菌感染的异同
感染医线 发表时间:2023/8/9 20:08:05
编者按:2023年7月21~23日,由中华医学会、中华医学会呼吸病学分会主办,上海市医学会、上海交通大学医学院附属瑞金医院协办的中华医学会第十九届全国呼吸系统感染学术会议在上海顺利召开。国内外知名专家汇聚一堂,通过专题报告等多种形式进行学术交流研讨。会上,北京大学第三医院沈宁教授带来了主题为《新冠和流感合并细菌感染的异同》的精彩报告。本刊特别整理如下。
流感合并细菌感染
基于流感病毒的研究发现,流感合并细菌感染比例为11%~35%。美国2005~2008年对4765名住院甲流患者进行的研究显示,金黄色葡萄球菌、肺炎链球菌为甲流合并细菌感染的主要致病菌。继发细菌感染为重症甲流的独立危险因素(OR 2.78;95%CI:1.11~7)。
1、流感继发细菌感染的机制
● 流感病毒损伤支气管和肺上皮细胞,导致细菌粘附增加,其原因包括PAFr和plgR受体数量增加、病毒神经氨酸酶对唾液酸的切割以及上皮剥脱暴露基底膜成分;这些因素都可通过增强细菌粘附因子(如ChoP、cbpA和PspA)的结合作用,增加细菌的复制和携带。
● 病毒诱导的炎症增强细菌毒力因子的表达,并增加上呼吸道生物膜中细菌从生物膜向浮游状态释放,从而增加细菌向下呼吸道的扩散。
● 过量细胞因子和趋化因子产生,过量分泌I型干扰素导致过多、混合的、未成熟和成熟中性粒细胞募集,从而引发严重的免疫病理学反应。
● 病毒介导的amphiregulin和其他重要组织再生因子的分泌减少,导致炎症加重,这进一步降低肺泡和内皮完整性,导致毛细血管渗漏、肺水肿以及细菌入血。
以继发肺炎链球菌感染为例,流感与肺炎链球菌感染之间协同作用的时间见图1。在肺炎链球菌感染早期,呈递抗原的细胞(包括树突状细胞)产生各种细胞因子,激活先天效应细胞,如巨噬细胞和中性粒细胞,导致细菌清除。而在甲流病毒感染过程中,肺泡巨噬细胞和中性粒细胞在数量和(或)功能上存在缺陷,无法有效清除细菌,导致继发细菌感染的出现。这种缺陷导致继发细菌感染的易感性增加多数发生在病毒感染后7天内。
.png)
注:Bars=接种肺炎球菌疫苗后的存活率;带黑色方块的线=平均存活时间(仅适用于死亡的小鼠)。
图1. 流感与肺炎链球菌感染之间协同作用的时间
2、流感继发细菌感染的危害
研究发现,与流感单一感染相比,合并细菌感染与更高的重症风险相关(见图2)。大约四分之一的流感死亡可归因于细菌共同感染。这些结果应为流感患者疑似细菌合并感染的预防、识别和治疗提供依据。
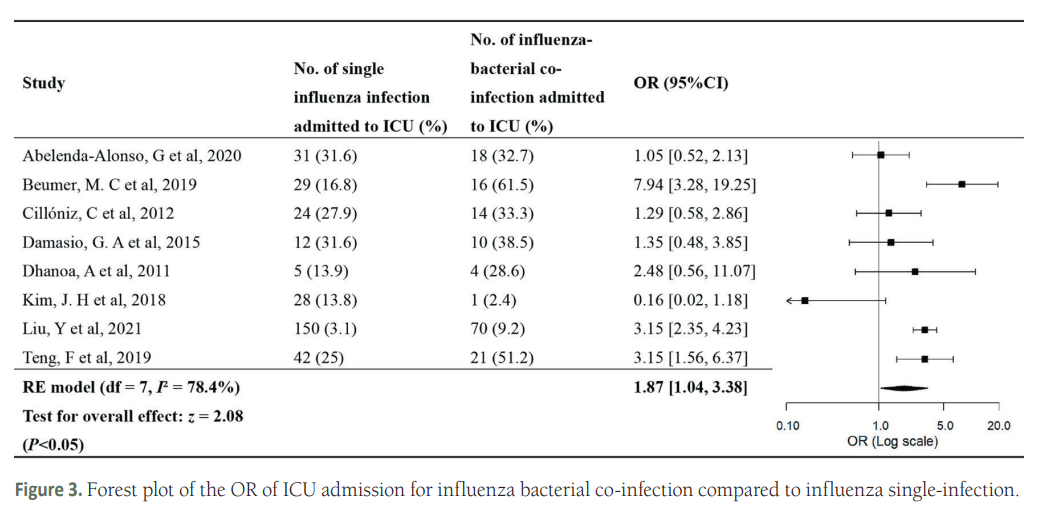
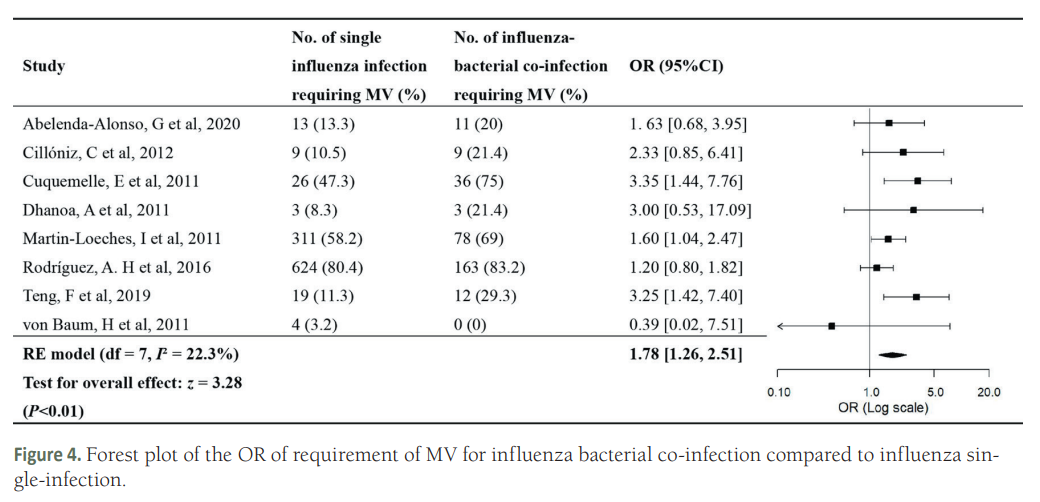
图2. 与流感单一感染相比,合并细菌感染入住ICU、需要机械通气(MV)的OR森林图
新冠合并细菌感染
新型冠状病毒疾病(COVID-19)合并细菌感染比例各文献报道差异很大。目前认为,COVID-19早期合并细菌感染比例低于流感,常见的细菌为金黄色葡萄球菌、肺炎链球菌等社区感染常见的细菌;后期继发细菌感染的比例较高,常见的细菌除了金黄色葡萄球菌外,肺炎克雷伯杆菌、铜绿假单胞菌、鲍曼不动杆菌等医院获得性感染常见的革兰阴性杆菌显著增加,和各医院院感控制水平、耐药菌流行情况、细菌检测技术等因素相关。研究显示,COVID-19合并感染的患病率为5.1%(95%CI:3.6~7.1%),继发感染率为13.1%(95%CI:9.8~17.2%)。在重症监护室(ICU)患者细菌感染率显著增高(调整OR 18.8,95%CI:6.5~54.8),见表1。机械通气患者细菌感染率也明显升高(调整OR 1.41,95%CI:1.30~1.52),见表1。
表1. COVID-19合并细菌感染的预测研究
.png)
1、新冠合并细菌感染机制
新冠继发细菌感染的机制并不完全清楚,大多数都是基于其他呼吸道病毒感染后的可能机制推断而来。通常认为,新冠病毒毒力因子与肺部相互作用并引发免疫反应。这些相互作用可能在几个水平上损害先天免疫,导致细菌附着、生长和传播增加。病毒感染可能会暴露介导细菌附着的细菌受体。共同感染可能导致过度的炎症反应(见图3)。
.png)
图3. 新冠合并细菌感染机制
2、新冠继发细菌感染的危害
2021年发表在《Scientific Reports》的一项研究,旨在通过与流感患者比较,探讨继发细菌感染对COVID-19患者临床病程和死亡率的影响。研究选取以色列一家大型三级中心收治的COVID-19患者(n=642)和流感患者(n=742),患者均接受了血液或痰培养,比较两组患者细菌培养结果、临床参数和死亡率。
结果显示,与流感患者相比,COVID-19患者从入院到细菌生长的时间更长[4(1~8)天 vs. 1(1~3)天]。晚期感染(入院后48小时以上)在COVID-19患者中更为常见(28% vs. 9.5%)。两组患者继发细菌感染的死亡风险均较高,COVID-19患者为2.70倍(1.22~5.83),流感患者为3.09倍(1.11~7.38)。调整年龄和各临床参数后,在COVID-19患者中,继发细菌感染与死亡的相关性仍然显著,而在流感患者中不再显著(见图4)。
.png)
图4. 疾病严重程度的多因素分析
总之,与流感患者相比,COVID-19患者继发细菌感染的预后更差。对于继发细菌感染的COVID-19患者,应给予仔细的监测和及时的抗菌药物治疗。
COVID-19合并细菌感染除了对患者预后的影响外,还对抗菌药物耐药产生影响。由于COVID-19流行期间医务人员超负荷工作、抗菌药物不合理使用增加、对细菌和真菌耐药性监测不足等因素,促进细菌耐药性增加。美国CDC在2022年发表了COVID-19对抗菌药物影响的报告,见表2,值得关注和思考。
表2. COVID-19对18种细菌和真菌耐药性的影响
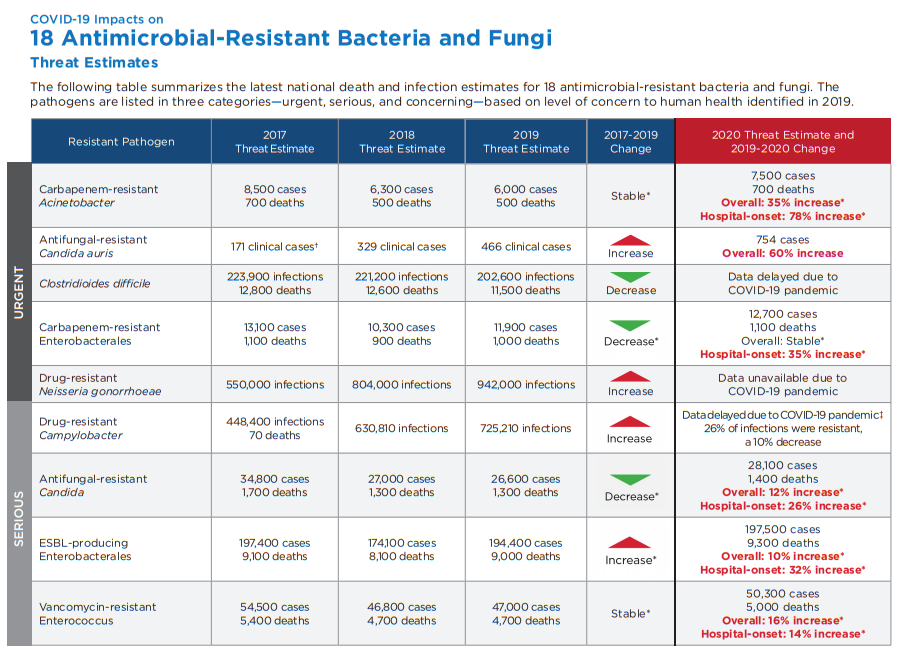
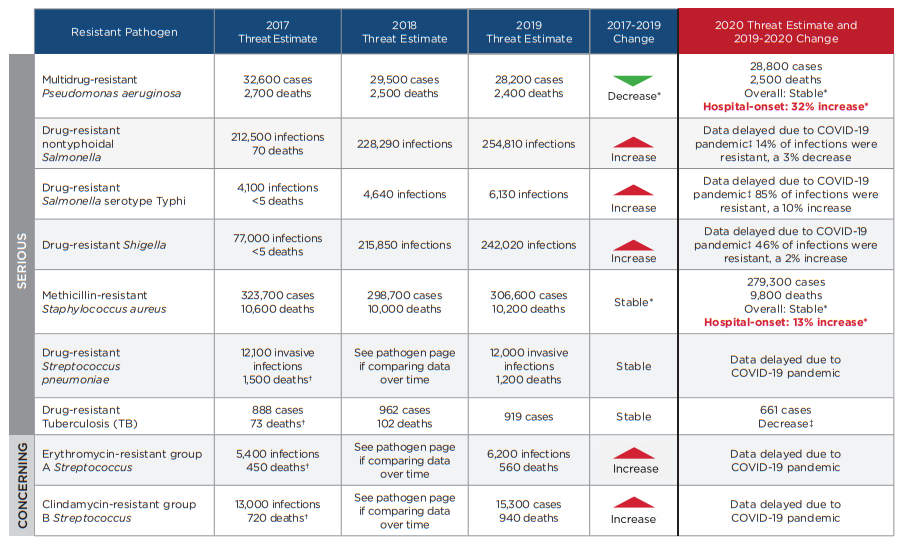
小结
病毒感染后继发细菌感染值得关注,无论流感还是新冠都带来不良预后。其中流感应更关注早期合并革兰阳性球菌的感染,而新冠应更关注后期继发革兰阴性杆菌的感染,深入探究呼吸道病毒感染继发细菌感染的机制,特别是机体免疫反应在不同个体不同病毒感染后的变化,对于理解疾病进展和精准治疗至关重要。此外病毒感染大流行后对细菌耐药情况的影响也需要进一步深入研究。
参考文献
[1]Martin-Loeches I, van Someren Gréve F, Schultz MJ. Bacterial pneumonia as an influenza complication. Curr Opin Infect Dis. 2017;30(2):201-207. doi:10.1097/QCO.0000000000000347.
[2]Garg S, Jain S, Dawood FS, et al. Pneumonia among adults hospitalized with laboratory-confirmed seasonal influenza virus infection-United States, 2005-2008. BMC Infect Dis. 2015;15:369. Published 2015 Aug 26. doi:10.1186/s12879-015-1004-y.
[3]Viasus D, Pa?o-Pardo JR, Pachón J, et al. Factors associated with severe disease in hospitalized adults with pandemic (H1N1) 2009 in Spain. Clin Microbiol Infect. 2011;17(5):738-746. doi:10.1111/j.1469-0691.2010.03362.x.
[4]Mina MJ, Klugman KP. The role of influenza in the severity and transmission of respiratory bacterial disease. Lancet Respir Med. 2014;2(9):750-763. doi:10.1016/S2213-2600(14)70131-6.
[5]Paget C, Trottein F. Mechanisms of Bacterial Superinfection Post-influenza: A Role for Unconventional T Cells. Front Immunol. 2019;10:336. Published 2019 Mar 1. doi:10.3389/fimmu.2019.00336.
[6]Qiao M, Moyes G, Zhu F, Li Y, Wang X. The prevalence of influenza bacterial co-infection and its role in disease severity: A systematic review and meta-analysis. J Glob Health. 2023;13:04063. Published 2023 Jun 16. doi:10.7189/jogh.13.04063.
[7]Langford BJ, So M, Leung V, et al. Predictors and microbiology of respiratory and bloodstream bacterial infection in patients with COVID-19: living rapid review update and meta-regression. Clin Microbiol Infect. 2022;28(4):491-501. doi:10.1016/j.cmi.2021.11.008.
[8]Bengoechea JA, Bamford CG. SARS-CoV-2, bacterial co-infections, and AMR: the deadly trio in COVID-19?. EMBO Mol Med. 2020;12(7):e12560. doi:10.15252/emmm.202012560.
[9]Shafran N, Shafran I, Ben-Zvi H, et al. Secondary bacterial infection in COVID-19 patients is a stronger predictor for death compared to influenza patients. Sci Rep. 2021;11(1):12703. Published 2021 Jun 16. doi:10.1038/s41598-021-92220-0.
[10]CDC.2022 Special Report:COVID-19 U.S. Impact On Antimicrobial Resistance.https://www.cdc.gov/drugresistance/pdf/covid19-impact-report-508.pdf

沈宁 教授
主任医师,教授,博士生导师
北京大学第三医院副院长
感染疾病中心主任
呼吸与危重症医学科副主任
中华医学会呼吸病学分会感染学组副组长
中国医师协会呼吸医师分会外事工作委员会副主任委员
中国女医师协会重症专业委员会副主任委员
中国女医师协会呼吸专业委员会常务委员
北京医学会呼吸内镜和介入学分会常务委员
中国医药教育协会感染疾病专业委员会委员
《The Clinical Respiratory Journal》副主编
《中华结核和呼吸杂志》编委等
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
.png)
责任编辑:彭伟彬
相关搜索: 新冠