- 首页 > 正文
CRAB感染治疗药物的迭代创新
感染医线 发表时间:2023/9/13 10:30:13
编者按:碳青霉烯耐药革兰阴性杆菌(CRO)是全球公共健康领域面临的重大挑战。世界卫生组织(WHO)将CRO的危险级别确定为首要等级,而在WHO发布的首份抗菌药物耐药“重点病原体”清单中,碳青霉烯类耐药鲍曼不动杆菌(CRAB)位列“极为重要”类别的首位。近年来,为规范抗菌药物使用、遏制细菌耐药,我国制定并颁布了多个指导性文件,也获得了较好的实践效果。然而,在经过数年的缓慢下降后,以CRAB为代表的耐药菌株检出率再次出现了上升趋势。最新发布的中国细菌耐药监测网(CHINET)2023上半年数据显示,CRAB的检出率已升至78.6%~79.5%,刷新了历史最高值。面对如此严峻的耐药形势,临床应该如何应对呢?
节节攀升
CRAB流行现状与治疗困境
鲍曼不动杆菌具有强大的获得耐药性和克隆传播的能力,多重耐药(MDR)、广泛耐药(XDR)、全耐药(PDR)鲍曼不动杆菌呈世界性流行,已成为我国院内感染最重要的病原菌之一[1]。鲍曼不动杆菌院内感染最常见的部位是肺部,是医院获得性肺炎(HAP)、尤其是呼吸机相关肺炎(VAP)的重要致病菌。
CHINET 2023上半年数据显示,鲍曼不动杆菌在临床分离菌株中占8.76%,并从去年的第五位升至第四位[2]。同时,与其他主要革兰阴性杆菌(G-菌)相比,鲍曼不动杆菌的耐药问题尤为突出。鲍曼不动杆菌对亚胺培南和美罗培南耐药的耐药率从去年的71.2%和71.9%陡然升至2023上半年的78.6%和79.5%,也是有记录以来的最高值。更为令人担忧的是,CRAB仅对黏菌素类和替加环素保持较好的敏感性,对检测的其他抗菌药的耐药率均高达70%以上,耐药形势不容乐观。
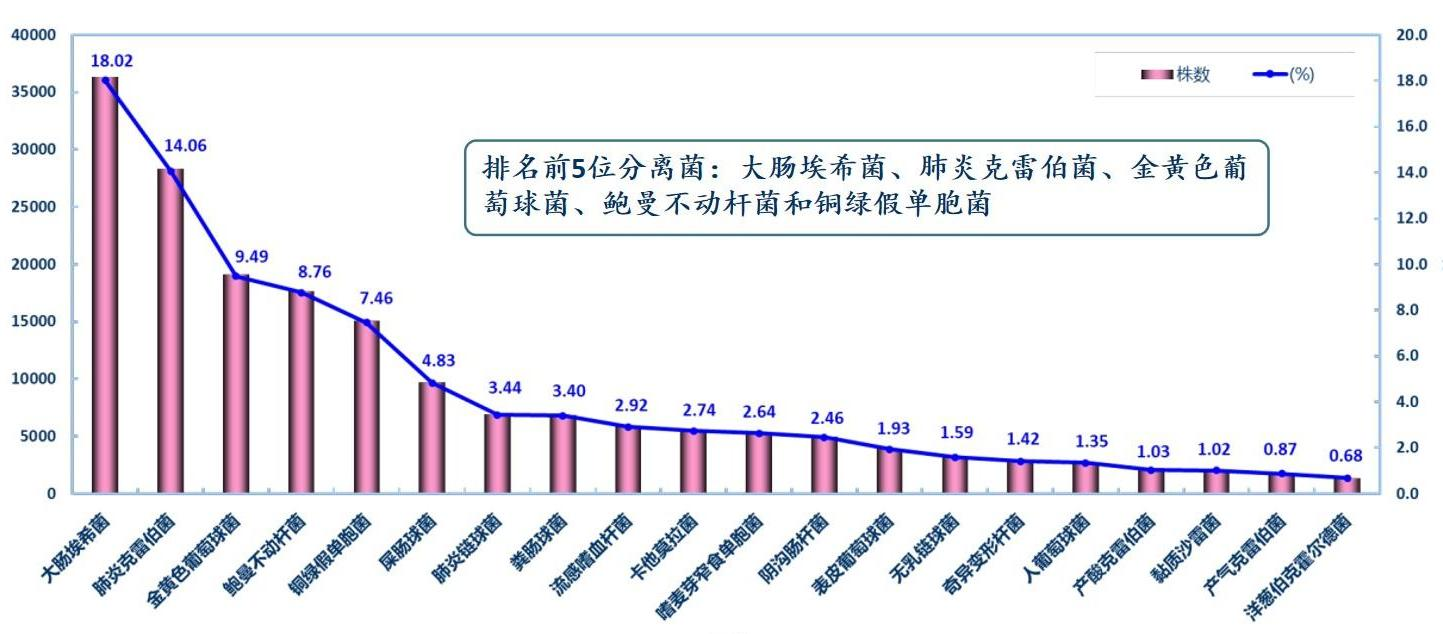
△主要临床分离菌种分布(来源:CHINET)
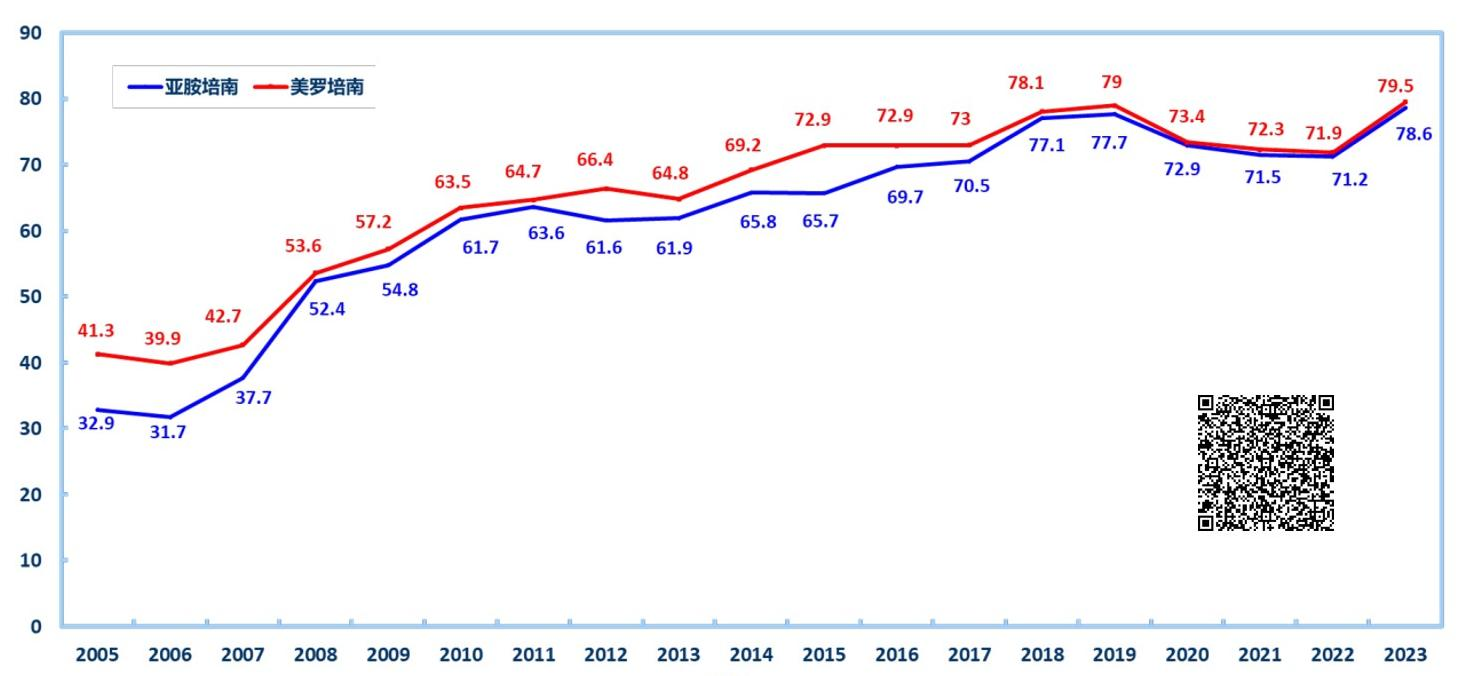
△鲍曼不动杆菌对亚胺培南和美罗培南的耐药变迁(来源:CHINET)
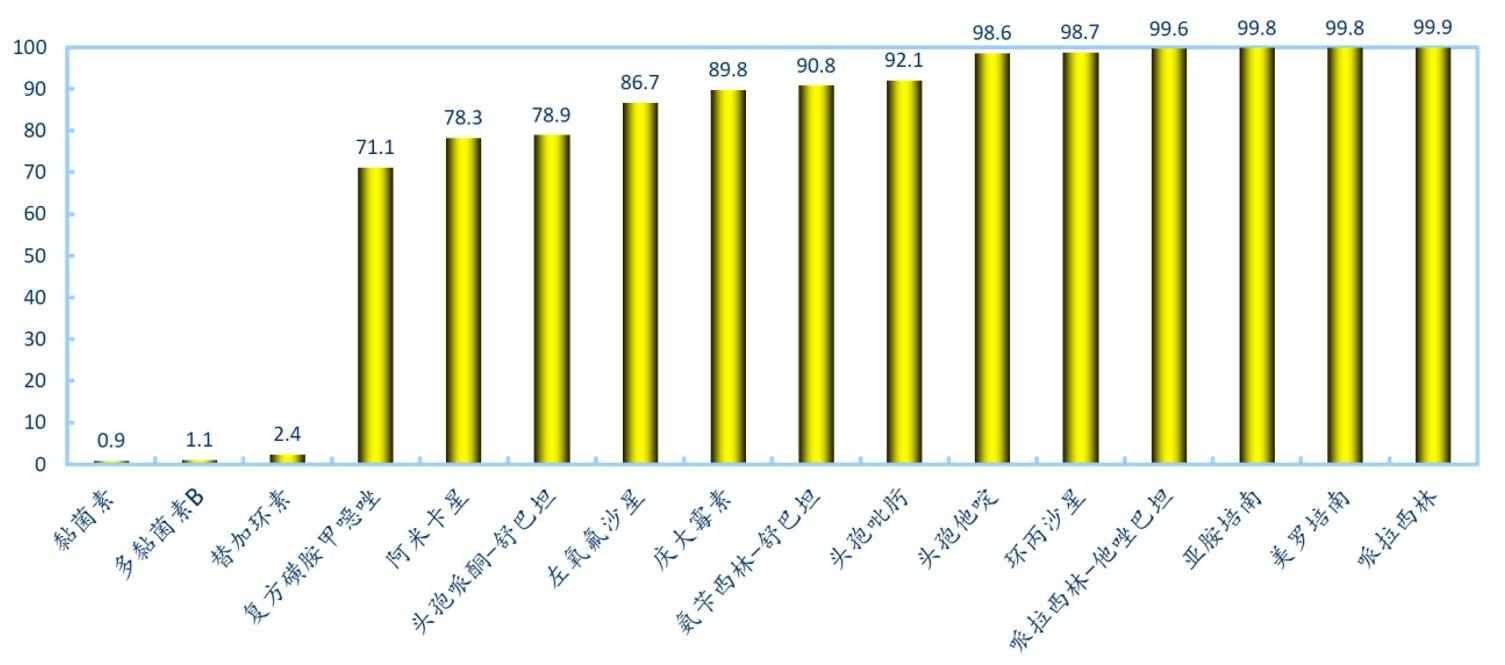
△2023上半年CRAB对抗菌药的耐药率(来源:CHINET)
CHINET 2022年监测结果显示,CRAB在我国多个省份呈高位流行,其中广西、黑龙江、辽宁等12个省/自治区的检出率已超过75%[2]。全国细菌耐药监测网(CARSS)2021年全国细菌耐药监测报告显示,CRAB在三级医院的检出率为55.4%,在重症患者中的检出率高达78.3%[3]。
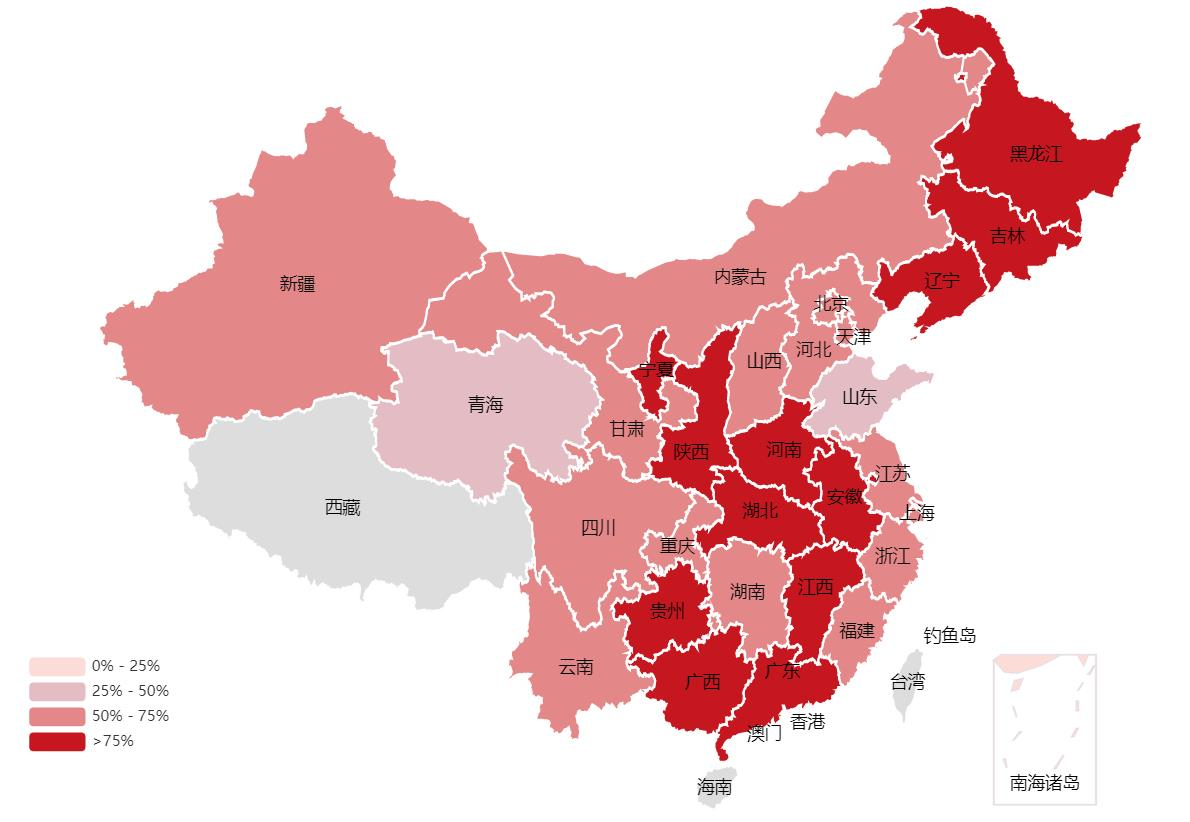
△各省市CRAB的检出率(2022年)(来源:CHINET)
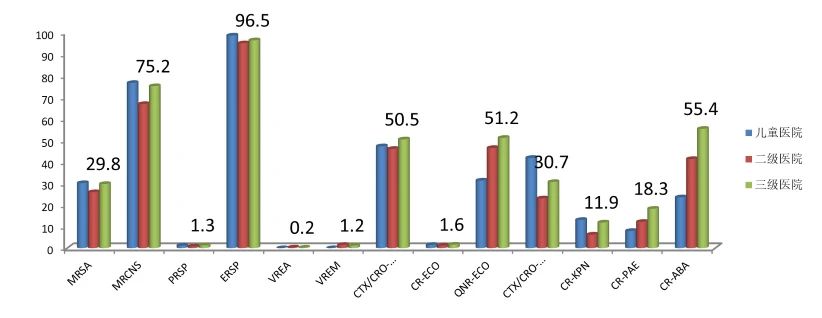
△不同等级医院常见耐药细菌的检出率(来源:CARSS)
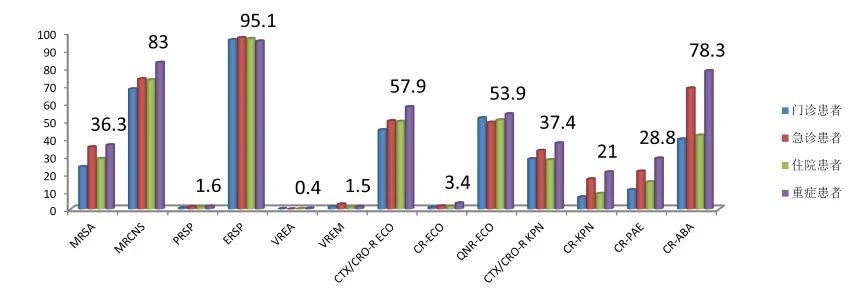
△医院不同区域常见耐药菌的检出率(来源:CARSS)
CRAB感染的治疗难度颇高。首先,CRAB通常在呼吸道标本或伤口标本中分离获得[4],因此临床医生常常很难准确判断分离株是定植还是感染,很难确定不良临床结局是由于抗感染疗效不佳还是潜在的宿主因素所造成的。
其次,当鲍曼不动杆菌对碳青霉烯类药物出现耐药时,通常也会对其他抗菌药物产生耐药性,使得抗感染治疗选择受限。CRAB的耐药机制复杂,如OXA-24/40型、OXA-23型等碳青霉烯酶介导对碳青霉烯类药物的耐药性[5-6];CRAB分离株也可能产金属β-内酰胺酶和丝氨酸碳青霉烯酶,从而进一步限制β-内酰胺类药物的临床应用[4]。
此外,目前尚无针对CRAB感染的“标准抗菌药物方案”,2023年版美国感染病学会(IDSA)指南建议使用至少两种活性药物联合治疗CRAB感染[4]。
新老交替
CRAB抗感染治疗药物的更新迭代
目前国内能够用于治疗CRAB感染的药物较为有限,主要依赖于替加环素、舒巴坦及其复合制剂、多黏菌素类抗菌药物。尤其以替加环素和黏菌素类药物为重。CRAB是CRO中耐药率最高的类型,且检出率逐渐增高,对临床威胁越来越大的今天,现有方案能否满足临床治疗需求?
现有药物难以满足临床需求
替加环素:研究显示,与治疗肺炎的其他方案相比,替加环素单药治疗的死亡率更高[7-10];如大使用剂量,其与对照药物的死亡率差异则不再明显[11-13];因此IDSA指南指出,如果选择替加环素治疗CRAB感染,建议使用高剂量,同时需要与至少一种其他药物联用。当然,高剂量使用可增加毒副作用风险,研究显示高维持剂量、延长疗程是替加环素相关性肝损伤的独立危险因素[14];另一项研究发现,替加环素导致的凝血障碍与剂量及疗程密切相关[15]。
舒巴坦及其复合制剂:舒巴坦合剂对不动杆菌属具良好的抗菌活性,但近年来不动杆菌属对该类药物的耐药率也在逐年攀升。CHINET 2023上半年数据显示,不动杆菌属对头孢哌酮/舒巴坦和氨苄西林/舒巴坦的耐药率已达59.7%和68.3%[2]。
多黏菌素类(黏菌素和多黏菌素B):虽然国内外多个指南/共识推荐多黏菌素用于耐药菌感染治疗。但考虑到多黏菌素血清浓度变化大、肾毒性强、肺上皮衬液活性不理想以及单药治疗临床失败率高,IDSA指南建议,对于CRAB引起的感染,使用多黏菌素B治疗时需与至少一种其他药物联用[4]。
新型药物崭露头角
随着全球药物研发进程的不断推进,近年来抗菌药物领域也涌现出了一些新面孔,多类抗菌药物均有新生力量加入,创新药物将为临床遏制耐药,尤其是为CRO抗感染治疗提供新的解决方案。
新型四环素及其衍生物:依拉环素是全球首个氟环素类抗菌药,使四环素类药物由半合成迈向了全合成时代。传统的生物合成和半合成法因难度大、结构变化受限等因素,极大限制了对四环素类抗菌药改造的发展空间。对核心D环引入氟原子修饰,使得依拉环素的药物性能得到全面提升。
新型铁载体头孢菌素:头孢地尔具有不易被水解的羧基丙氧基亚氨基和具有两性特质的吡咯烷环,增强了稳定性和水溶性。IDSA指南建议头孢地尔仅用于治疗因其他抗菌药物疗效不佳或不能耐受的CRAB感染,并建议将其与其他药物联用[4]。
新型多黏菌素:EVER206是一种新型多黏菌素类抗菌药,临床前研究显示其具有低细胞毒性和肾脏暴露的双重优点[16];Ⅰ期临床试验结果证实了EVER206所有给药剂量在健康受试者中的安全性和耐受性良好。
在上述新的具有抗CRAB活性的药物中,目前仅依拉环素已在国内获批上市,那么在治疗CRAB感染方面,依拉环素具有哪些优势呢?
创新改构
依拉环素抗菌作用全面升级
结构优化:依拉环素对核心D环进行了独特修饰[17],包括氟原子取代C-7处的二甲胺部分、吡咯烷乙酰氨基取代C-9处的2-叔丁基甘氨酰胺基[18]。四环素通过与细菌30S核糖体亚单位结合抑制蛋白质合成,与之相比,依拉环素与核糖体30S亚单位结合力增强14倍,使其具有更强的抗菌活性。
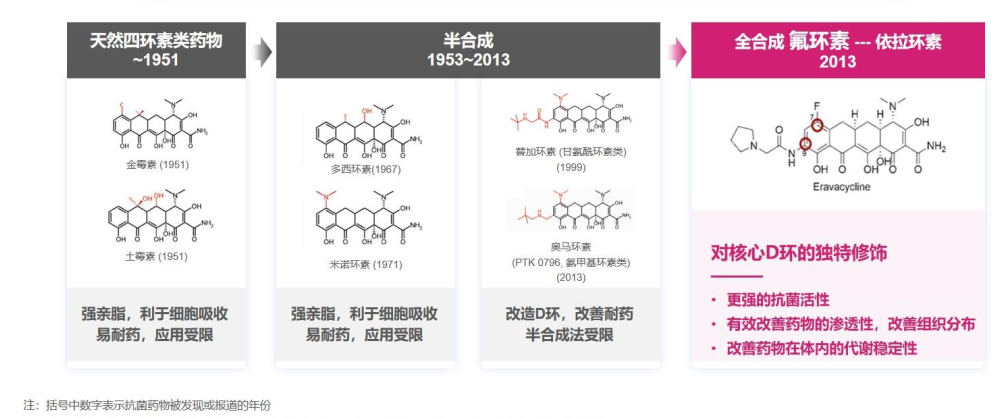
△从四环素到氟环素的发展历程
抗菌谱广、活性强:依拉环素可覆盖包括鲍曼不动杆菌在内的常见G-菌、G+菌和非典型病原菌,而且对多种耐药机制介导的MDR细菌也可以覆盖。同时,全球药敏数据(2017-2020)显示,依拉环素对鲍曼不动杆菌的体外抗菌活性是替加环素的4倍[19]。
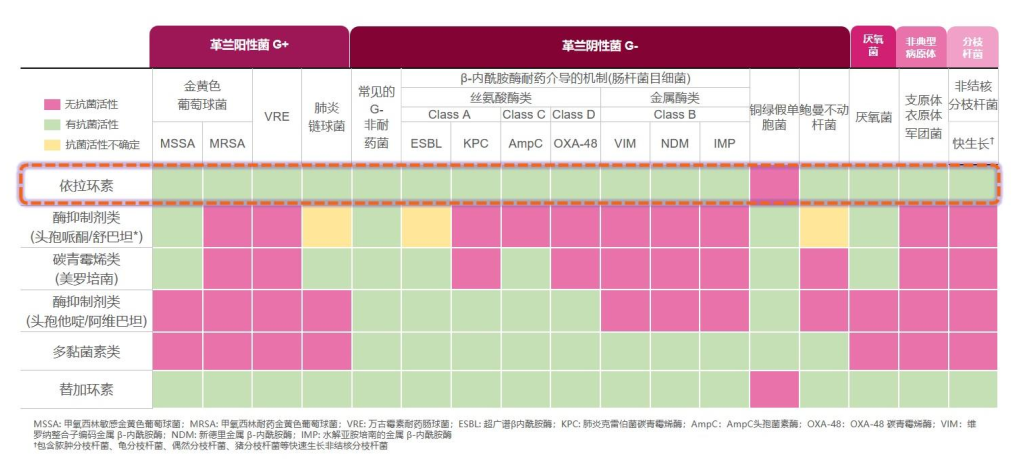
△依拉环素可覆盖常见多重耐药G-菌和G+菌
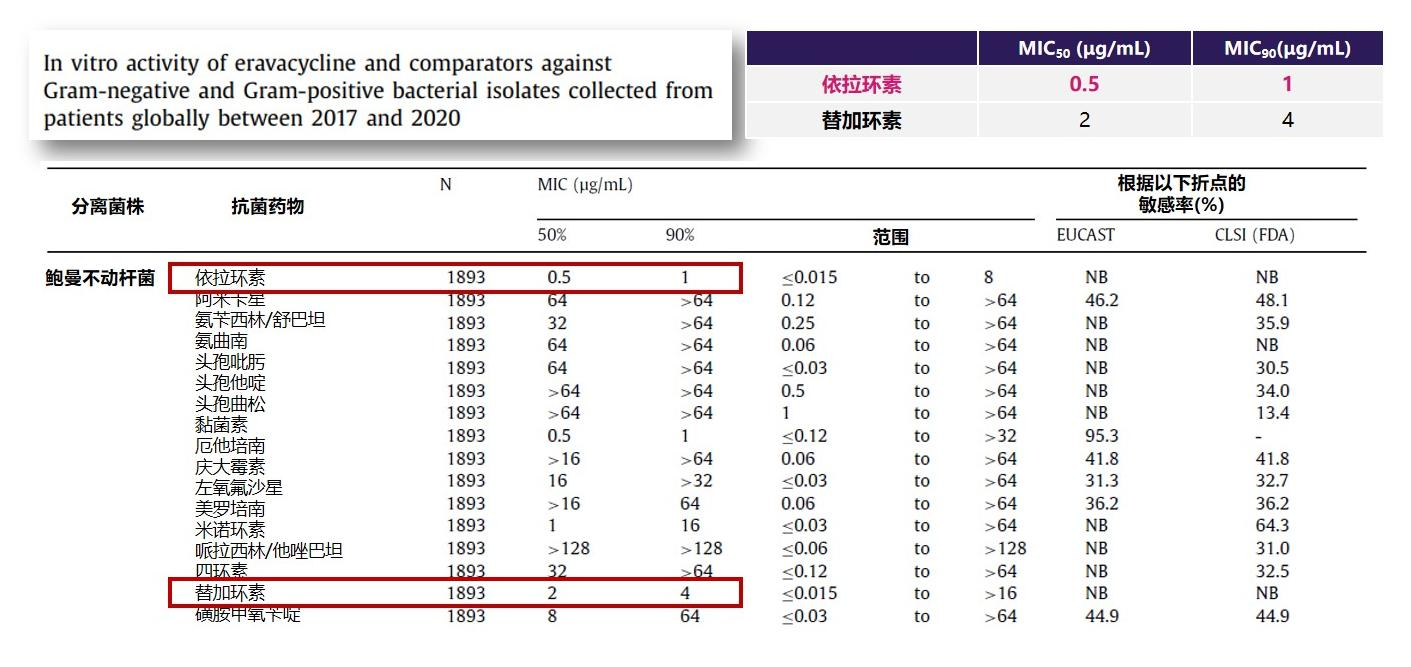
△依拉环素对鲍曼不动杆菌的体外抗菌活性是替加环素的4倍
联合用药协同无拮抗:研究发现依拉环素在与亚胺培南、头孢他啶、环丙沙星、头孢哌酮舒巴坦、阿米卡星、多黏菌素B联用时,对CRAB等耐药菌具有协同作用而无拮抗作用[20]。
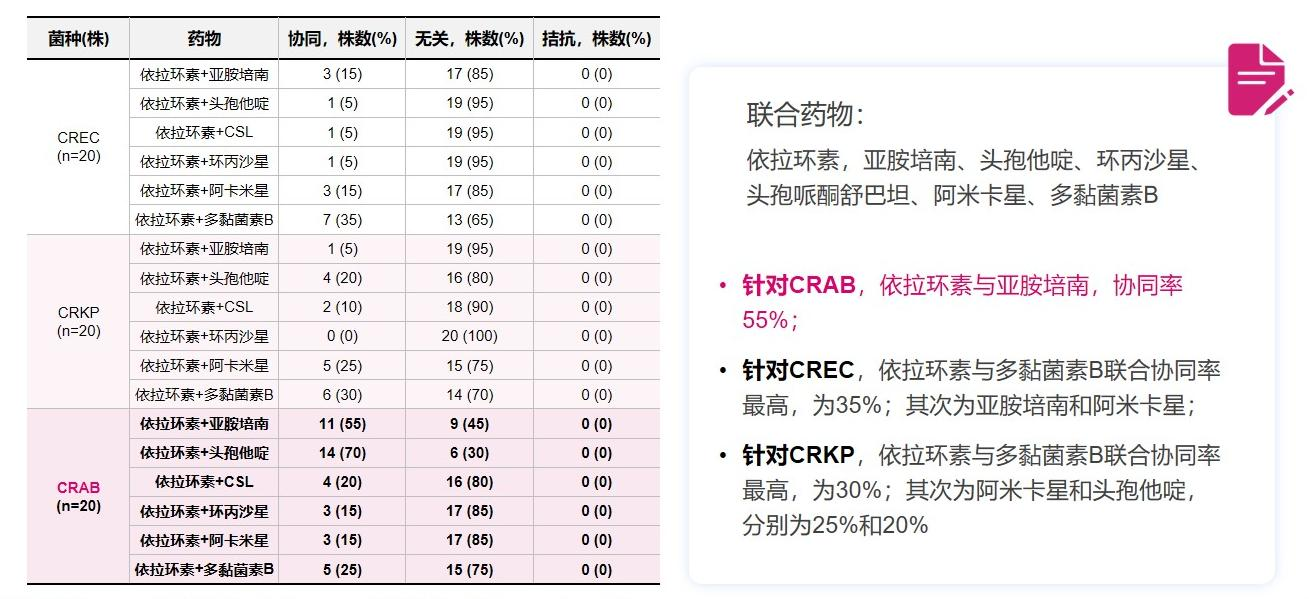
△依拉环素与试验药物联用对CREC、CRKP、CRAB具有协同和相加作用,无拮抗作用[20]
组织浓度高:依拉环素在体内分布广泛,依拉环素在体内分布广泛、组织中浓度高,蛋白结合率约为79%~90%,使用推荐剂量即可达较高成功率。

△依拉环素的组织浓度高、穿透性强
临床疗效和安全性好:依拉环素的疗效和安全性在多项真实世界研究中得到证实[21-24]。一项多中心、真实世界、观察性研究显示,依拉环素方案治疗CRAB感染患者的30天存活率可达78.1%[23];另一项回顾性病例系列研究显示,依拉环素方案治疗CRAB肺炎的临床缓解率可达72%[24]。
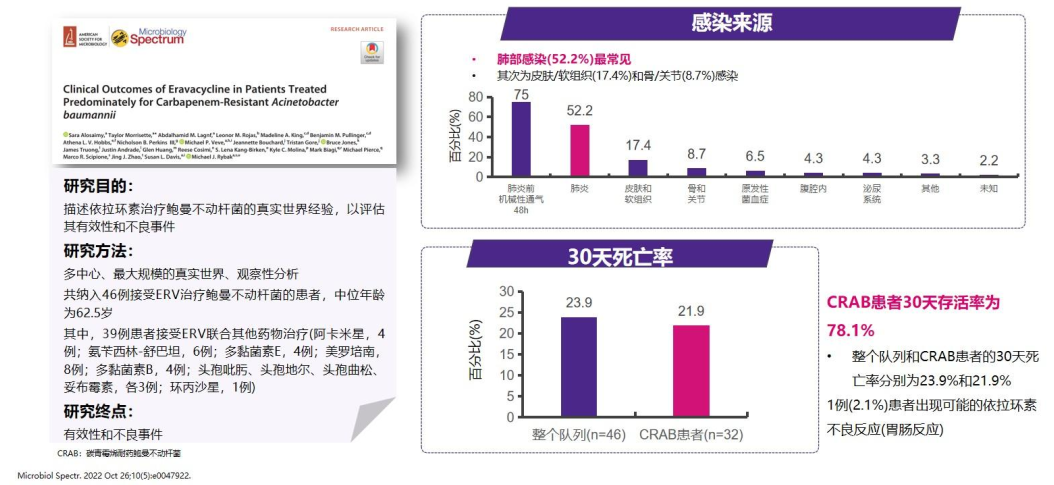
△依拉环素方案治疗CRAB感染[23]
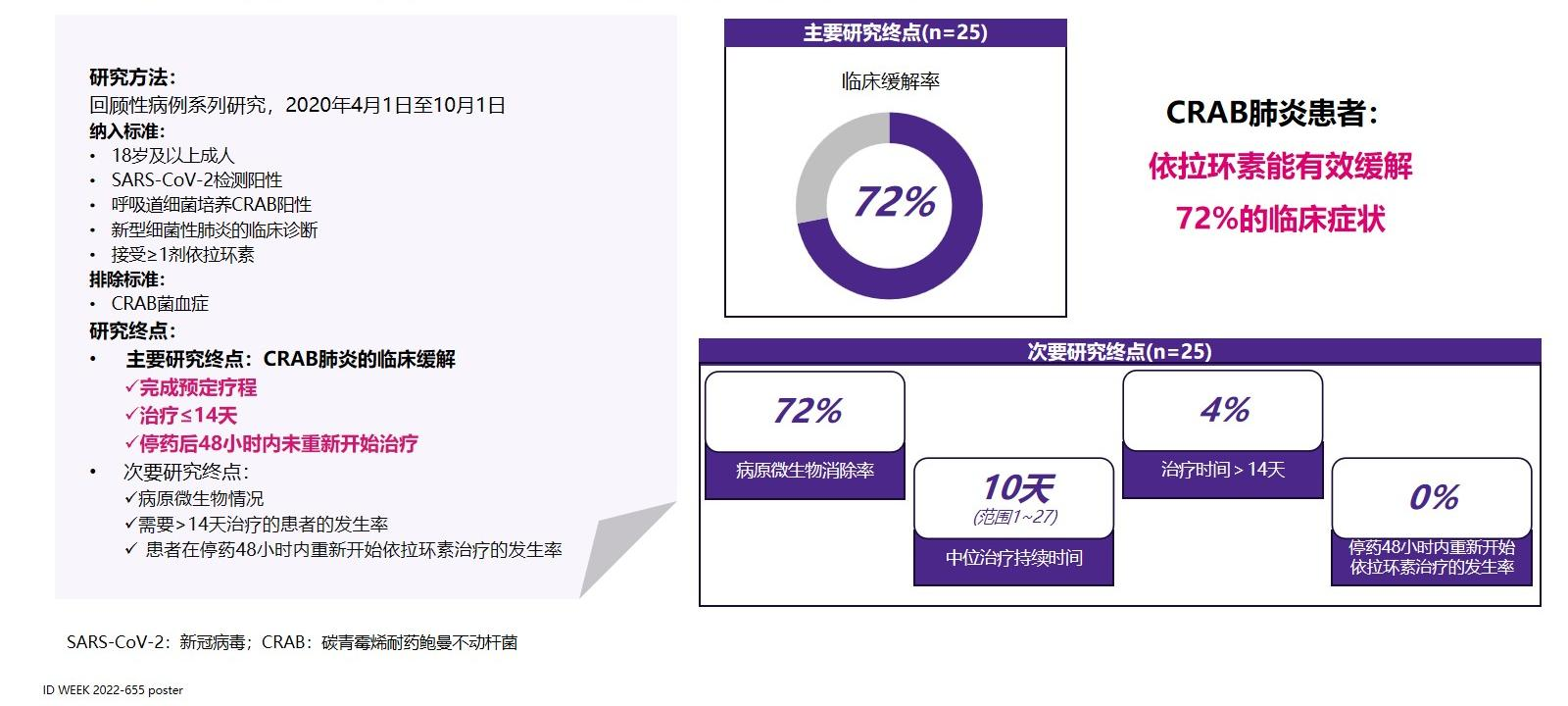
△依拉环素方案治疗CRAB肺炎[24]
基于充分的循证医学证据,依拉环素已获得IDSA耐药革兰阴性菌感染治疗指南、欧洲临床微生物与感染病学会(ESCMID)多重耐药革兰阴性菌感染治疗指南以及中国耐碳青霉烯类革兰阴性杆菌感染诊疗及防控指南等多个权威指南推荐[4, 26-27]。

△依拉环素得到多个国内外权威临床指南的推荐
总结
CRAB在国内一直处于高位流行,且有继续上升的趋势,而针对CRAB感染的治疗药物十分有限,创新药物的出现将对临床合理用药和遏制耐药菌感染起到积极作用。目前,依拉环素已在国内上市可及,创新改构使其抗菌作用得到全面优化,在未来的实践中也将使更多患者获益。同时,也期待更多新型药物的问世,实现治疗手段的多点开花。
参考文献
[1] 陈佰义,何礼贤,胡必杰,等.中国鲍曼不动杆菌感染诊治与防控专家共识[J].中华医学杂志,2012,92(2):76-85.DOI:10.3760/cma.j.issn.0376-2491.2012.02.002.
[2] 中国细菌耐药监测网(CHINET). www.chinets.com
[3] 全国细菌耐药监测网(CARSS). 2021年全国细菌耐药监测报告(简要版). available from: http://www.carss.cn/Report/Details/862
[4] Tamma PD, Aitken SL, Bonomo RA, Mathers AJ, van Duin D, Clancy CJ. Infectious Diseases Society of America 2023 Guidance on the Treatment of Antimicrobial Resistant Gram-Negative Infections [published online ahead of print, 2023 Jul 18]. Clin Infect Dis. 2023;ciad428. doi:10.1093/cid/ciad428
[5] Vijayakumar S, Biswas I, Veeraraghavan B. Accurate identification of clinically important Acinetobacter spp.: an update. Future Sci OA. 2019;5(6):FSO395. Published 2019 Jun 27. doi:10.2144/fsoa-2018-0127
[6] Turton JF, Ward ME, Woodford N, et al. The role of ISAba1 in expression of OXA carbapenemase genes in Acinetobacter baumannii. FEMS Microbiol Lett. 2006;258(1):72-77. doi:10.1111/j.1574-6968.2006.00195.x
[7] Yahav D, Lador A, Paul M, Leibovici L. Efficacy and safety of tigecycline: a systematic review and meta-analysis. J Antimicrob Chemother. 2011;66(9):1963-1971. doi:10.1093/jac/dkr242
[8] Liang CA, Lin YC, Lu PL, Chen HC, Chang HL, Sheu CC. Antibiotic strategies and clinical outcomes in critically ill patients with pneumonia caused by carbapenem-resistant Acinetobacter baumannii. Clin Microbiol Infect. 2018;24(8):908.e1-908.e7. doi:10.1016/j.cmi.2017.10.033
[9] Lee YT, Wang YC, Kuo SC, et al. Multicenter Study of Clinical Features of Breakthrough Acinetobacter Bacteremia during Carbapenem Therapy. Antimicrob Agents Chemother. 2017;61(9):e00931-17. Published 2017 Aug 24. doi:10.1128/AAC.00931-17
[10] Freire AT, Melnyk V, Kim MJ, et al. Comparison of tigecycline with imipenem/cilastatin for the treatment of hospital-acquired pneumonia. Diagn Microbiol Infect Dis. 2010;68(2):140-151. doi:10.1016/j.diagmicrobio.2010.05.012
[11] Zha L, Pan L, Guo J, French N, Villanueva EV, Tefsen B. Effectiveness and Safety of High Dose Tigecycline for the Treatment of Severe Infections: A Systematic Review and Meta-Analysis. Adv Ther. 2020;37(3):1049-1064. doi:10.1007/s12325-020-01235-y
[12] Chen Z, Shi X. Adverse events of high-dose tigecycline in the treatment of ventilator-associated pneumonia due to multidrug-resistant pathogens. Medicine (Baltimore). 2018;97(38):e12467. doi:10.1097/MD.0000000000012467
[13] De Pascale G, Montini L, Pennisi M, et al. High dose tigecycline in critically ill patients with severe infections due to multidrug-resistant bacteria. Crit Care. 2014;18(3):R90. Published 2014 May 5. doi:10.1186/cc13858
[14] Shi X, Zuo C, Yu L, et al. Real-World Data of Tigecycline-Associated Drug-Induced Liver Injury Among Patients in China: A 3-year Retrospective Study as Assessed by the Updated RUCAM. Front Pharmacol. 2021;12:761167. Published 2021 Nov 2. doi:10.3389/fphar.2021.761167
[15] Cui N, Cai H, Li Z, Lu Y, Wang G, Lu A. Tigecycline-induced coagulopathy: a literature review. Int J Clin Pharm. 2019;41(6):1408-1413. doi:10.1007/s11096-019-00912-5
[16] Brown P, Abbott E, Abdulle O, et al. Design of Next Generation Polymyxins with Lower Toxicity: The Discovery of SPR206. ACS Infect Dis. 2019;5(10):1645-1656. doi:10.1021/acsinfecdis.9b00217
[17] Sutcliffe JA, O'Brien W, Fyfe C, Grossman TH. Antibacterial activity of eravacycline (TP-434), a novel fluorocycline, against hospital and community pathogens. Antimicrob Agents Chemother. 2013;57(11):5548-5558
[18] Zhanel GG, Cheung D, Adam H, et al. Review of Eravacycline, a Novel Fluorocycline Antibacterial Agent. Drugs. 2016;76(5):567-588.
[19] Hawser S, Kothari N, Monti F, Morrissey I, Siegert S, Hodges T. In vitro activity of eravacycline and comparators against Gram-negative and Gram-positive bacterial isolates collected from patients globally between 2017 and 2020. J Glob Antimicrob Resist. 2023;33:304-320. doi:10.1016/j.jgar.2023.04.017
[20] Li Y, Cui L, Xue F, Wang Q, Zheng B. Synergism of eravacycline combined with other antimicrobial agents against carbapenem-resistant Enterobacteriaceae and Acinetobacter baumannii. J Glob Antimicrob Resist. 2022;30:56-59. doi:10.1016/j.jgar.2022.05.020
[21] Van Hise N, Petrak RM, Skorodin NC, et al. A Real-World Assessment of Clinical Outcomes and Safety of Eravacycline: A Novel Fluorocycline. Infect Dis Ther. 2020;9(4):1017-1028. doi:10.1007/s40121-020-00351-0
[22] Hobbs ALV, Gelfand MS, Cleveland KO, Saddler K, Sierra-Hoffman MA. A retrospective, multicentre evaluation of eravacycline utilisation in community and academic hospitals. J Glob Antimicrob Resist. 2022;29:430-433. doi:10.1016/j.jgar.2021.10.020
[23] Alosaimy S, Morrisette T, Lagnf AM, et al. Clinical Outcomes of Eravacycline in Patients Treated Predominately for Carbapenem-Resistant Acinetobacter baumannii. Microbiol Spectr. 2022;10(5):e0047922. doi:10.1128/spectrum.00479-22
[24] ID WEEK 2022-655 poster
[26] Paul M, Carrara E, Retamar P, et al. European Society of Clinical Microbiology and Infectious Diseases (ESCMID) guidelines for the treatment of infections caused by multidrug-resistant Gram-negative bacilli (endorsed by European society of intensive care medicine). Clin Microbiol Infect. 2022;28(4):521-547. doi:10.1016/j.cmi.2021.11.025
[27] Zeng M, Xia J, Zong Z, et al. Guidelines for the diagnosis, treatment, prevention and control of infections caused by carbapenem-resistant gram-negative bacilli. J Microbiol Immunol Infect. 2023;56(4):653-671. doi:10.1016/j.jmii.2023.01.017
往期推荐
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
.png)
责任编辑:彭伟彬
相关搜索: 依拉环素