- 首页 > 正文
科学治疗HIV晚发现者!全面了解HIV晚发现者的治疗考量因素丨热点争鸣
感染医线 发表时间:2023/9/14 17:52:24
在前两期“HIV晚发现者”系列文章中,我们分别讨论了HIV晚发现者的重新定义,危害、流行趋势、疾病特征和预防。本期中,我们特邀中国医学科学院北京协和医院的吕玮教授为大家介绍HIV晚发现者的治疗方案及考量因素。
01
快速启动抗反转录病毒治疗
目前,各大国际指南均建议,无论CD4细胞计数如何,HIV感染者在诊断后有条件的情况下应尽早启动抗反转录病毒治疗(ART)[1-4],欧洲艾滋病临床学会(EACS)指南特别指出,CD4细胞计数<350个/μL的HIV晚发现者不应延迟ART启动[4]。
快速启动ART对于HIV感染者自身来说,可以更快达到病毒学抑制[5],降低炎症水平及AIDS、非AIDS相关严重事件和死亡风险[6],从公共卫生层面来说,可以增加晚发现者接受ART的比例[7],提高病毒学抑制率从而降低HIV传播风险[8,9]。
中国艾滋病综合防治信息管理系统(CRIMS)2006-2014年登记的52万余例HIV感染者中,34.0%为晚发现者(确诊AIDS或世界卫生组织定义的3/4级HIV/AIDS,或CD4细胞计数<200个/μL),确诊后第一年内,未接受ART的晚发现者有46.1%死亡,而接受了ART的仅为7.4%,晚发现者确诊后及早启动ART显著降低了死亡率[10]。
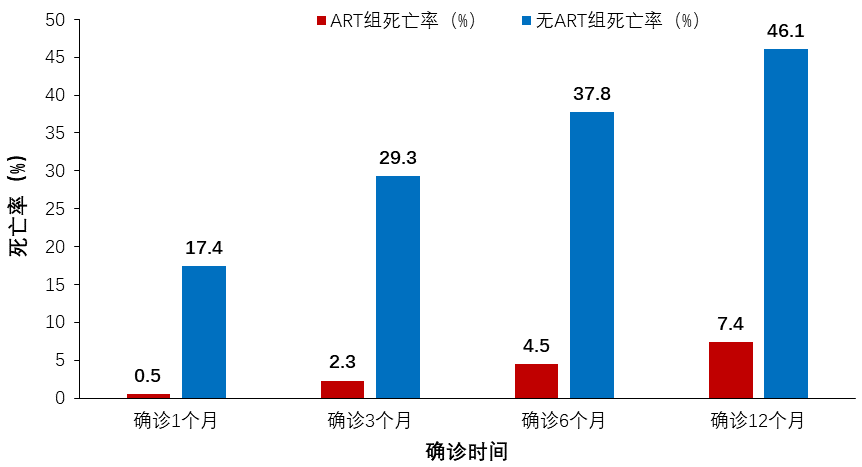
HIV晚发现者确诊后第一年内接受ART(红)和未接受ART(蓝)的死亡率
在各国际指南推荐的一线方案中,比克替拉韦/恩曲他滨/丙酚替诺福韦(B/F/TAF)被推荐用于快速启动,特别是确诊后当天启动,不受耐药检测结果、HBV合并感染、病毒载量和CD4细胞计数的影响[2-4]。
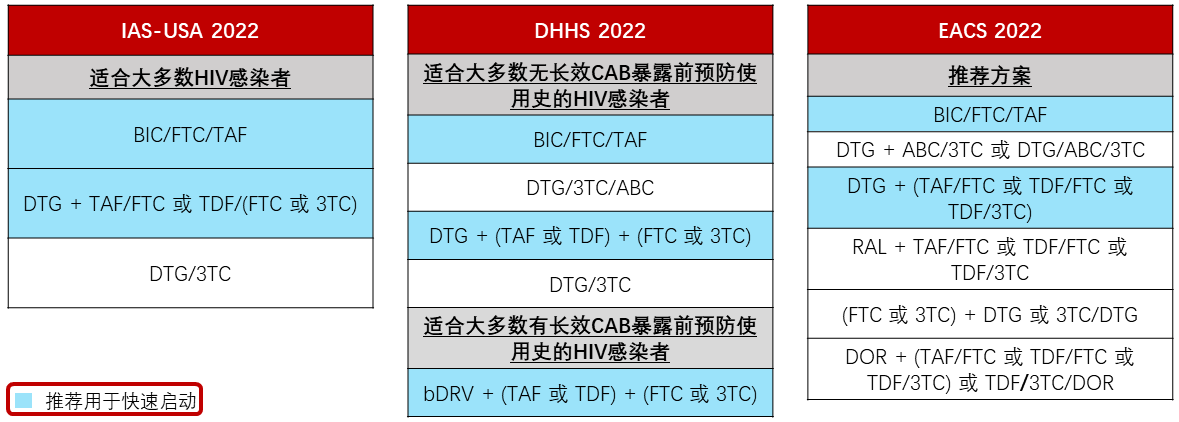
美国卫生与人类服务部(DHHS)、国际抗病毒学会(IAS)和EACS指南推荐的一线方案[2-4]
多替拉韦/拉米夫定(DTG/3TC)方案对病毒载量、耐药检测和HBV血清学结果有要求[3],含阿巴卡韦(ABC)的三联方案需HLA-B*57:01和HBsAg阴性[4],多拉韦林(DOR)方案需要耐药检测结果[4],其他可选方案中,基于利匹韦林(RPV)的三联方案[2-4]和达芦那韦/利托那韦+拉替拉韦(DRV/r+RAL)[2]不适用于CD4细胞计数≤200个/μL的HIV感染者,故均不适用于快速启动。
需在高危人群ART启动前进行系列筛查,例如合并感染,绝经后女性、老年男性和有骨折或性腺功能减退史个体的骨密度筛查,有怀孕可能性个体的妊娠筛查,以及初治或因治疗失败而转换治疗方案个体的基因型耐药检测[11]。
02
选择强效ART方案以快速控制病毒载量和免疫功能重建
HIV晚发现者通常具有较高的病毒载量和较低的CD4细胞计数,北京协和医院李太生教授团队开展了一项回顾性研究[12],基于两项中国HIV感染者多中心研究,在2009年和2013-2015年间共纳入758例感染者,接受非核苷类反转录酶抑制剂(NNRTI)联合2种核苷类反转录酶抑制剂(NRTI)治疗,34.2%的治疗前HIV RNA≥100,000拷贝/mL,76.1%的CD4细胞计数<350个/μL。
与HIV RNA<100,000拷贝/mL相比,100,000≤HIV RNA<500,000拷贝/mL和HIV RNA≥500,000拷贝/mL与病毒学抑制延迟、不完全病毒学抑制和病毒学反弹有关。因此,治疗前高病毒载量的HIV感染者应考虑更强效的ART启动方案。
同时也观察到ART药物的类别对晚发现者疗效的影响,西班牙的一项研究[13]选取了开放性多中心PISCIS队列研究中2010-2020年间入组的1594例初治HIV晚发现者(CD4细胞计数<200个/μL和/或存在AIDS定义性疾病),其中46.9%接受基于整合酶抑制剂(INSTI)的ART方案,35.7%接受基于蛋白酶抑制剂(PI)的方案,17.4%接受基于非核苷类反转录酶抑制剂(NNRTI)的方案,中位随访时间为4.4年。
随访结束时,PI、NNRTI和INSTI组5年总死亡率分别为9.5%、6.1%和3.5%(p<0.001),基于INSTI的方案与死亡风险下降50%有关。
INSTI组达到病毒学抑制(HIV RNA≤50拷贝/mL)的时间为0.3年,早于NNRTI组(0.4年)和PI组(0.5年),实现免疫重建所需的时间更短可能是死亡率更低的原因。这表明,HIV晚发现者接受基于INSTI的ART方案能够更快达到病毒学抑制和免疫重建,降低长期死亡风险。
在两项双盲、多中心、非劣效性临床研究中,研究人员分别比较了B/F/TAF和DTG/ABC/3TC、B/F/TAF和DTG+F/TAF在初治HIV感染者中的有效性和安全性(1489和1490研究)。
随访96周时,汇总的遵循研究方案(PP)分析显示,所有参与者、基线HIV RNA>100,000拷贝/mL、基线CD4细胞计数<200个/μL,以及基线HIV RNA>100,000拷贝/mL且CD4细胞计数<200个/μL的亚组中,三种方案均具有高病毒学抑制率,没有参与者因疗效不佳停药或出现耐药[14]。
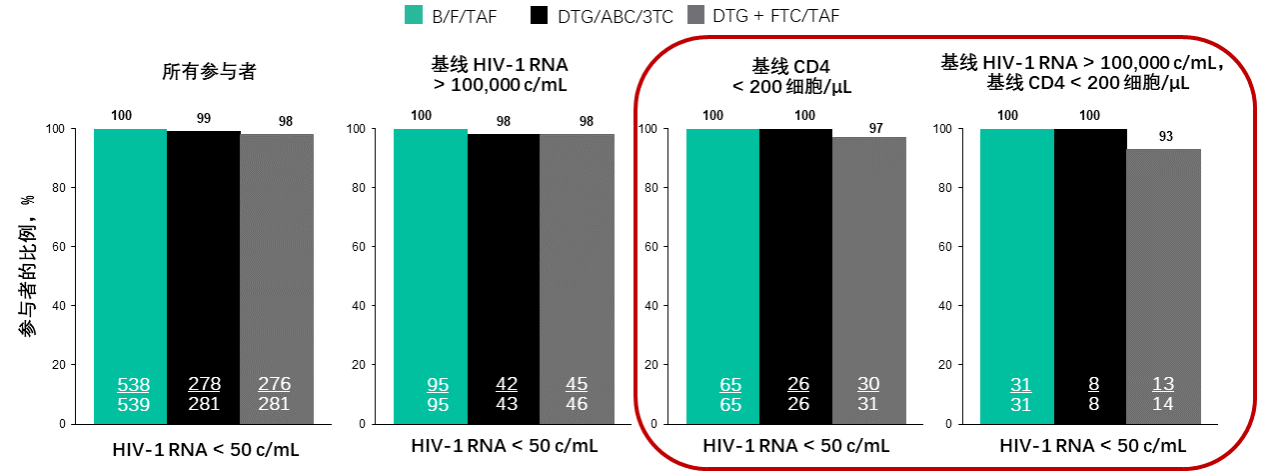
HIV RNA<50拷贝/mL的患者比例
一项基于OPERA队列的分析研究[15]纳入了2018- 2019年间启动ART的961例HIV晚发现者(CD4细胞计数<200个/μL),接受B/F/TAF(43%)、增效DRV(bDRV)+2种核苷类反转录酶抑制剂(NRTI)(11%)、DTG+2 NRTI(28%)或艾维雷韦/考比司他(EVG/c)+2 NRTI(18%)治疗。最长随访时间为31个月。有随访数据的771例参与者中,B/F/TAF组未校正的病毒学抑制率(HIV RNA<50拷贝/mL)高于bDRV组(70.9)、DTG组(81.1)和EVG/c组(85.5)。校正后分析显示,与B/F/TAF相比,bDRV与病毒学抑制风险比显著降低28%有关。bDRV组、DTG组和EVG/c组停药(校正后分析)风险分别是B/F/TAF组的2.65倍、2.42倍和3.52倍。
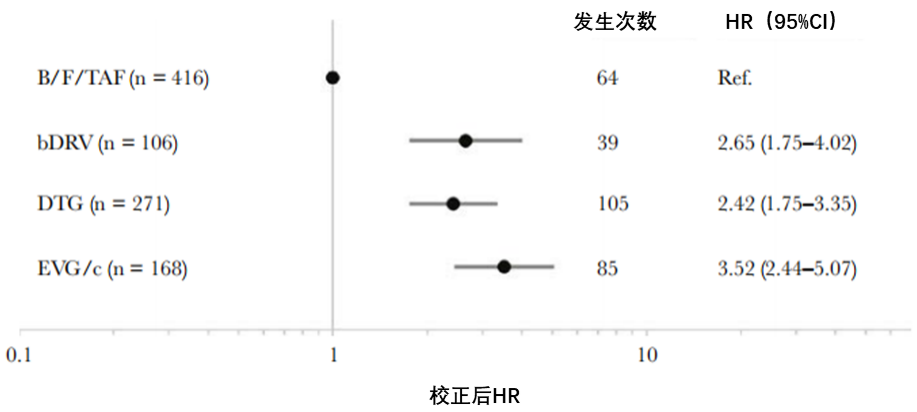
与B/F/TAF相比,bDRV、DTG和EVG/c方案均与停药风险增加有关
另一项同样基于OPERA队列的分析研究[16]发现了B/F/TAF在免疫恢复方面的优势。研究纳入了2018-2020年间启动ART的1349例HIV晚发现者(CD4细胞计数<200个/μL),所有参与者均接受三联方案,60%为B/F/TAF,19%为DTG方案,11%为EVG/c方案,10%为bDRV方案。中位随访时间为22个月。
在ART启动后中位时间3个月内,B/F/TAF组有77%的参与者CD4细胞计数恢复至200个/μL以上,显著高于bDRV组(63%)、DTG组(70%)和EVG/c组(60%)。
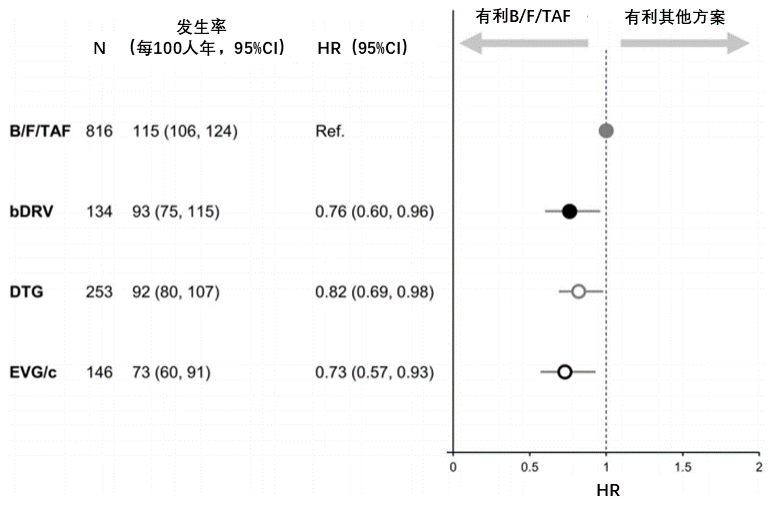
B/F/TAF、bDRV、DTG和EVG/c方案与CD4细胞计数恢复的相关性
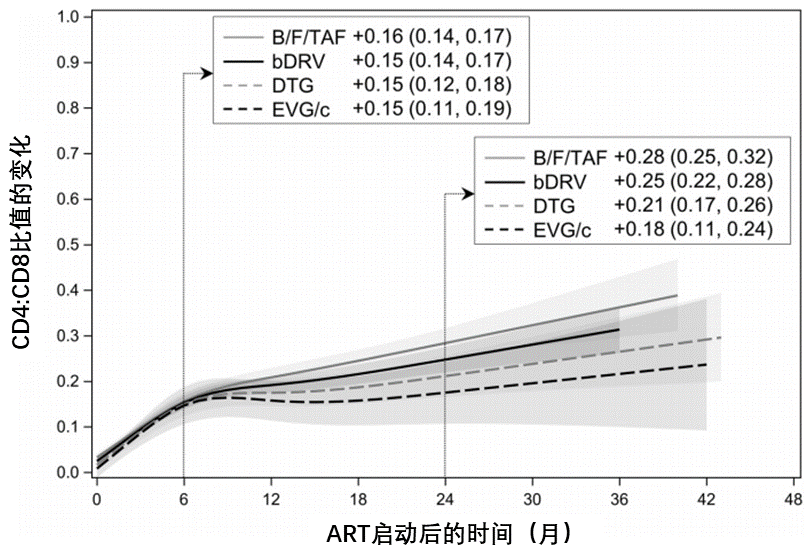
ART启动后48个月内,B/F/TAF、bDRV、DTG和EVG/c组的CD4:CD8比值恢复情况
有85%的参与者在ART启动后中位时间2个月内达到病毒学抑制(HIV RNA<200拷贝/mL),B/F/TAF组有90%,显著高于bDRV组(72%)、DTG组(82%)和EVG/c组(75%)。共398例参与者停药,B/F/TAF组有149例,占组内参与者的18%,bDRV组有51例,占38%,DTG组有121例,占48%,EVG/c组有77例,占53%。与B/F/TAF相比,其余三组中止/转换方案风险均显著增加。
这些结果表明,使用B/F/TAF与更快的CD4细胞计数恢复、更高的病毒学抑制率和更低的停药率有关。
在中国台湾开展的一项回顾性多中心研究[17]在2019-2020年间纳入了162例HIV晚发现者(CD4细胞计数<200个/μL或在ART启动前/时存在AIDS相关机会性感染疾病[AOI]),接受B/F/TAF或DTG/ABC/3TC治疗。
48周时,两组的病毒学抑制率(HIV RNA<50拷贝/mL)分别为85.71%和73.47%(p=0.178),共发生25例停药(15.04%),B/F/TAF组有4例(6.35%),DTG/ABC/3TC组有21例(21.21%)(p=0.017),启动至停药的中位时间分别为22天和57天,相比使用DTG/ABC/3TC,使用B/F/TAF与停药风险降低77%有关(p=0.027)。
这表明,同为单片制剂方案,B/F/TAF与DTG/ABC/3TC在病毒学抑制和病毒学失败方面没有差异,但B/F/TAF的停药风险显著降低。
治疗依从性不足是ART结局不佳的主要原因之一,除了ART药物外,HIV晚发现者通常需要同时使用其它药物治疗或预防机会性感染,尤其是CD4细胞计数<200个/μL的晚发现者,较高的药物负担会降低治疗依从性,而新一代ART药物的复方单片制剂有利于降低药片负担,提高治疗依从性[11]。
03
机会性感染与ART方案
低CD4细胞计数是机会性感染的独立风险因素,且与机会性感染次数和死亡率显著相关[18,19],因此,HIV晚发现者合并机会性感染风险更高,可能会影响ART的启动时机、方案选择和预后。
根据各大国际指南,大多数合并机会性感染者可在启动抗机会性感染治疗1-2周内启动ART[2-4],部分机会性感染会影响ART的启动时机,例如隐球菌脑膜炎和结核性脑膜炎,如存在结核性脑膜炎,ART启动应延迟至抗结核后的4-8周,如同时伴CD4细胞计数<50(100)个/μL,可在2周内启动ART,如存在隐球菌脑膜炎,ART启动应延迟至少4周[4]。
由于基线CD4细胞计数和病毒载量、机会性感染,以及ART启动时间等均是免疫重建炎症综合征(IRIS)的风险因素[20,21],因此,在ART启动前需做好机会性感染的筛查、预防和治疗,评估IRIS发生风险以优化ART启动时机,如发生IRIS,则应在继续ART的同时,根据IRIS和机会性感染的类型进行相应治疗。
许多机会性感染仍无有效治疗方法,例如日本脑炎病毒相关进行性多灶性白质脑病,ART能够有效促进免疫重建,从而成为最好的防御手段[11]。
各大指南并未对合并机会性感染的晚发现者的ART方案进行特别推荐,但考虑晚发现者可能CD4细胞计数很低,可参照指南中对于低 CD4细胞计数者的治疗推荐。对于 CD4 细胞计数<200个/μL的感染者,指南不建议使用基于RPV的方案、DRV/r+RAL以及齐多夫定(AZT),DTG/3TC在CD4细胞计数<200个/μL的HIV感染者中疗效欠佳[22]。HIV晚发现者可选择疗效不受基线CD4细胞计数影响的方案。
04
专家点评
所有HIV感染者在有条件的情况下均应尽快启动ART,这一点在HIV晚发现者中意义尤为重要,是减少HIV传播,改善晚发现者预后的关键因素。
中国的HIV晚发现者通常基线CD4细胞计数低、病毒载量高,合并机会性感染风险高,对ART启动时机和方案选择都提出了挑战,目前使用比例较高的基于NNRTI的ART方案对高病毒载量患者病毒抑制率比较低和病毒学失败风险增加,免疫重建较慢,另外,有研究显示,2年内的免疫恢复是HIV晚发现者长期死亡率的重要预测因子,良好的免疫恢复可以使晚发现者的预期寿命接近非晚发现者[23]。
因此,需考虑能够提高病毒学抑制率和速度,加快免疫恢复的优化ART方案。根据各大国际指南的推荐,在有条件的情况下,可为HIV晚发现者选择符合这些需求的基于INSTI的ART方案,例如B/F/TAF。前文中基于OPERA队列的分析研究[16]也显示,bDRV和DTG组分别有39%和24%的参与者因简化方案而停药,随时间推移,HIV晚发现者启动ART时选择B/F/TAF的比例升高,表现出“倾向于新ART方案”的趋势。
与一般人群相比,HIV感染者的年龄相关非感染性合并症发生风险较高,且发生年龄较早,例如慢性肾病和心脏疾病,通常与慢性免疫激活有关。HIV感染者的合并症与HIV感染本身需同时进行治疗和管理,这仍是目前的一个重要挑战[11]。
总而言之,HIV晚发现者作为HIV相关公共卫生领域的重点监测人群,需要从筛查、治疗到随访完善的全病程管理,目前,我国为了应对HIV晚发现问题制定了“One4All”策略,旨在将快速即时的病毒载量和CD4细胞计数检测集中在同一时间地点进行,以促进快速完整的诊断和分期,为符合条件的HIV感染者提供即时咨询并尽早启动ART,这一策略的实施将降低晚发现而导致的HIV传播,并有助于改善HIV晚发现者的预后[24]。
参考文献
[1] 中华医学会感染病学分会艾滋病丙型肝炎学组. 中国艾滋病诊疗指南(2021年版)[J]. 中国艾滋病性病杂志, 2021, 27: 1182-1201.
[2] DHHS. Guidelines for the Use of Antiretroviral Agents in Adults and Adolescents Living with HIV. Accessed: March 2023. Available at: https://clinicalinfo.hiv.gov/sites/default/files/guidelines/documents/adult-adolescent-arv/guidelines-adult-adolescent-arv.pdf.
[3] Gandhi R T, Bedimo R, Hoy J F, et al. Antiretroviral drugs for treatment and prevention of HIV infection in adults: 2022 recommendations of the International Antiviral Society–USA Panel[J]. JAMA, 2023, 329(1): 63-84.
[4] EACS. Guidelines for treatment of people living with HIV version 11.1. Accessed: October 2022. Available at: https://www.eacsociety.org/media/guidelines-11.1_final_09-10.pdf.
[5] Pilcher C D, Ospina-Norvell C, Dasgupta A, et al. The effect of same-day observed initiation of antiretroviral therapy on HIV viral load and treatment outcomes in a US public health setting[J]. Journal of acquired immune deficiency syndromes, 2017, 74(1): 44.
[6] Baker J V, Sharma S, Grund B, et al. Systemic inflammation, coagulation, and clinical risk in the START trial[C]//Open Forum Infectious Diseases. US: Oxford University Press, 2017, 4(4): ofx262.
[7] 董玉连, 农桂德, 毛艳芳, 等. 广西钟山县艾滋病检测与治疗 “一站式服务” 模式效果[J]. 中国热带医学, 2017, 17(2): 163-166.
[8] Insight Start Study Group. Initiation of antiretroviral therapy in early asymptomatic HIV infection[J]. New England Journal of Medicine, 2015, 373(9): 795-807.
[9] Cohen M S, Chen Y Q, McCauley M, et al. Antiretroviral therapy for the prevention of HIV-1 transmission[J]. New England Journal of Medicine, 2016, 375(9): 830-839.
[10] Tang H, Mao Y, Tang W, et al. “Late for testing, early for antiretroviral therapy, less likely to die”: results from a large HIV cohort study in China, 2006–2014[J]. BMC infectious diseases, 2018, 18: 1-13.
[11] Wong C S, Wei L, Kim Y S. HIV Late Presenters in Asia: Management and Public Health Challenges[J]. AIDS Research and Treatment, 2023, 2023.
[12] Chen S, Han Y, Song X J, et al. Very high baseline HIV viremia impairs efficacy of non-nucleoside reverse transcriptase inhibitor-based ART: a long-term observation in treatment-na?ve patients[J]. Infectious Diseases of Poverty, 2020, 9(1): 1-10.
[13] Burgos J, Moreno-Fornés S, Reyes-Urue?a J, et al. Mortality and immunovirological outcomes in patients with advanced HIV disease on their first antiretroviral treatment: differential impact of antiretroviral regimens[J]. Journal of Antimicrobial Chemotherapy, 2023, 78(1): 108-116.
[14] Podzamczer D, et al. HIV Drug Therapy 2018. Glasgow, UK. Poster 119.
[15] Mounzer K, Brunet L, Fusco J S, et al. Advanced HIV infection in treatment-na?ve individuals: effectiveness and persistence of recommended 3-drug regimens[C]//Open Forum Infectious Diseases. US: Oxford University Press, 2022, 9(3): ofac018.
[16] Mounzer K, Brunet L, Fusco J S, et al. Immune response to ART initiation in advanced HIV infection[J]. HIV medicine, 2023.
[17] Lee C Y, Lee C H, Tang H J, et al. Comparison of Virological Efficacy of DTG/ABC/3TG and B/F/TAF Regimens and Discontinuation Patterns in Persons Living with Advanced HIV in the Era of Rapid ART: A Retrospective Multicenter Cohort Study[J]. Infectious Diseases and Therapy, 2023, 12(3): 843-861.
[18] Pang W, Shang P, Li Q, et al. Prevalence of opportunistic infections and causes of death among hospitalized HIV-infected patients in Sichuan, China[J]. The Tohoku journal of experimental medicine, 2018, 244(3): 231-242.
[19] Zhang F, Dou Z, Yu L, et al. The effect of highly active antiretroviral therapy on mortality among HIV-infected former plasma donors in China[J]. Clinical infectious diseases, 2008, 47(6): 825-833.
[20] 李彦媚, 周海卫, 曾辉, 等. 艾滋病免疫重建炎症综合征研究进展[J]. 中华实验和临床感染病杂志(电子版), 2013, 7(5): 121-124.
[21] Walker N F, Scriven J, Meintjes G, et al. Immune reconstitution inflammatory syndrome in HIV-infected patients[J]. HIV/AIDS-Research and Palliative Care, 2015, 7: 49-64.
[22] Saag M S, Gandhi R T, Hoy J F, et al. Antiretroviral drugs for treatment and prevention of HIV infection in adults: 2020 recommendations of the International Antiviral Society–USA panel[J]. JAMA, 2020, 324(16): 1651-1669.
[23] Martin-Iguacel R, Reyes-Uruena J, Bruguera A, et al. Determinants of long-term survival in late HIV presenters: the prospective PISCIS cohort study[J]. EClinicalMedicine, 2022, 52: 101600.
[24] Wu Z, Tang Z, Mao Y, et al. Testing and linkage to HIV care in China: a cluster-randomised trial[J]. The lancet HIV, 2017, 4(12): e555-e565.
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
.png)
责任编辑:彭伟彬
相关搜索: HIV