- 首页 > 正文
各有千秋,择优而用!两性霉素B不同制剂的结构功能差异
感染医线 发表时间:2023/9/2 17:16:13
近年来,随着免疫缺陷人群的增加、免疫抑制剂和抗肿瘤靶向药物使用的增多,在接受化疗的血液恶性肿瘤患者中,侵袭性真菌病(IFD)的发生风险呈上升趋势[1]。尤其是接受造血干细胞移植的患者,确诊和临床诊断IFD的发生率可达7.7%,拟诊IFD发生率为19%[1]。IFD诊断困难,花费巨大,已成为威胁人类健康的重要公共卫生问题。
多烯类抗真菌药物两性霉素B(AMB)在临床长期使用过程中,很少有耐药菌株出现,所以AMB在很长一段时间内被认为是治疗深部真菌感染的“金标准”[2]。但由于传统两性霉素B(cAmB)的肾毒性及输注相关不良反应较大,严重影响着临床应用[3]。那么cAmB产生相关副作用机制是什么?临床中又该如何兼顾AMB的疗效及安全性而选择合适的制剂呢?
一、 cAmB的相关毒性
cAmB以两性霉素B脱氧胆酸盐(D-AmB)为经典制剂,D-AmB进入血液后,AMB分子与脱氧胆酸盐分离,以游离形式存在并发挥作用,AMB通过与真菌细胞膜上的麦角固醇结合,在细胞膜上形成管状离子通道,使得电解质等胞内物质外流从而导致真菌细胞死亡 [4]。
研究发现,D-AmB入血后产生大量游离AMB,迅速先与血浆脂蛋白中的高密度脂蛋白(HDL)结合,继而与低密度脂蛋白(LDL)结合。而肾小管上皮细胞表面存在着丰富的LDL受体,AMB得以迅速到达至肾远端小管上皮细胞处,并与其细胞膜中的胆固醇结合,产生跨膜孔洞,导致胞内物质外流,直接损伤肾小管上皮细胞[5],产生肾毒性。此外,AMB还会增加肾脏血管收缩张力,使得患者出现肾脏灌注减少和肾小球滤过率下降。一项Meta分析显示,在使用cAmB的患者中,肾损伤的发生率为33.8%[6],主要表现为患者血尿素氮和血肌酐的明显升高。
此外,研究指出,cAmB制剂在进入血液后,分离出的AMB通过单核细胞中CD14相关toll样受体2(TLR2)微生物模式识别受体,导致促炎细胞因子TNF-α、IL-1β、IL-6、IL-8和前列腺素E2的表达和释放,从而诱发寒战、发热、恶心等输液相关反应[5]。临床试验也显示,使用cAMB的患者中出现输注相关不良反应的概率超60%[7-8]。
由于cAmB临床不良反应发生率高,研究人员因此致力于AMB各种剂型的研究。两性霉素B脂质复合物(ABLC)、胶质分散体(ABCD)与脂质体(L-AmB)等剂型陆续问世,均在提高药物溶解性、生物利用度以及降低毒性方面得到了一定的改善。
二、 新型两性霉素B剂型在结构、性质与功能方面的差异
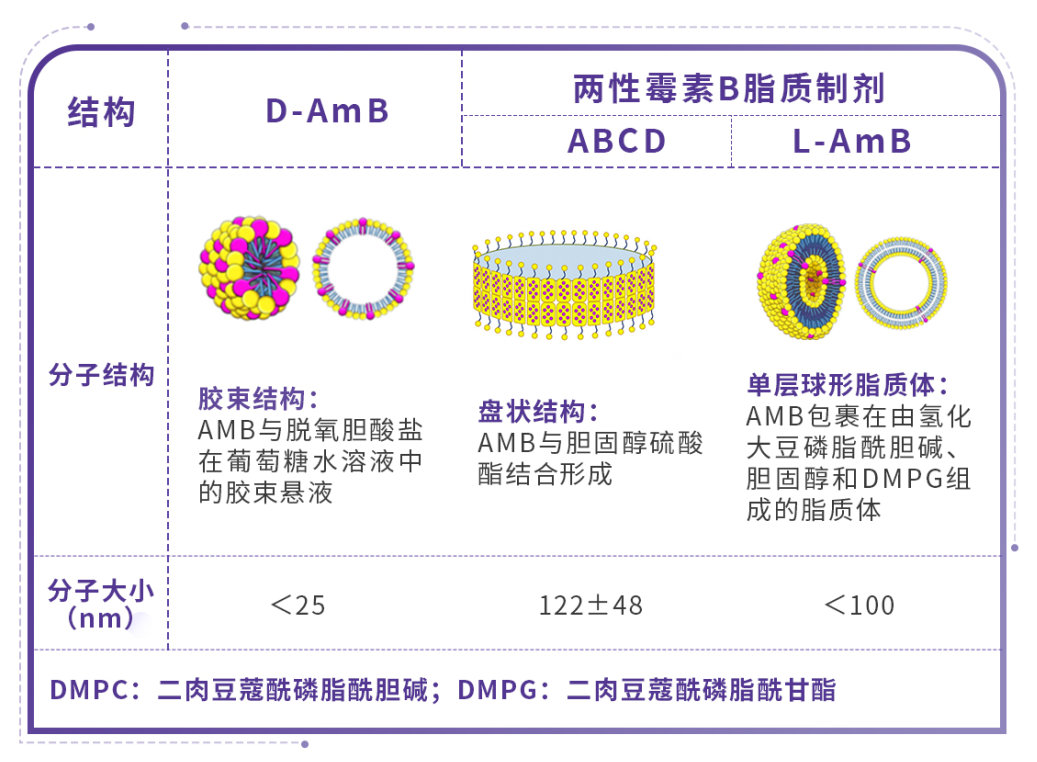
尽管同为两性霉素B类药物,但不同剂型的微观结构(表)仍可能带来疗效上的差异。不同微观结构对其在体内分布和清除的药代动力学过程产生了一定的影响[9]。D-AmB起效的方式是AMB与脱氧胆酸盐形成胶束悬浮液[10],进行静脉给药;ABCD是由AMB和胆固醇硫酸酯钠(SCS)组成比例约1:1的盘状复合物,AMB通过范德华力、静电力和氢键力等非共价键相互作用穿插在SCS中[11];L-AmB则是由外部的氢化大豆磷脂酰胆碱、胆固醇和二硬脂酰磷脂酰甘油组成的球形单层脂质体,并将AMB分子牢固地包裹在脂质体结构中[10,12]。
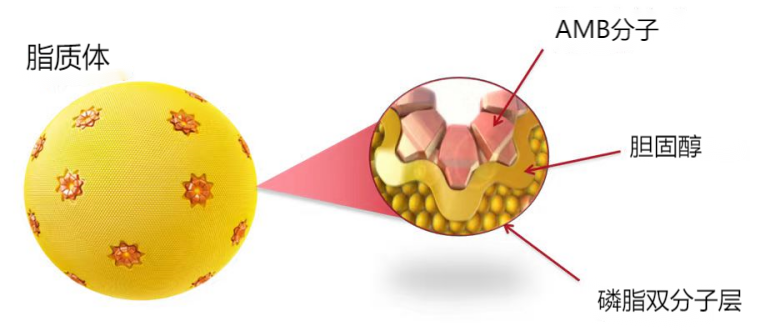
图1 L-AmB结构图
表1 不同两性霉素B剂型的结构差异[10,11]
而当L-AmB进入体内后,脂质体优先在富含网状内皮细胞的器官中分布,AMB被限制在脂质体内不进行肾小球滤过[5],且由于L-AmB在血浆中解离出的游离AMB药物浓度<1 μg/ml[13],大幅降低了肾损害发生率;AMB肾毒性的发生是在AMB分子与LDL结合后导致,而在L-AmB中,AMB被包裹在脂质体中,更倾向与HDL受体优先结合,而肾脏中HDL受体较少,所以L-AmB与LDL结合比例大大降低[14-15]。不仅如此,L-AmB中AMB分子与真菌细胞膜中麦角固醇的结合力要比与脂质体双分子层胆固醇的结合力高10倍[16],这也在一定程度上减少了药物与人体细胞中的胆固醇结合而产生的毒性[9]。
此前一项发布于NEJM[17]的随机、双盲、多中心试验研究,纳入687例患者,比较cAmB(344例)与L-AmB(343例)作为经验性抗真菌治疗的疗效差异,发现两组在综合治疗成功率相似的前提下,使用L-AmB治疗患者出现突破性真菌感染的几率显著低于使用cAmB治疗的患者(11例/3.2% vs 27例/7.8%,P=0.009);其次L-AmB组肾损伤发生率也显著低于cAmB组(19% vs 34%,P<0.001)。因此研究结果表明,在接受经验性抗真菌治疗过程中,L-AmB与cAmB相比,突破性真菌感染发生率与肾损伤发生率均更低。
值得一提的是,ABCD虽在肾毒性方面低于cAmB[18],但基于与cAmB相似的炎症机制,ABCD进入血液后,游离的AMB较多,会导致TLR2型应答增强[19],因此输液反应发生率高[20]。而L-AmB分子较小且外部的二硬脂酰磷脂酰甘油成分带有负电荷[14],单核吞噬细胞对其吞噬相对较少,以TLR4型应答为主,并促进抗炎细胞因子IL-10的生成和释放,产生抗炎作用[21]。
为给L-AmB的工业生产提供预配方,Rogayeh Seify等人[22]制备了大小范围在150.3~263.9nm且聚合物分散度指数<0.32的脂质体。这类载体物理化学性质稳定,常规条件下药物能以线性规律进行降解,并且将亲水或疏水的药物分别包裹在水核与脂质双分子层中,有效降低了进入体内后游离药物的比例。此外,通过1,2-二硬脂酰磷脂酰甘油(DSPG)使得该脂质体表面具有更高的负电荷,有效减少单核吞噬细胞系统的吞噬[23]。
该研究成果不仅降低了成本,省去了工业工厂主要关注的蒸发步骤,在最终产品中没有溶剂残留,并且对生物系统无害,是既环保又经济的制备方法。
三、 小结
cAmB抗菌谱广,耐药率低,但在安全性方面劣势明显,L-AmB在保留其优点的同时,在肾脏毒性等安全性方面有显著改善[23],已被《2016年美国感染病学会(IDSA)临床实践指南:念珠菌病的管理》[24]、《2017 欧洲临床微生物与感染性疾病学会(ESCMID)/欧洲医学真菌学联盟(ECMM)/欧洲呼吸学会(ERS)指南:曲霉菌病的诊断和管理》[25]等国内外多个指南列为抗真菌一线治疗用药。提升对L-AmB临床应用的系统性认识有助于优化血液病患者中IFD治疗策略,降低患者死亡风险。
参考文献
[1] 中国医师协会血液科医师分会,中国侵袭性真菌感染工作组.血液病/恶性肿瘤患者侵袭性真菌病的诊断标准与治疗原则(第六次修订版)[J].中华内科杂志, 2020, 59(10):754-763.
[2] 宋明华.临床应用的两性霉素B活性及毒性研究进展[J].生物化工,2022,8(05):166-169.
[3] Faustino C, Pinheiro L. Lipid Systems for the Delivery of Amphotericin B in Antifungal Therapy. Pharmaceutics. 2020;12(1):29. Published 2020 Jan 1.
[4] Baginski M, Resat H, Borowski E. Comparative molecular dynamics simulations of amphotericin B-cholesterol/ergosterol membrane channels. Biochim Biophys Acta. 2002;1567(1-2):63-78.
[5] Adler-Moore J, Lewis RE, Brüggemann RJM, Rijnders BJA, Groll AH, Walsh TJ. Preclinical Safety, Tolerability, Pharmacokinetics, Pharmacodynamics, and Antifungal Activity of Liposomal Amphotericin B. Clin Infect Dis. 2019;68(Suppl 4):S244-S259.
[6] Steimbach LM, Tonin FS, Virtuoso S, et al. Efficacy and safety of amphotericin B lipid-based formulations-A systematic review and meta-analysis. Mycoses. 2017;60(3):146-154.
[7] Johnson PC, Wheat LJ, Cloud GA, et al. Safety and efficacy of liposomal amphotericin B compared with conventional amphotericin B for induction therapy of histoplasmosis in patients with AIDS. Ann Intern Med. 2002;137(2):105-109.
[8] Hamill RJ, Sobel JD, El-Sadr W, et al. Comparison of 2 doses of liposomal amphotericin B and conventional amphotericin B deoxycholate for treatment of AIDS-associated acute cryptococcal meningitis: a randomized, double-blind clinical trial of efficacy and safety. Clin Infect Dis. 2010;51(2):225-232.
[9] 孔旭东,王晓星,陈玥等.两性霉素B不同制剂的药学特性和临床应用[J].临床药物治疗杂志,2022,20(07):7-12.
[10] Cavassin FB, Baú-Carneiro JL, Vilas-Boas RR, Queiroz-Telles F. Sixty years of Amphotericin B: An Overview of the Main Antifungal Agent Used to Treat Invasive Fungal Infections. Infect Dis Ther. 2021;10(1):115-147.
[11] Guo LS. Amphotericin B colloidal dispersion: an improved antifungal therapy. Adv Drug Deliv Rev. 2001;47(2-3):149-163.
[12] Adler-Moore JP, Proffitt RT. Amphotericin B lipid preparations: what are the differences?. Clin Microbiol Infect. 2008;14 Suppl 4:25-36.
[13] Bekersky I, Fielding RM, Dressler DE, Lee JW, Buell DN, Walsh TJ. Plasma protein binding of amphotericin B and pharmacokinetics of bound versus unbound amphotericin B after administration of intravenous liposomal amphotericin B (AmBisome) and amphotericin B deoxycholate. Antimicrob Agents Chemother. 2002;46(3):834-840.
[14] Stone NR, Bicanic T, Salim R, Hope W. Liposomal Amphotericin B (AmBisome(?)): A Review of the Pharmacokinetics, Pharmacodynamics, Clinical Experience and Future Directions. Drugs. 2016;76(4):485-500.
[15] Working PK. Amphotericin B colloidal dispersion. Pre-clinical review. Chemotherapy. 1999;45 Suppl 1:15-26.
[16] Walker L, Sood P, Lenardon MD, Milne G, Olson J, Jensen G, Wolf J, Casadevall A, Adler-Moore J, Gow NAR. The Viscoelastic Properties of the Fungal Cell Wall Allow Traffic of AmBisome as Intact Liposome Vesicles. mBio. 2018 Feb 6;9(1):e02383-17.
[17] Walsh TJ, Finberg RW, Arndt C, et al. Liposomal amphotericin B for empirical therapy in patients with persistent fever and neutropenia. National Institute of Allergy and Infectious Diseases Mycoses Study Group. N Engl J Med. 1999;340(10):764-771.
[18] Groll AH, Müller FM, Piscitelli SC, Walsh TJ. Lipid formulations of amphotericin B: clinical perspectives for the management of invasive fungal infections in children with cancer. Klin Padiatr. 1998 Jul-Aug;210(4):264-73.
[19] Simitsopoulou M, Roilides E, Dotis J, et al. Differential expression of cytokines and chemokines in human monocytes induced by lipid formulations of amphotericin B. Antimicrob Agents Chemother. 2005;49(4):1397-1403.
[20] Hamill RJ. Amphotericin B formulations: a comparative review of efficacy and toxicity. Drugs. 2013 Jun;73(9):919-34.
[21] Bellocchio S, Gaziano R, Bozza S, et al. Liposomal amphotericin B activates antifungal resistance with reduced toxicity by diverting Toll-like receptor signalling from TLR-2 to TLR-4. J Antimicrob Chemother. 2005;55(2):214-222.
[22] Seify R, Zahednezhad F, Zakeri-Milani P, Valizadeh H. Amphotericin B liposomal formulation: applicable preparation methods, challenges, and tips. Drug Dev Ind Pharm. 2023;49(5):367-376.
[23] 高雯慧,王丽宁,王苓等.两性霉素B脂质体在血液疾病患者侵袭性真菌病中应用研究进展[J].中国感染与化疗杂志,2023,23(01):111-116.
[24] Pappas PG, Kauffman CA, Andes DR, et al. Clinical Practice Guideline for the Management of Candidiasis: 2016 Update by the Infectious Diseases Society of America. Clin Infect Dis. 2016;62(4):e1-e50.
[25] Ullmann AJ, Aguado JM, Arikan-Akdagli S, et al. Diagnosis and management of Aspergillus diseases: executive summary of the 2017 ESCMID-ECMM-ERS guideline. Clin Microbiol Infect. 2018;24 Suppl 1:e1-e38.
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。

责任编辑:彭伟彬
相关搜索: 两性霉素B