- 首页 > 正文
新型抗菌药物在血液肿瘤化疗后粒缺伴发热患者MDR感染中的应用探索
杨晓珊 Yang Xiaoshan 发表时间:2024/1/8 20:46:52
编者按:血液肿瘤患者在化疗后常出现中性粒细胞缺乏(粒缺)伴发热。由于免疫功能低下,炎症相关临床症状和体征常不明显,病原菌及感染灶也不明确,发热可能是感染的唯一征象,如未及时给予恰当的抗菌药物治疗,感染相关死亡率高,特别是多重耐药(MDR)菌感染。为提高患者治疗安全及抗肿瘤化疗疗效,需要及早对患者进行个体化评估并予以恰当的经验性抗菌治疗。《感染医线》特邀上海交通大学医学院附属瑞金医院吴文教授对血液肿瘤化疗后粒缺伴发热患者的耐药菌感染现状进行分享,并结合自身临床经验分享此类患者的抗感染治疗策略。
粒缺伴发热的流行现状
中性粒细胞减少是应用化疗药物最常见的血液学不良事件和剂量限制性不良反应。化疗导致的中性粒细胞减少(CIN)是指使用骨髓抑制性化疗药物后引发外周血中性粒细胞绝对计数(ANC)的降低,即血常规ANC<2.0×109/L。CIN的谷值通常出现在化疗后第7~14天,其降低程度与患者所使用的化疗药物的种类和剂量有关,当患者采用高剂量或密集方案化疗时,患者的外周血中性粒细胞更可能出现低于正常范围的长时间谷值。
超过80%的血液肿瘤患者在≥1个疗程化疗后会出现与中性粒细胞缺乏(粒缺)有关的发热。粒缺伴发热会增加侵袭性感染的发生风险,可能会引起治疗费用的增加、抗生素的使用、住院时间的延长、化学药物的减量或延迟,严重者可导致感染性休克、脓毒症等危及生命的并发症,甚至导致患者死亡。血液肿瘤患者粒缺伴发热常有较高的死亡率,其血流感染的相关死亡率可达7.1%~42%[1]。
一项国内多中心、前瞻性研究显示,感染的发生率随粒缺持续时间的延长而升高,粒缺持续7~56天,发热的累积发生率可从60.9%攀升至99.7%[2];接受化疗的患者粒缺伴发热的累积发生率明显高于接受造血干细胞移植(HSCT)及接受抗人胸腺细胞球蛋白(ATG)治疗的患者(91.0% vs. 83.6% vs. 54.5%,P=0.006)[2]。一项国内回顾性分析显示,由于自身疾病特点以及化疗、HSCT、深静脉导管置入、化疗后骨髓抑制等因素,恶性血液病患者是发生血流感染的高危人群,发生率为11%~38%,病死率高达37.6%[3]。
在致病微生物分布方面,粒缺伴发热患者感染细菌总体以革兰阴性(G-)菌为主(44.54%)[2];在血流感染中,G-菌占比更高(81.3%)[3]。G-菌一直是临床最主要的分离菌株,而其带来的耐药问题也长期困扰着临床,尤其是近年迅速增加的碳青霉烯耐药革兰阴性菌(CRO)。中国细菌耐药监测网(CHINET)数据显示[4],我国肺炎克雷伯菌对美罗培南和亚胺培南的耐药率,即碳青霉烯耐药肺炎克雷伯菌(CRKP)检出率,已从2022年的24.2%和22.6%,上升至2023上半年的30%和29%,刷新了历史最高值。
血液肿瘤患者碳青霉烯耐药肠杆菌目细菌(CRE)感染的发生率和死亡率较其他科室更高,在血液肿瘤患者中,分离出的CRE主要为大肠埃希菌、其次为肺炎克雷伯菌,这与ICU患者中主要为肺炎克雷伯菌、其次为大肠埃希菌不同;不同的CRE菌株其碳青霉烯酶的分布也不同;而针对不同的碳青霉烯酶,抗菌药物的选择也不同[5]。因此,针对血液肿瘤患者,当患者在化疗后出现粒缺伴发热时,临床需考虑病原菌分布的特征及患者个体危险因素等,制定合理的抗感染治疗方案。
初始经验性抗菌治疗策略
既往有研究显示,经验性抗菌治疗不足、严重脓毒症或脓毒性休克是CRKP血流感染患者死亡的独立危险因素[6]。这也提示临床应及时启动恰当的抗菌治疗,以早期控制感染、减少严重感染的出现,进而降低患者死亡率。而恰当的抗菌治疗方案需要从多个维度进行个体化评估:
患者自身评估:危险分层、感染部位、脏器功能及全身状况。
细菌及耐药风险评估:既往耐药菌定植及感染情况、既往抗菌药物使用情况、本院及本科室耐药菌流行情况。
抗菌药物选择:在危险分层和耐药危险因素评估后,尽快使用抗菌药物初始经验性治疗,而不必等待微生物学的结果,选择具有杀菌活性和安全性良好的广谱抗菌药物,并需注意与治疗原发疾病的药物(化疗药物、免疫抑制剂等)之间是否存在毒副作用的叠加。对于临床表现不复杂、不确定是否存在耐药菌定植、以及既往无耐药菌感染,且本院很少发生因耐药菌导致感染的情况,那么治疗方案可以采取升阶梯策略;反之,则采取降阶梯策略。

△粒缺伴发热患者的危险分层

△粒缺伴发热患者的抗菌药物选择
既往CRE感染/定植
CRE感染的治疗选择非常有限,也是当前抗感染领域最为棘手的问题之一。对于既往有CRE感染或定植的患者,《广泛耐药革兰阴性菌感染的实验诊断、抗菌治疗及医院感染控制:中国专家共识》、《中国碳青霉烯耐药肠杆菌科细菌感染诊治与防控专家共识》及《血液肿瘤患者碳青霉烯类耐药的肠杆菌科细菌(CRE)感染的诊治与防控中国专家共识(2020年版)》均强调联合治疗是重要的治疗策略[5,7-8],其原因在于抗菌药物单药治疗的疗效不能令人满意,比如:
头孢他啶/阿维巴坦:血液肿瘤患者分离出的CRE以大肠埃希菌常见,其主要产NDM金属酶,而头孢他啶/阿维巴坦对产NDM金属酶菌株100%无效[9],这一短板在一定程度上限制了头孢他啶/阿维巴坦的应用。
多黏菌素:多黏菌素类药物治疗窗窄,与产生肾毒性浓度几乎重叠[10],同时还存在异质性耐药特点,这使得临床面临两难选择,即高剂量可能增加肾毒性风险,低剂量暴露则可能增加耐药性;此外,雾化吸入的给药方式,尚未有确切的临床获益证据,仍需更多研究探索,另外其不同黏菌素制剂的复杂剂量换算也限制了多黏菌素类药物临床应用的便捷性。
替加环素:首先,铜绿假单胞菌天然对四环素类药物耐药。其次,替加环素在血液中的浓度较低,而加大用药剂量则可能会提高凝血功能障碍、肝功能损伤、消化道副作用等不良事件发生率[11],给临床实践带来困扰;且美国FDA早在2010年即向医生发布警告,提示替加环素与其他抗菌药相比有更高的死亡风险,并在2013年将这一黑框警告信息更新至替加环素说明书[12-13]。而在制定经验性治疗方案时,抗菌药物的自身特性也是临床医生需要考虑的重要因素,替加环素的天然劣势和不良反应问题使得临床不得不谨慎考虑其应用。
在此背景下,临床可以根据国内外各个权威指南/共识考虑新型抗菌药物的应用。
依拉环素的临床应用探索
依拉环素是全球首个氟环素类抗菌药,其对四环素的核心D环进行了结构改造,包括在C7位引入氟原子,在C9位引入吡咯烷乙酰氨基,结构修饰使其药物性能获得了显著提升:

△引入氟原子可优化药物特性
抗菌谱广:可覆盖多种常见耐药菌G+(MRSA,VRE)和G-(CRAB、CRE、CRKP),还可覆盖支原体、衣原体、军团菌等非典型病原体,而且对多种耐药机制介导的MDR细菌也可以覆盖,包括产ESBL、KPC、AmpC、OXA-48、VIM、NDM、IMP等β-内酰胺酶耐药介导的肠杆菌目细菌[14-15]。
抗菌活性强:经过结构改造的依拉环素与细菌核糖体30S亚基结合位点的亲和力是四环素的14倍[16],因而具备更强抗菌活性,全球药敏数据(2017-2020)显示[17],依拉环素对肺炎克雷伯菌、肠杆菌科细菌体外抗菌活性是替加环素的2倍,对鲍曼不动杆菌体外抗菌活性是替加环素的4倍。
与其他抗菌药物联合协同无拮抗:联合药敏研究显示[18],依拉环素与多种药物联用显示出协同作用、无拮抗作用,其中依拉环素与多黏菌素B联用对CREC和CRKP协同率最高,分别达35%和30%。这一特点也与各个专家共识所强调的联合治疗相契合。
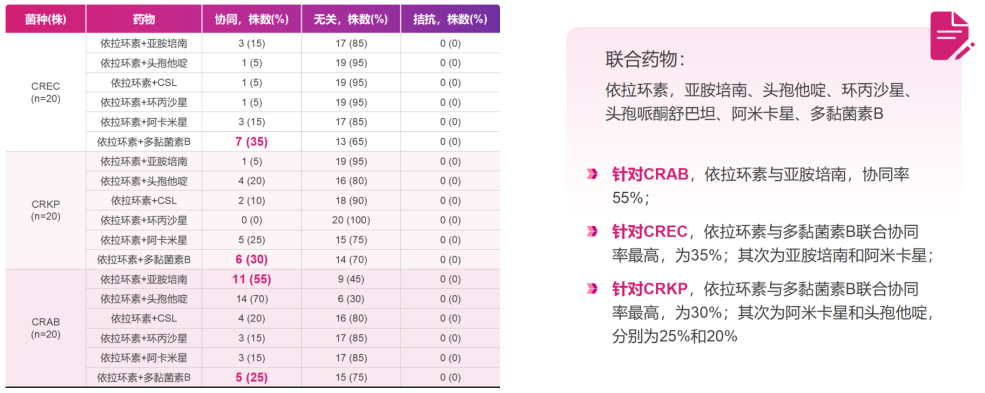
△依拉环素与多种药物联用显示出协同作用
组织和血浆浓度均较高:依拉环素在肺泡上皮衬液(ELF)、肺泡巨噬细胞(AM)和血浆中的浓度均较高,使用推荐剂量即可达到很好的疗效[fAUC/MIC≥1.87时,临床成功率为100%(E.coli)][19]。
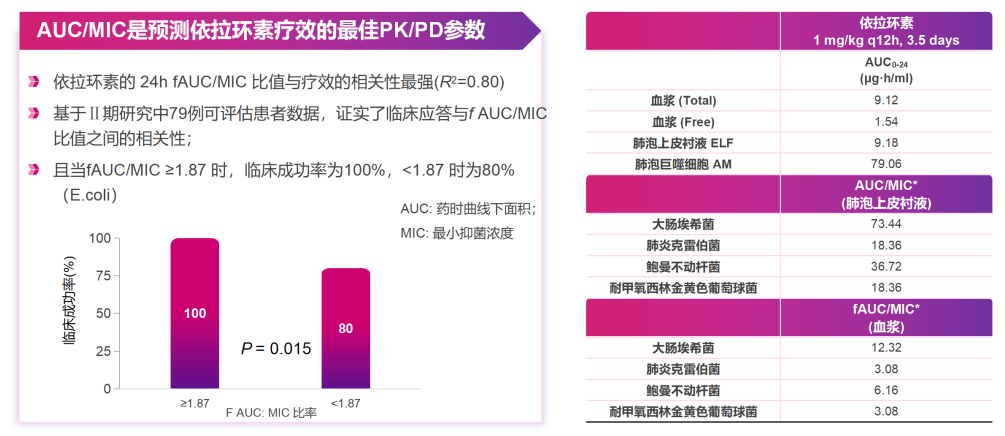
△依拉环素组织浓度高
退热快:在一项随机、双盲Ⅱ期研究中,与接受厄他培南治疗的患者相比,接受标准剂量依拉环素治疗腹腔内感染患者的中位退热时间更短(15.7 vs. 31.3 h)[20]。
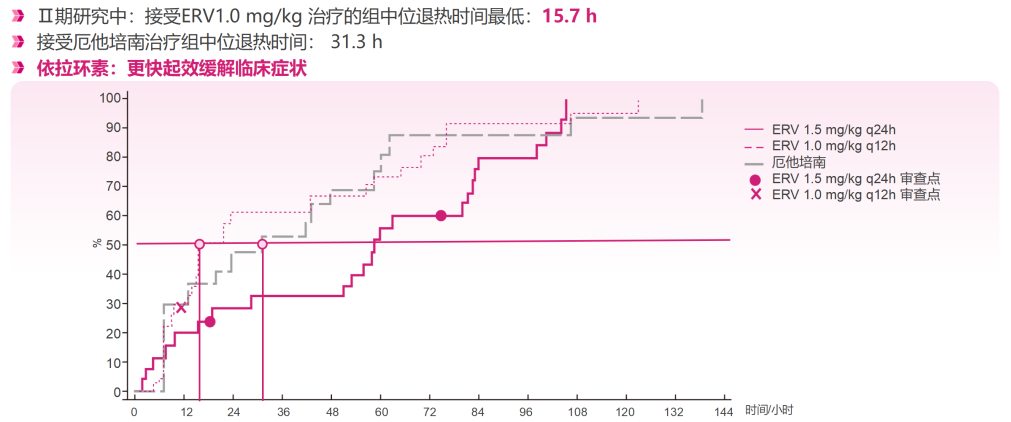
△标准剂量依拉环素治疗组中位退热时间<24h
安全性好:来自全球的多项真实世界研究将依拉环素用于肺炎、骨关节感染、皮肤软组织感染、血流感染等不同感染部位的患者,均显示良好的临床缓解率,且安全性和耐受性良好[21-25]。
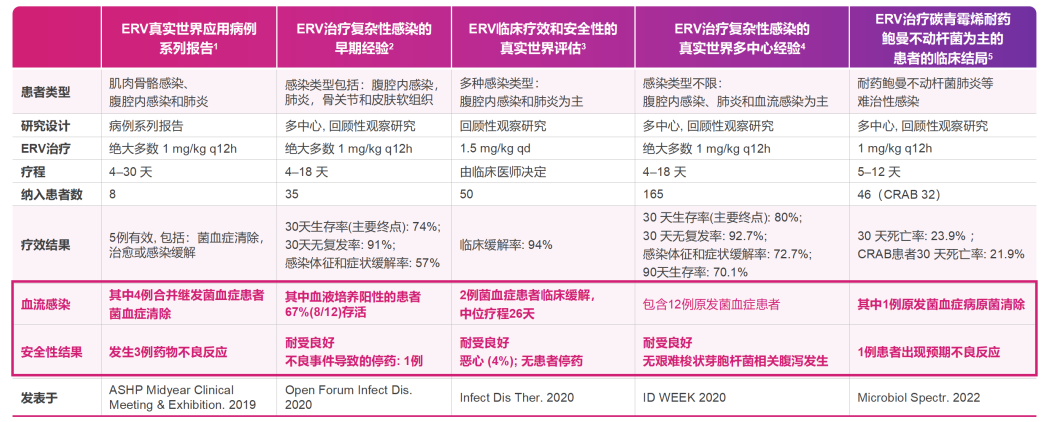
△依拉环素真实世界研究
也正是基于以上良好的药物特性以及确切的临床疗效和安全性,目前依拉环素已经获得美国感染病学会(IDSA)耐药G-菌感染治疗指南、欧洲临床微生物学和感染病学会(ECSMID)多重耐药G-菌感染指南,以及中国CRO感染诊疗及防控指南等权威指南共识推荐用于MDR细菌感染治疗[26-28]。
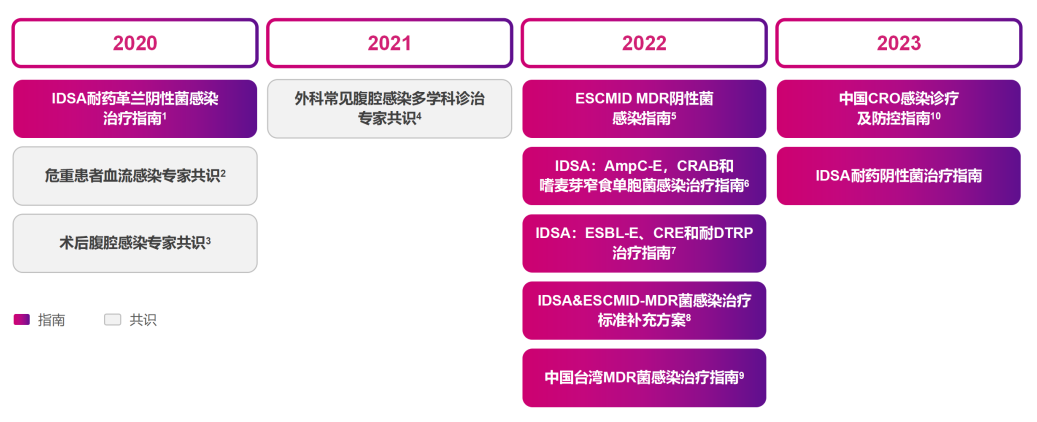
△依拉环素已被国内外多个指南/共识推荐作为MDR菌治疗方案
总结
恶性血液病患者在接受化疗后,由于持续的免疫抑制,容易发生机会性感染,尤其是由MDR细菌引起的感染。此类患者由于合并其他合并症或器官损伤,抗感染治疗难度较大,预后也相对较差。依拉环素作为一种抗菌谱广、抗菌活性强、组织浓度高、疗效和安全性好、退热迅速的新型抗菌药物,为血液肿瘤化疗后粒缺伴发热患者的初始经验性治疗提供了更多选择。
参考文献
[1] 中华医学会血液学分会,中国医师协会血液科医师分会.中国中性粒细胞缺乏伴发热患者抗菌药物临床应用指南(2020年版)[J].中华血液学杂志,2020,41(12):969-978.DOI:10.3760/cma.j.issn.0253-2727.2020.12.001.
[2] 闫晨华,徐婷,郑晓云,孙洁,段显林,谷景立,赵川莉,朱骏,吴玉红.中国血液病患者中性粒细胞缺乏伴发热的多中心、前瞻性流行病学研究[J].中华血液学杂志,2016,37(3):177-182.DOI:10.3760/cma.j.issn.0253-2727.2016.03.001.
[3] 蔡林静,魏小磊,魏永强,郭绪涛,江雪杰,张钰,余国攀,戴敏,叶洁瑜,周红升,徐丹,黄芬,范志平,许娜,史鹏程,宣丽,冯茹,刘晓力,孙竞,刘启发.恶性血液病患者血流感染的病原菌分布及耐药性单中心回顾性分析[J].中华血液学杂志,2023,44(6):479-483.DOI:10.3760/cma.j.issn.0253-2727.2023.06.006.
[4] CHINET 2023年上半年细菌耐药监测结果(2023年1-6月). www.chinets.com
[5] 中华医学会血液学分会,中国医师协会血液科医师分会.血液肿瘤患者碳青霉烯类耐药的肠杆菌科细菌(CRE)感染的诊治与防控中国专家共识(2020年版)[J].中华血液学杂志,2020,41(11):881-889.DOI:10.3760/cma.j.issn.0253-2727.2020.11.001.
[6] Chen J, Ma H, Huang X, et al. Risk factors and mortality of carbapenem-resistant Klebsiella pneumoniae bloodstream infection in a tertiary-care hospital in China: an eight-year retrospective study. Antimicrob Resist Infect Control. 2022;11(1):161. Published 2022 Dec 19. doi:10.1186/s13756-022-01204-w
[7] 王明贵.广泛耐药革兰阴性菌感染的实验诊断、抗菌治疗及医院感染控制:中国专家共识[J].中国感染与化疗杂志,2017,17(1):82-93.DOI:10.16718/j.1009-7708.2017.01.015.
[8] 中国碳青霉烯耐药肠杆菌科细菌感染诊治与防控专家共识编写组,中国医药教育协会感染疾病专业委员会,中华医学会细菌感染与耐药防控专业委员会.中国碳青霉烯耐药肠杆菌科细菌感染诊治与防控专家共识[J].中华医学杂志,2021,101(36):2850-2860.DOI:10.3760/cma.j.cn112137-20210219-00438.
[9] Han R, Shi Q, Wu S, et al. Dissemination of Carbapenemases (KPC, NDM, OXA-48, IMP, and VIM) Among Carbapenem-Resistant Enterobacteriaceae Isolated From Adult and Children Patients in China. Front Cell Infect Microbiol. 2020;10:314. Published 2020 Jul 3. doi:10.3389/fcimb.2020.00314
[10] 中国医药教育协会感染疾病专业委员会,中华医学会呼吸病学分会,中华医学会重症医学分会,中华医学会血液学分会,中华医学会细菌感染与耐药防治分会,中国药学会药物临床评价研究专业委员会,全球华人临床微生物与感染学会.中国多黏菌素类抗菌药物临床合理应用多学科专家共识[J].中华结核和呼吸杂志,2021,44(4):292-310.DOI:10.3760/cma.j.cn112147-20201109-01091.
[11] Shi X, Zuo C, Yu L, et al. Real-World Data of Tigecycline-Associated Drug-Induced Liver Injury Among Patients in China: A 3-year Retrospective Study as Assessed by the Updated RUCAM. Front Pharmacol. 2021;12:761167. Published 2021 Nov 2. doi:10.3389/fphar.2021.761167
[12] Tasina E, Haidich AB, Kokkali S, Arvanitidou M. Efficacy and safety of tigecycline for the treatment of infectious diseases: a meta-analysis. Lancet Infect Dis. 2011;11(11):834-844. doi:10.1016/S1473-3099(11)70177-3
[13] FDA Drug Safety Communication: FDA warns of increased risk of death with IV antibacterial Tygacil (tigecycline) and approves new Boxed Warning.https://www.fda.gov/drugs/drug-safety-and-availability/fda-drug-safety-communication-fda-warns-increased-risk-death-iv-antibacterial-tygacil-tigecycline
[14] Alosaimy S, Abdul-Mutakabbir JC, Kebriaei R, Jorgensen SCJ, Rybak MJ. Evaluation of Eravacycline: A Novel Fluorocycline. Pharmacotherapy. 2020;40(3):221-238.
[15] The Sanford guide to antimicrobial therapy (52th 2022 Edition).
[16] Grossman TH, Starosta AL, Fyfe C, et al. Target- and resistance-based mechanistic studies with TP-434, a novel fluorocycline antibiotic [published correction appears in Antimicrob Agents Chemother. 2015 Sep;59(9):5870]. Antimicrob Agents Chemother. 2012;56(5):2559-2564. doi:10.1128/AAC.06187-11
[17] Hawser S, Kothari N, Monti F, Morrissey I, Siegert S, Hodges T. In vitro activity of eravacycline and comparators against Gram-negative and Gram-positive bacterial isolates collected from patients globally between 2017 and 2020. J Glob Antimicrob Resist. 2023;33:304-320. doi:10.1016/j.jgar.2023.04.017
[18] Li Y, Cui L, Xue F, Wang Q, Zheng B. Synergism of eravacycline combined with other antimicrobial agents against carbapenem-resistant Enterobacteriaceae and Acinetobacter baumannii. J Glob Antimicrob Resist. 2022;30:56-59. doi:10.1016/j.jgar.2022.05.020
[19] Bhavnani SM, Rubino CM, Hammel JP, et al. Pharmacokinetic-Pharmacodynamic (PK-PD) and Dose Selection Analyses for Eravacycline Using Phase 2 Data from Patients with Community-Acquired Complicated Intra-Abdominal Infections (cIAI).
[20] Solomkin JS, Ramesh MK, Cesnauskas G, et al. Phase 2, randomized, double-blind study of the efficacy and safety of two dose regimens of eravacycline versus ertapenem for adult community-acquired complicated intra-abdominal infections. Antimicrob Agents Chemother. 2014;58(4):1847-1854. doi:10.1128/AAC.01614-13
[21] Shayna Lunsted, et al. Real-World Useof Eravacvcline: A Case Series. ASHP 2019, Poster.
[22] Alosaimy S, Molina KC, Claeys KC, et al. Early Experience With Eravacycline for Complicated Infections. Open Forum Infect Dis. 2020;7(5):ofaa071. Published 2020 Mar 2. doi:10.1093/ofid/ofaa071
[23] Van Hise N, Petrak RM, Skorodin NC, et al. A Real-World Assessment of Clinical Outcomes and Safety of Eravacycline: A Novel Fluorocycline. Infect Dis Ther. 2020;9(4):1017-1028. doi:10.1007/s40121-020-00351-0
[24] Alosaimy S, et al. Real-world Multi-center experience with ERV for complicated infection. ID WEEK 2020, Poster.
[25] Alosaimy S, Morrisette T, Lagnf AM, et al. Clinical Outcomes of Eravacycline in Patients Treated Predominately for Carbapenem-Resistant Acinetobacter baumannii. Microbiol Spectr. 2022;10(5):e0047922. doi:10.1128/spectrum.00479-22
[26] Tamma PD, Aitken SL, Bonomo RA, Mathers AJ, van Duin D, Clancy CJ. Infectious Diseases Society of America 2023 Guidance on the Treatment of Antimicrobial Resistant Gram-Negative Infections [published online ahead of print, 2023 Jul 18]. Clin Infect Dis. 2023;ciad428. doi:10.1093/cid/ciad428
[27] Lawandi A, et al. IDSA guidance and ESCMID guidelines: complementary approaches toward a care standard for MDR Gram-negative infections. Clin Microbiol Infect. 2022 Apr;28(4):465-469.
[28] Zeng M, Xia J, Zong Z, et al. Guidelines for the diagnosis, treatment, prevention and control of infections caused by carbapenem-resistant gram-negative bacilli. J Microbiol Immunol Infect. 2023;56(4):653-671. doi:10.1016/j.jmii.2023.01.017

吴文 主任医师
上海交通大学医学院附属瑞金医院
血液转化医学病区主任
国家食品药品监督总局药品审评中心专家组成员
上海市社会医疗机构协会肿瘤学分会副会长
上海市社会医疗机构协会血液肿瘤多学科专委会主任委员
中华医学会上海血液学分会MPN协作组副组长
“Frontiers of Medicine”, “Oncotarget”, “中华临床医师杂志” 等杂志审稿专家
作为高级研究人员及主要参加者,承担了国家“九五”攻关、 科技部973计划、国家自然科学基金、国家教委、卫生部科研基金、浦江人才计划等十余项科研课题,并取得了上海市科技进步一等奖、教育部科学进步二等奖和卫生部科技进步三等奖。
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
.png)
责任编辑:彭伟彬
相关搜索: MDR感染