- 首页 > 正文
胡晓慧教授:力挽狂澜,两性霉素B脂质体挽救性治疗血液病患者侵袭性真菌病,为血液病患者带来曙光
感染医线 发表时间:2024/10/13 19:38:53
*备注:本研究中治疗方案药物为注射用两性霉素B脂质体(国药准字HJ20233123,规格50mg/支)
01
疗效为先,L-AmB治疗既往抗真菌治疗不耐受或无效的IFD患者有效率近80%
研究回顾性收集了既往抗真菌治疗失败后2023年6月至2023年12月期间于苏州弘慈血液病医院血液科接受L-AmB治疗的80例血液病患者资料。患者中位年龄49岁,65.0%为男性。基础疾病包括急性髓系白血病(45.0%)、急性淋巴细胞白血病(12.5%)、再生障碍性贫血(8.8%)、骨髓增生异常综合征(18.8%)等。既往使用的抗真菌治疗药物包括三唑类(57.5%)、棘白菌素类卡泊芬净(12.5%)、多烯类普通两性霉素B(10.0%)以及这些药物联用。分别有20.0%和80.0%的患者换用L-AmB前对既往抗真菌治疗药物不耐受和无效。最主要的感染部位为肺部(88.8%),其次是血流(11.2%)。最主要的感染病原菌为曲霉属(22.5%),其次为念珠菌属(21.3%)、毛霉属(6.3%)。本次IFD诊断分层为拟诊IFD28例、临床诊断IFD43例、确诊IFD9例。
疗效分析显示,L-AmB挽救性治疗临床有效率高。中位每日剂量3mg·kg-1·d-1,中位用药疗程14d,中位累积剂量1800mg。使用L-AmB后,中位退热时间为3d,肺部病灶缩小的中位时间为17.5d。根据疗效评价标准:L-AmB治疗后26.2%患者获得完全缓解,51.3%患者获得部分缓解,10.0%稳定,7.5%进展,5.0%死亡,临床有效率为77.5%。
单因素分析显示,患者年龄<60岁、血液疾病处于缓解状态,L-AmB每日剂量≥3.0mg·kg-1·d-1、用药疗程≥14d,L-AmB治疗IFD临床疗效更好(均P<0.05)。此外,L-AmB单药治疗对比L-AmB联合治疗IFD感染的完全缓解率(33.3%对19.5%,P=0.283)及部分缓解率(41.0%对61.0%,P=0.309)差异无统计学意义,同时临床中位退热时间[3(2.0,6.5)d对3(2.8,4.0)d,P=0.606]及肺部感染病灶中位缩小时间[23(11,30)d对14(9,24)d,P=0.203]差异无统计学意义。
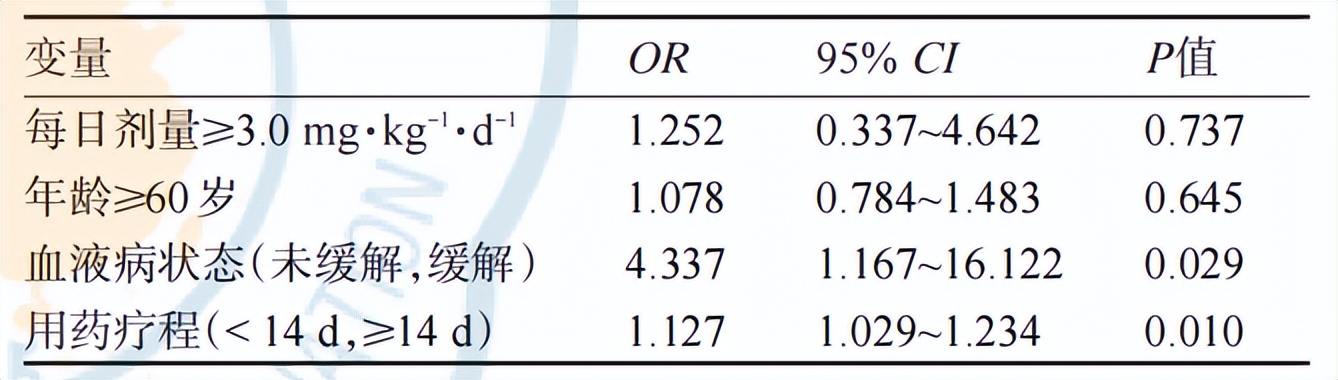
将单因素分析中P<0.05的变量纳入多因素Logistic回归,结果显示:L-AmB用药疗程(OR=1.127,95% CI 1.029~1.234,P=0.010)以及L-AmB治疗IFD时疾病是否缓解(OR=4.337,CI 1.167~16.122,P=0.029)是影响L-AmB疗效的独立因素,而L-AmB的每日剂量及患者年龄并不影响L-AmB疗效(表1)。
表1.多因素Logistic回归分析影响两性霉素B脂质体(L-AmB)治疗侵袭性真菌病(IFD)疗效的因素
02
兼顾安全,L-AmB在血液病患者中输液相关反应少,肾毒性低
本研究中,L-AmB不良反应发生率低,安全性良好。相关输液反应包括发热和寒战(5.0%)。3.8%出现恶心及呕吐,经对症处理后症状迅速消失。低钾血症发生率为28.8%,主要为1~2级,经加强补钾治疗后血钾恢复正常。发生顽固性低钾血症的比例仅为2.5%,其中1例为3级低钾血症,经停止用药3d及补钾治疗后血钾恢复正常;另1例为4级低钾血症,经停止用药 5d及补钾治疗后血钾恢复正常。低镁血症的发生率为20.0%,主要为1~2级,经补镁治疗后恢复正常。肾毒性发生率为11.3%,主要为1~2级(表2)。经L-AmB减量、加强保肾治疗5~7d后肾功能恢复正常。
表2.两性霉素B脂质体(L-AmB)治疗侵袭性真菌病(IFD)的肾毒性发生情况


胡晓慧教授点评
IFD是血液病患者感染性致死病因之一,有效且安全的抗真菌治疗对改善患者预后至关重要。抗真菌治疗面临唑类耐药及药物相互作用、棘白菌素类疗效局限且耐药增加的难题。两性霉素B(AmB)虽广谱、低耐药,但传统剂型毒副作用大,临床应用受限。L-AmB(两性霉素B脂质体)有望成为解决当前困境的“钥匙”。
本研究聚焦于L-AmB(两性霉素B脂质体)对既往抗真菌治疗不耐受或无效的血液病患者IFD临床疗效与安全性。血液病患者由于免疫系统受损,常面临IFD的高风险,这类感染往往病情复杂,治疗难度大,因此探索更为有效且安全的治疗方案显得尤为重要。研究结果显示,L-AmB在中国这一特定患者群体中展现出了很好的抗真菌疗效,用药疗程及疾病缓解状态是影响其临床疗效的独立因素,不良反应发生率低,在安全性方面具有优势,可为临床合理使用L-AmB提供参考。
疗效方面,本研究中,L-AmB挽救性治疗临床有效率为77.5%。L-AmB在血液病患者IFD中的疗效与剂量、年龄与疾病状态等多因素有关。本研究单因素分析显示,患者年龄<60岁、血液疾病处于缓解状态,L-AmB每日剂量≥3.0mg·kg-1·d-1、用药疗程≥14d,L-AmB治疗IFD临床疗效更好。
安全性方面,本研究中,L-AmB整体安全性良好。肾毒性多为轻度,且其发生与L-AmB的剂量及用药疗程无明显相关性。低钾血症主要为1~2级。关于肾毒性,由于血液病患者在治疗过程中时常需要联合用药,可能增加使用L-AmB的肾毒性风险。另外,血液肿瘤及其相关并发症、放化疗均可导致肾损伤[9],因此治疗过程中如果出现肾功能异常,需综合考虑原因,不仅仅是L-AmB所致药物性肾损伤。低血钾是两性霉素B(AmB)最常见的不良反应之一。本研究中,低钾血症的发生可能与HSCT早期患者常合并存在黏膜炎,进食量少,存在钾摄入量不足有关,经相应处理后血钾恢复正常。
展望未来,为了更全面地验证L-AmB在血液病患者IFD治疗中的疗效与安全性,以及进一步探索其最佳使用策略,需要开展多中心随机对照研究来进一步评估,为临床医生在制定抗真菌治疗方案时提供更加科学、有力的依据。同时,随着研究的深入,我们期待获得更多L-AmB在中国临床应用的数据,探索与其他抗真菌药物的联合应用策略,从而为血液病患者提供更加个性化、精准的治疗方案。
参考文献
[1]. Sun Y, Meng F, Han M, et al. Epidemiology, management, and outcome of invasive fungal disease in patients undergoing hematopoietic stem cell transplantation in China: a multicenter prospective observational study[J]. Biol Blood Marrow Transplant,2015, 21(6):1117-1126. DOI: 10.1016/j.bbmt.2015.03.018.
[2]. Logan A, Wolfe A and Williamson JC. Antifungal Resistance and the Role of New Therapeutic Agents[J]. Curr Infect Dis Rep . 2022;24(9):105-116.
[3]. Stewart AG and Paterson DL. How urgent is the need for new antifungals?[J]. Expert Opin Pharmacother . 2021 Oct;22(14):1857-1870
[4]. Hoenigl M, Sprute R, Egger M et al. The Antifungal Pipeline: Fosmanogepix, Ibrexafungerp, Olorofm, Opelconazole, and Rezafungin[J]. Drugs. 2021; 81:1703–1729.
[5]. Nivoix Y, Ledoux MP, Herbrecht R. Antifungal Therapy: New and Evolving Therapies[J]. Semin Respir Crit Care Med. 2020 Feb;41(1):158-174.
[6]. Nett JE and Andes DR. Antifungal Agents: Spectrum of Activity, Pharmacology, and Clinical Indications[J]. Infect Dis Clin North Am. 2016 Mar;30(1):51-83.
[7]. 中华血液学杂志2024年7月第45卷第7期 Chin J Hematol,July 2024,Vol. 45,No. 7
[8]. Bridoux F, Cockwell P, Glezerman I, et al. Kidney injury and disease in patients with haematological malignancies[J]. Nat Rev Nephrol, 2021, 17(6):386- 401. DOI: 10.1038/s41581- 021-00405-7.
[9]. TsotF,et al Haematologica 2017 Mar,102 3 433-444
[10]. Maertens Jet al.Bone Marrow Transplant.2011 May.40(5):709-18
[11]. 中国医师协会血液科医师分会中国侵袭性真菌感染工作组.中华内科杂志,2020:59(10)754-763
[12]. Tissot F et al. Haematologica. 2017 Mar;102(3):433-444
[13]. Patterson TF et al. Clinical Infectious Diseases® 2016;63(4):e1–60
Cornely OA et al. Lancet Infect Dis 2019;10.1016/S1473-3099(19)30312-3

胡晓慧 教授
苏州大学附属第一医院
血液科,主任医师,医学博士,硕士生导师
中华医学会血液学分会中西整合医学学组委员
中国抗癌协会肿瘤营养专业委员会营养预防学组委员
江苏省研究型医院学会造血干细胞移植和免疫治疗分会委员
苏州市医学会血液病学分会老年血液病学组成员
苏州市抗癌协会血液肿瘤专业委员会委员
美国费城儿童医院访问学者
在国际及国内刊物发表论文多篇
参与多项国家及省级科研项目
参与多项国际及国家临床试验
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
