- 首页 > 正文
“小4”不升的潜在“元凶”:CD4自身抗体的流行率、临床特征及对免疫重建的影响
感染医线 发表时间:2024/12/27 23:41:22
编者按:免疫功能重建不全或免疫无应答是不少HIV感染者面临的治疗难题,可影响感染者预后。目前缺乏明确的免疫重建不全的解释机制和可用于指导预后或治疗的标志物。一项发表于CID杂志的研究,描述了CD4自身抗体在晚期HIV感染者中的发生率可达29%,而且自身抗体阳性的感染者表现出CD4细胞计数更低、免疫反应更差,而对自身抗体的免疫抑制干预一定程度上可以恢复CD4细胞[1]。
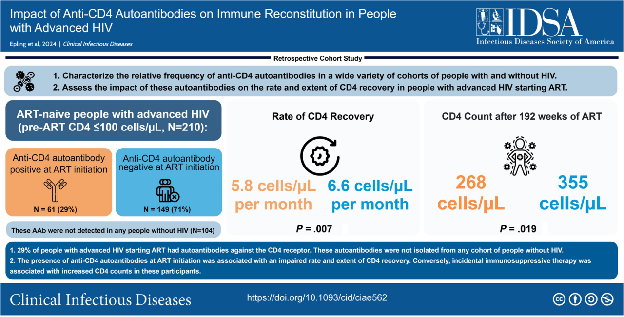
大多数HIV感染者在启动ART后2年内CD4计数可超过500个/µL,但仍有15%~30%的感染者即使在长期病毒学抑制下也表现出有限的CD4恢复,被称为免疫学无反应(INR)[2-3]。这类免疫重建不全的感染者发生机会性疾病的风险更高,预后更差[4]。
导致免疫重建不全的重要机制是CD4细胞产生减少(如例如骨髓产生淋巴前体细胞减少、胸腺输出减少和淋巴组织纤维化)或破坏增加(如持续的免疫激活)。已有研究在HIV感染者中鉴定出针对CD4 T细胞的抗CD4 T细胞自身抗体[5-7],是作为导致CD4淋巴细胞减少症的可能机制。但有关抗CD4自身抗体在HIV感染者中的相对流行率,以及它们在启动ART时的免疫学或临床意义,仍然不完全清楚。
本研究使用流体相荧光素免疫沉淀系统(LIPS)免疫测定法评估了ART未治疗的晚期HIV患者中抗CD4自身抗体的血清流行率。并旨在于前瞻性临床环境中评估启动ART时的抗CD4自身抗体是否会影响这一人群中CD4重建的速率和INR的风险。此外,研究还评估了偶然的免疫调节干预措施是否可以通过干扰抗CD4自身抗体的产生和/或生物学效应来影响CD4重建。
不同人群的抗CD4自身抗体发生率
对未经抗反转录病毒治疗(ART)的晚期HIV感染者(n = 210)、CD4计数大于200个/µL且未接受ART治疗的HIV感染者(n = 38)、长期非进展者(LTNPs,n = 55)、特发性CD4淋巴细胞减少症(ICL,n = 70)、自身免疫性淋巴细胞增生综合征(ALPS,n = 23)患者以及健康对照组(HCs,n = 11)的血浆进行抗CD4自身抗体检测,以评估不同人群中的抗CD4自身抗体水平。
如图1所示,所有健康对照组、ALPS患者和ICL患者的血清学检测结果均为阴性。
相比之下,未经ART治疗的晚期HIV感染者(29%)、CD4计数大于200细胞/µL的HIV感染者(26%)、LTNPs(9%)有不同程度的抗CD4自身抗体阳性。
与病毒载量未被抑制的HIV感染者相比,LTNPs中抗CD4自身抗体的患病率显著降低(P=0.0016)。所有5名抗CD4自身抗体阳性的LTNP参与者在所有测量时间点上都有超过1次可量化的病毒血症(中位随访时间9.76年),而45名阴性参与者中只有25名有这种情况。在一组有(n = 9)和没有(n = 40)抗CD4自身抗体的HIV感染者中,通过荧光素酶免疫沉淀系统(LIPS)对其他T细胞膜潜在免疫靶点和自身抗原进行的额外检测,没有发现对这些蛋白有统计学意义的血清阳性。
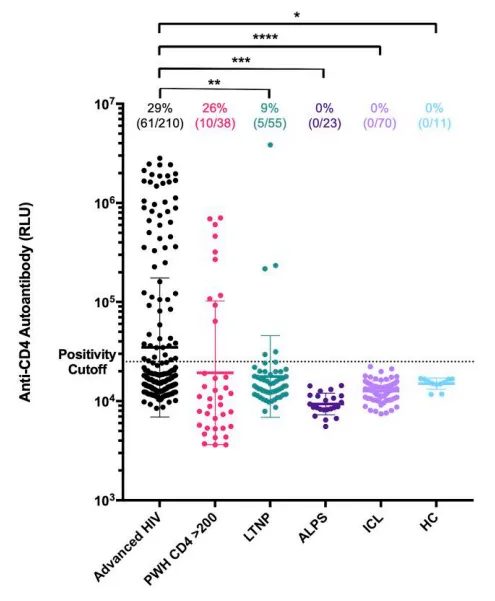
图1.不同人群的抗CD4自身抗体发生率
自身抗体与CD4受体的结合域
为了进一步验证并反映与CD4受体细胞外结构域的免疫反应性,研究者们使用LIPS免疫检测法,对一组选定的CD4血清阳性和血清阴性的HIV感染者(PWH)样本进行了不同CD4受体蛋白片段的检测(图2)。
众所周知,CD4受体最接近的D1结构域能够结合HIV-1的gp120和主要组织相容性复合体II类(MHC-II),但这一区域并未显示出自身抗体的免疫反应性(图2B)。相比之下,包含完整D3-D4结构域的CD4蛋白片段显示出了高抗体结合性(图2C)。对自身抗体免疫反应性的进一步描绘显示,单独的D3结构域结合性较弱(图2D),而包含部分D3和完整D4结构域的片段则具有强烈的结合活性(图2E)。总体而言,这些结果表明D3-D4结构域包含了抗CD4自身抗体产生和结合的表位。
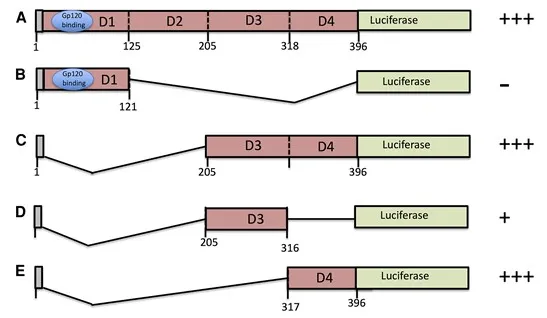
图2.自身抗体与CD4受体不同区域结合的图谱
晚期HIV队列的临床特征
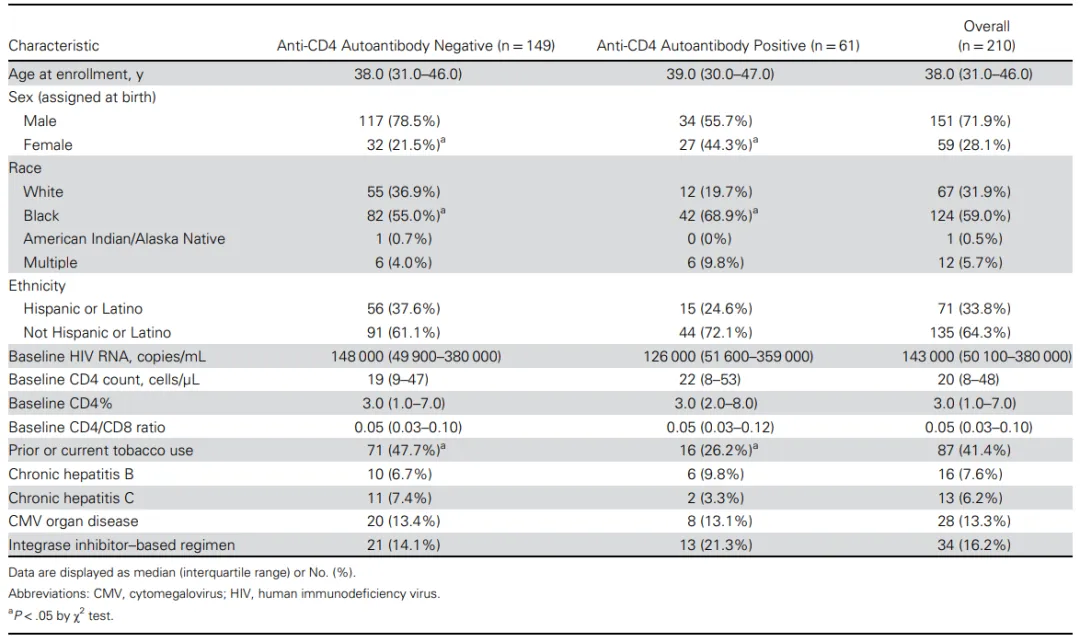
随后对210名未经ART的晚期HIV感染者进行了分析,以评估在ART开始时抗CD4自身抗体对随后免疫重建的影响(图3)。表1显示了抗CD4自身抗体阴性(n = 149)和阳性(n = 61)感染者的临床特征。两组感染者的基线临床特征大体相似;然而,携带抗CD4自身抗体的患者更可能是女性(优势比[OR],4.1;卡方检验P < 0.0001)、黑人(OR,2.3;P = .019),并且没有吸烟史(P = 0.005)。这些参与者在ART开始后的中位随访时间为192周。
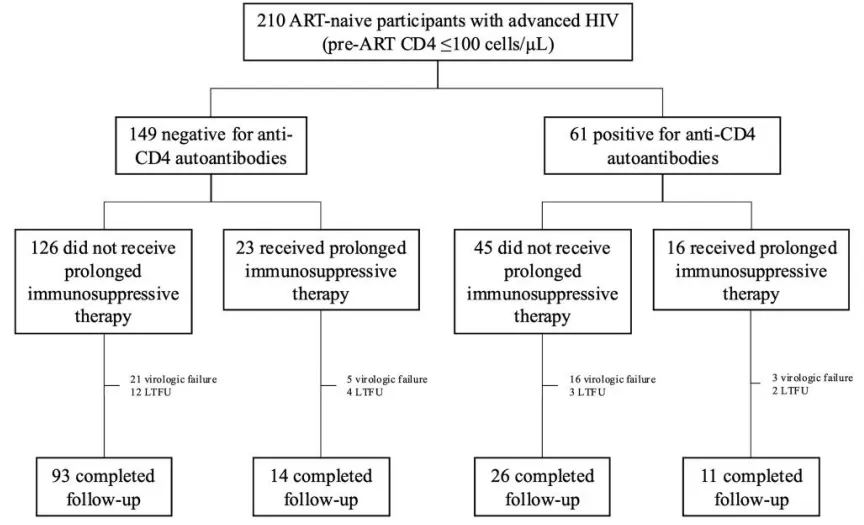
图3. 基是否存在抗CD4自身抗体以及是否接受长期免疫抑制治疗的CONSORT流程图
表1.不同抗CD4自身抗体状态的晚期HIV感染者的临床特征
自身抗体对CD4 T细胞重建的影响
作者首先比较了血清阳性与血清阴性参与者的CD4恢复速度和程度。在一项针对CD4计数重复测量的混合效应模型中,与血清阴性的HIV感染者相比,在启动ART时携带抗CD4自身抗体的HIV感染者的CD4恢复速度显著较慢(5.8 vs 6.6 个/µL/月;P = 0.0068);值得注意的是,在0至12周之间恢复速度没有差异,但在12周后恢复速度有显著差异(4.8 vs 5.8 个/µL/月,P = 0.0036)。
在96周时,自身抗体血清阳性感染者的中位CD4计数较低(217 vs 291 个/µL);在单变量分析中这没有统计学意义(P = 0.084),但在调整性别、基线CD4计数、HIV病毒载量和年龄后具有显著性(P = 0.029)(图4A)。在176周和192周时,血清阳性参与者的中位CD4计数显著较低(192周时中位CD4计数:血清阴性为355 vs血清阳性为268 个/µL;在单变量分析中P = 0.018,在多变量模型中P = 0.037)。
在整个随访期间,血清阳性感染者产生免疫反应(CD4 >350 个/µL)的可能性降低,但差异没有显著统计学意义(HR 0.61;P = 0.10)(图4B)。
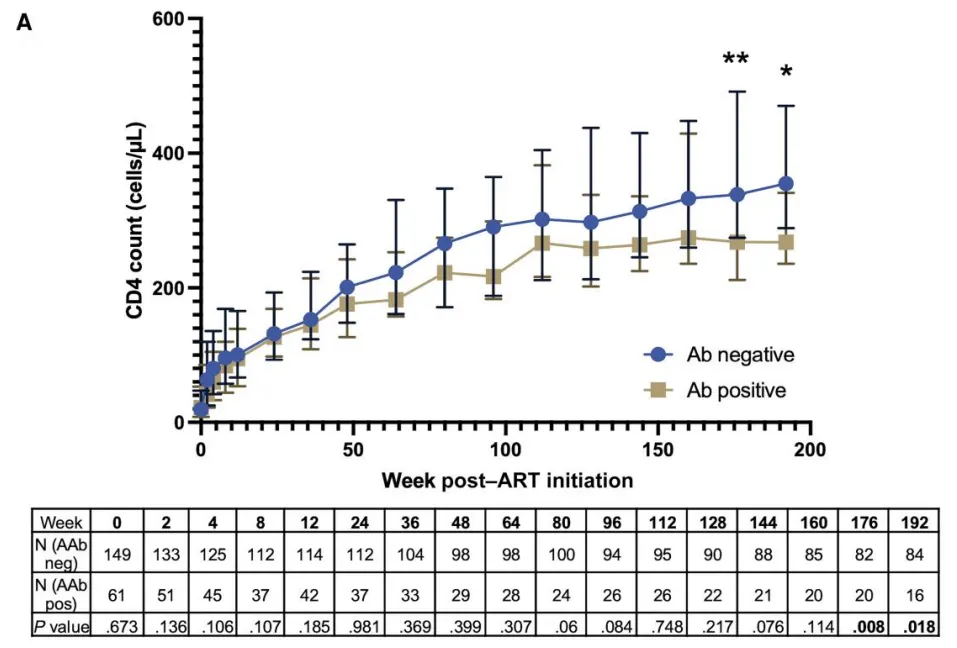
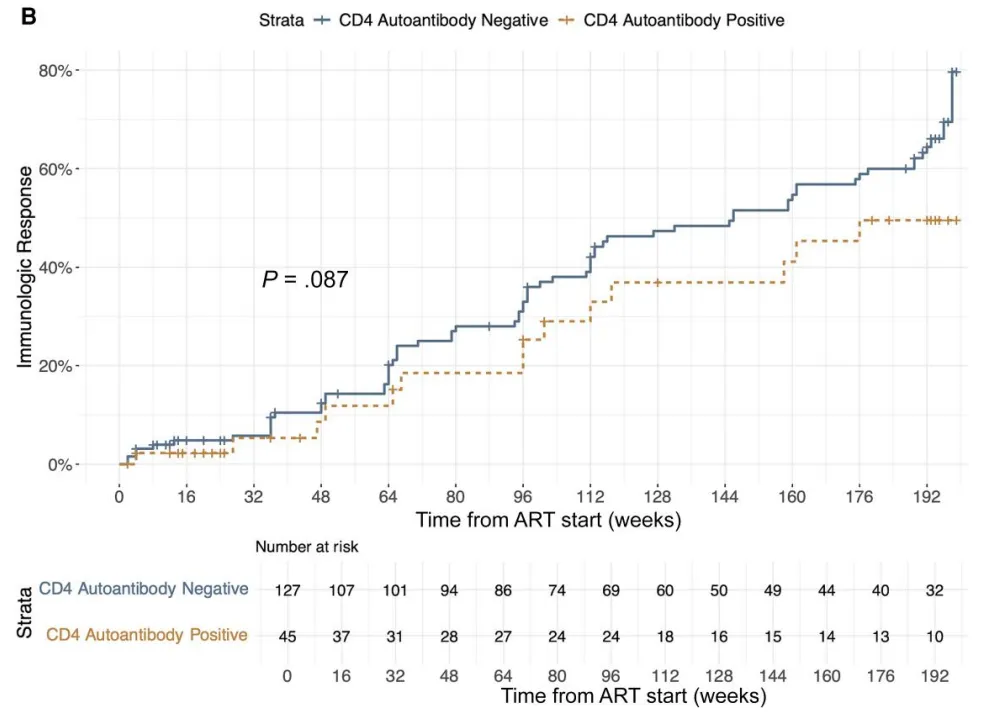
图4.自身抗体或阴性感染者的CD4细胞计数变化(A)及达到免疫反应所需时间(B)
免疫抑制对血清阳性感染者的影响
作者随后评估了偶然的、临床指示的免疫抑制对61名在启动ART时具有抗CD4自身抗体的感染者CD4重建的影响。接受长期免疫抑制治疗的患者基线CD4计数略高,但这一差异在统计学上并不显著(P = 0.059)。其他基线特征相似。最常见的免疫抑制治疗是皮质类固醇(38%),这通常是用于免疫重建炎症综合征(IRIS)的治疗。
在免疫抑制期间,血清阳性感染者的CD4恢复率显著更高(9.8 vs 17.0 个/µL/月,P = 0.0019)。在完成长期免疫抑制治疗后,CD4恢复率的显著增加持续存在(P < 0.0001;补充图6)。值得注意的是,在这些参与者接受免疫抑制治疗之前,CD4恢复率没有差异(P = 0.31)。接受长期免疫抑制的血清阳性感染者在第96周的中位数CD4计数更高(316 vs 217个/µL),但在单变量(P = 0.064)或多变量(P = 0.42)分析中这一差异并不具有统计学意义(图5A);然而,从第128周到第192周,CD4计数显著更高。接受长期免疫抑制治疗的血清阳性感染者在第192周的中位数CD4计数为551 个/µL,而未接受治疗的参与者为268 个/µL(在单变量分析中P < .001,在多变量模型中P = 0.019);即使排除了患有IRIS的患者,这种差异仍然存在(P = 0.021)。
免疫抑制能够增加感染者免疫反应(HR 2.11),通过log-rank检验显著(P = 0.02),但在多变量模型中不显著(P = 0.083)(图5B)。IRIS本身与这些参与者的CD4恢复没有差异,而在血清阴性感染者中,长期免疫抑制与任何时间点的CD4计数差异或CD4恢复率无关(P = 0.27)。
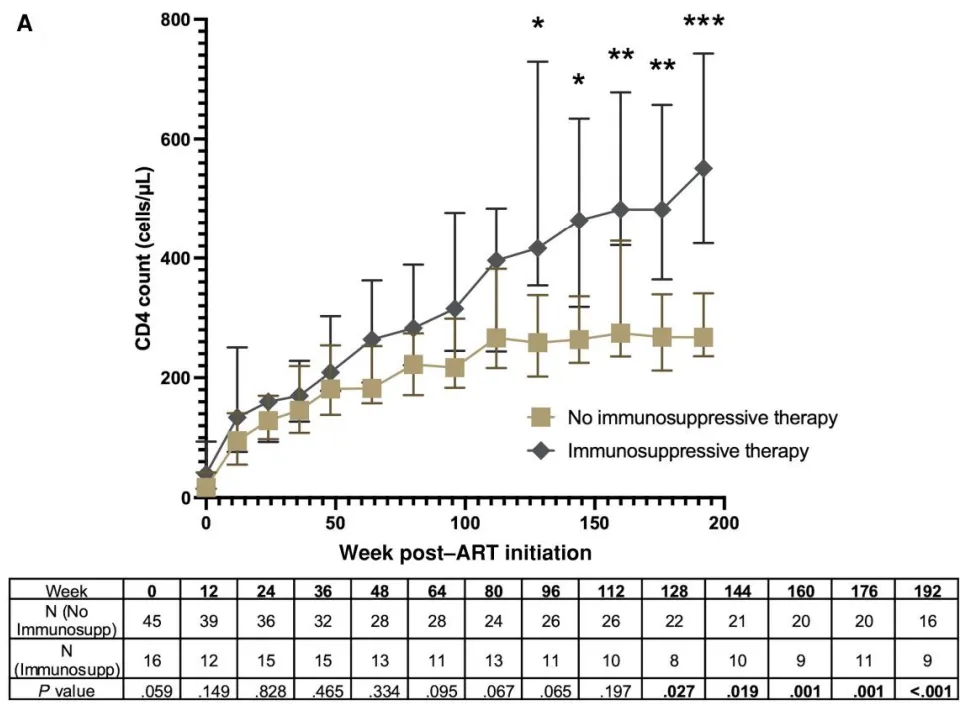
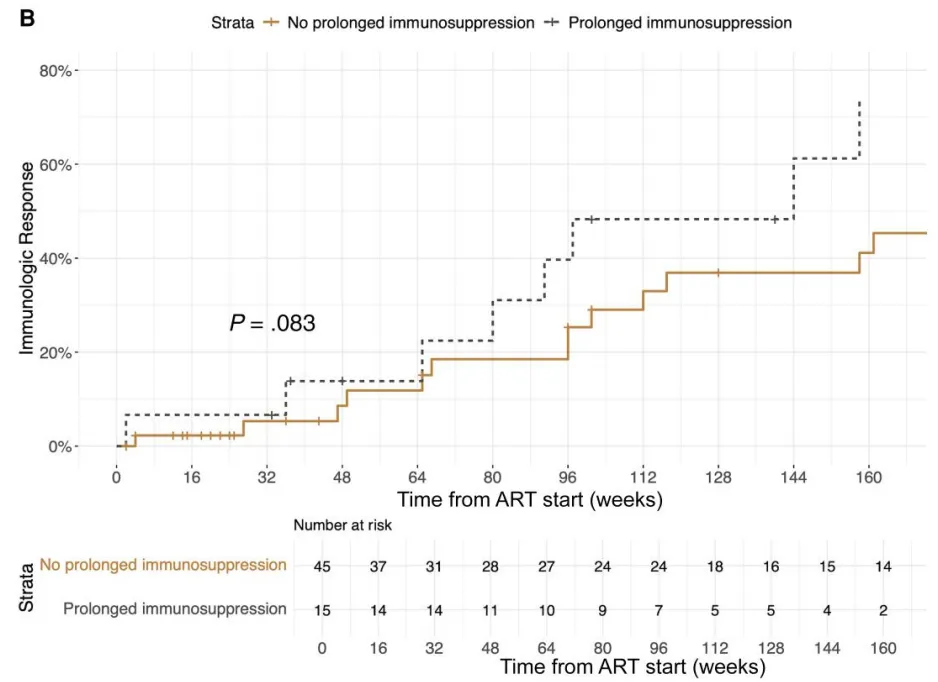
图5.根据是否接受免疫抑制治疗,抗CD4自身抗体感染者的CD4计数变化(A)和免疫反应时间(B)
抗CD4自身抗体可以转阴或转阳吗?
在27名参与者中纵向测量了抗CD4自身抗体。所有基线
总之,这项研究发现在启动ART的晚期HIV感染者中,携带抗CD4自身抗体与CD4细胞恢复速率和程度的降低之间存在关联,这种关联可发生于持续长达192周的ART期间。这些发现对于理解ART后CD4恢复受损的病理生理学以及潜在的治疗靶点具有重要意义。有必要进行更大规模队列的研究来验证这些发现,以及进一步理解这些自身抗体在CD4恢复和健康中的发生发展和下游效应。
参考文献
[1]中华医学会感染病学分会艾滋病丙肝学组,李太生.艾滋病免疫重建不全临床诊疗专家共识(2023版)[J].传染病信息,2023,36(6):481-491.DOI:10.3969/j.issn.1007-8134.2023.06.001.
[2]Yang X, Su B, Zhang X, Liu Y, Wu H, Zhang T. Incomplete immune reconstitution in HIV/AIDS patients on antiretroviral therapy: challenges of immunological non-responders. J Leukoc Biol 2020; 107:597–612.
[3]Mutoh Y, Nishijima T, Inaba Y, et al. Incomplete recovery of CD4 cell count, CD4 percentage, and CD4/CD8 ratio in patients with human immunodeficiency virus infection and suppressed viremia during long-term antiretroviral therapy. Clin Infect Dis 2018; 67:927–33.
[4]Gazzola L, Tincati C, Bellistri GM, Monforte Ad, Marchetti G. The absence of CD4+ T cell count recovery despite receipt of virologically suppressive highly active antiretroviral therapy: clinical risk, immunological gaps, and therapeutic options. Clin Infect Dis 2009; 48:328–37.
[5]Seidel MG. Autoimmune and other cytopenias in primary immunodeficiencies: pathomechanisms, novel differential diagnoses, and treatment. Blood 2014; 124:2337–44.
[6]Henriksson G, Manthorpe R, Bredberg A. Antibodies to CD4 in primary Sjogren's syndrome. Rheumatology (Oxford) 2000; 39:142–7.
[7]Perez-Diez A, Wong CS, Liu X, et al. Prevalence and pathogenicity of autoantibodies in patients with idiopathic CD4 lymphopenia. J Clin Invest 2020; 130:5326–37.