- 首页 > 正文
CROI 2024丨B/F/TAF转换治疗在预存耐药突变者的纵向分析及老年HIV感染者的疗效和安全性
任珈墨(Jiamo Ren ) 发表时间:2024/3/25 19:10:27
编者按:B/F/TAF(比克替拉韦/恩曲他滨/丙酚替诺福韦)是已经在国内外上市应用的高效、安全的最小单片口服复方制剂(FDC),且耐药屏障较高。近年来,有越来越多的循证医学证据支持该方案的临床应用在广泛人群中的应用,包括作为快速启动ART的一线优选方案、用于HIV/HBV共感染患者等。在近日举行的第三十一届反转录病毒和机会性感染大会(CROI 2024)上,一项研究公布了B/F/TAF转换治疗队列中预先存在耐药相关突变(RAMs)的HIV感染者的纵向分析数据,揭示了预存RAMs对B/F/TAF转换治疗的影响。此外,还有一项随机对照研究探讨了B/F/TAF转换治疗在老年HIV感染者中的疗效和安全性。上述两项研究成果为B/F/TAF的临床实践拓展带来了更多的指导。
预存RAMs 的HIV感染者B/F/TAF转换治疗的的纵向分析数据[1]
众所周知,预先存在HIV耐药会影响抗反转录病毒治疗(ART)的疗效[2-4]。既往研究表明,在接受ART的HIV感染者中,即使病毒载量达到检测不到水平,也可能存在RAMs [5]。另一项研究显示,具有RAM的HIV-1变体可以在病毒库中持续存在,被HIV-1变体潜伏感染的记忆 CD4+T细胞库会根据刺激(包括细胞因子和抗原暴露)进行调节,表现在RAMs的检测结果可能存在波动性(取决于病毒拷贝数是否高于检测阈值)[6]。
该项研究回顾性纳入B/F/TAF 转换研究队列(4449、4030、4580研究[5-7])中242例已获得病毒学抑制≥3-6个月的HIV感染者,其中包括既往无病毒学失败者(4030、4580研究,n=207)和基线HIV-1 RNA> 400 copies/mL者(4449研究,n=35),通过比较受试者在既往和/或基线时的纵向基因检测(≥2次HIV-1 RNA或前病毒HIV-1 DNA基因检测)报告,以调查RAMs的持久性。受试者的临床及人口统计学特征如表1所示,平均年龄52(39-61)岁,男性占76%,HIV-1 RNA< 50 copies/mL者占99%,平均CD4细胞计数644(IQR:468-871)个/μL,HIV-1基因型B占90%。
表1. 研究受试者的基线临床及人口统计学特征
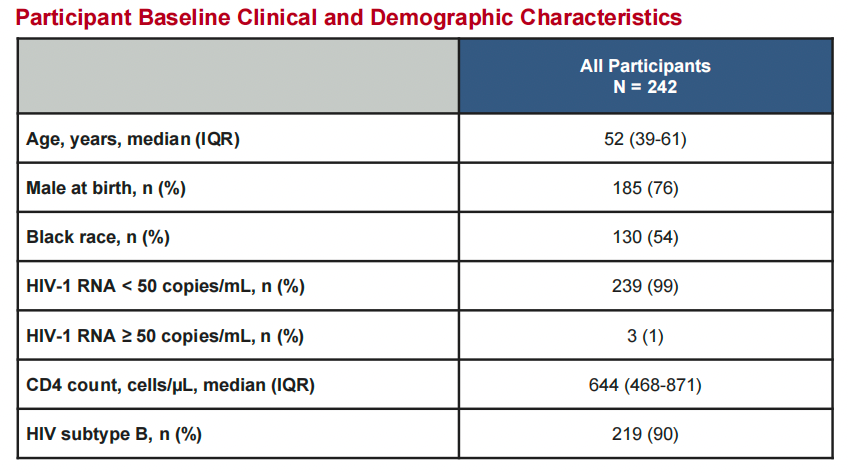
结果,收集到在B/F/TAF 转换治疗前具有2次基因检测报告的受试者223例,共分析了262个RAMs,其中103个RAMs(39.3%)的检测率为100%;159个RAMs(60.7%)的检测率为50%。101个 RAMs(63.5%)在第2个时间点检测到,58个RAMs(36.5%)在第1个时间点检测到。这些数据表明在该项研究的时间范围内,60.7%的RAMs检测呈现出了波动性,RAM被检测到的频率在大多数情况下没有减少。
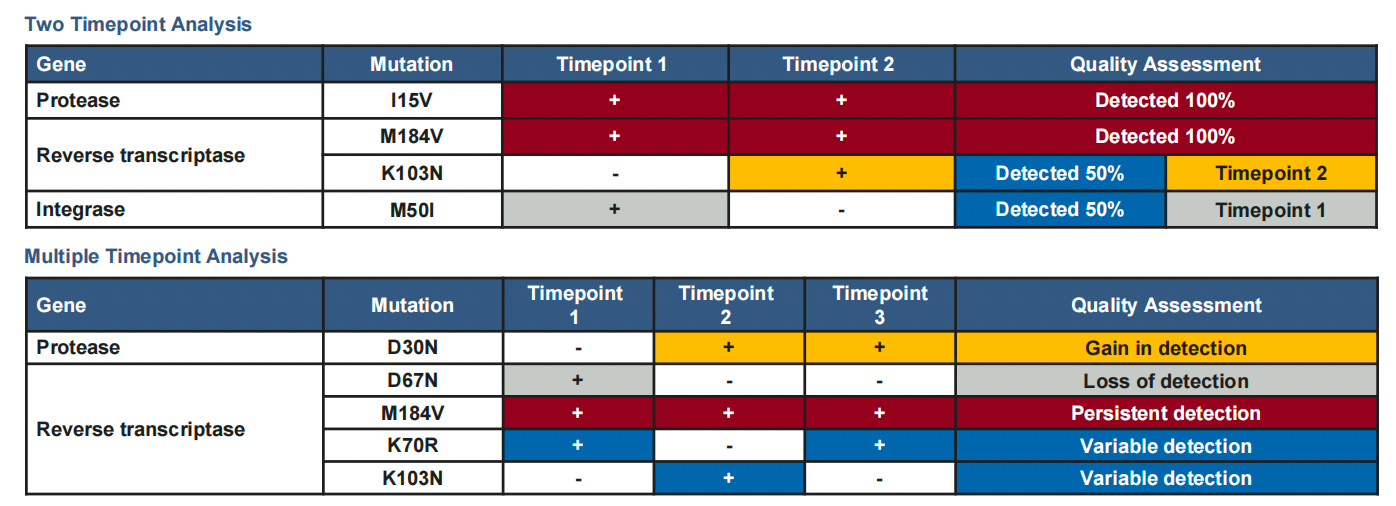
图1. 主要RAMs检测结果分析举例
有26例受试者具有>2次基因检测报告,分析了64个RAMs,结果如图2所示。其中检测结果具有波动性者(having variable detection)占45.3%(29/64);检测结果数增加(gain in detection)者占26.6%(17/64);持续检测到的(persistent detection)占18.8%(12/64,例如M184V);检测消失者(loss of detection)占9.4%(6/64)。
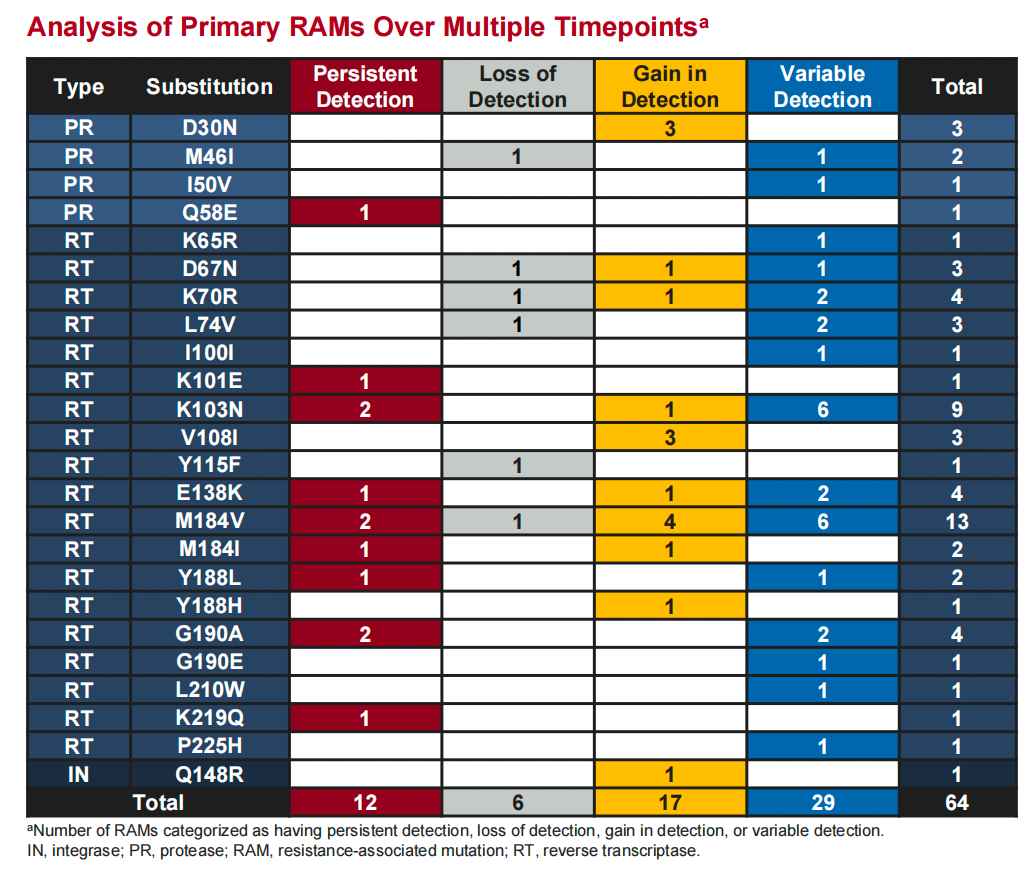
图2. HIV感染者主要RAMs分析(多个时间点的分析)
M184V/I是最普遍的一种核苷类反转录酶抑制剂(NRTIs)RAM。该项研究结果显示,M184V/I在两个时间点的分析中,31%在第2个时间点未检测到;在多个时间点的报告中,7%检测消失,40%的结果具有波动性。而在所有考察的RAMs中,分别有60.7%和45.3%的RAMs在两个时间点和多个时间点的检测结果具有波动性。
这项研究结果进一步证实,RAMs的纵向检测结果存在很大的波动性,在某一时间点RAMs检测报告为阴性的患者并不意味着不存在RAMs,只是由于HIV潜在宿主的动态性质(可能正在衰变或处于增殖)而没有检测到。
总而言之,该项研究结果提示我们综合考虑HIV感染者既往治疗史和耐药检测结果的必要性,应尽量选择高耐药屏障的抗病毒治疗药物以实现最佳的治疗管理。
老年HIV感染者B/F/TAF转换治疗的随机试验:第48周结果[8]
老年HIV感染者的转换治疗影响因素颇为复杂,包括老年人的免疫和生理状态、可能合并复杂的基础疾病、治疗药物间的相互作用(DDI)等。既往针对1844、1878、4030、4449研究的汇总分析显示,在年龄≥65岁、已实现病毒学抑制的老年人中,B/F/TAF转换治疗的48周病毒学抑制率(HIV-RNA<50 copied/mL)达92%,这些患者基线合并糖尿病、高血压、心血管疾病、血脂异常等复杂疾病[9];此外,真实世界研究显示老年HIV感染者转换为B/F/TAF,在维持病毒学抑制前提下可降低DDI风险[10]。
本次CROI大会报道的B/F/TAF-elderly研究,是一项在肯尼亚两个中心开展的开放标签、随机对照、非劣效性临床试验。入组患者为HIV-1阳性老年人(≥60岁),在入组前至少12周接受任何一线方案,HIV RNA<50 copies/mL,并按1:1随机分配至B/F/TAF组或维持既往ARV方案组(CAR组)。主要终点是第48周时,意向治疗暴露人群中HIV-1 RNA≥50 copies/mL的患者比例,以及从基线到第48周腰椎骨密度(BMD)的平均百分比变化。该试验将持续随访至第96周。
在2022年2月至5月期间,共有520名受试者随机接受治疗(两组各260名)。其中,296名受试者参加了BMD监测(B/F/TAF组143名,CAR组153名)。受试者平均年龄64岁(60-80岁),267名(51%)为女性,两组间基线特征平衡。基线时,495名(95%)受试者既往接受了含替诺福韦酯(TDF)的治疗方案,177名(60%)受试者患有骨质疏松症。
在第48周,B/F/TAF组中5/260名受试者(1.9%)、CAR组中有7/260名受试者(2.7%)的HIV-1 RNA≥50 copies/mL,符合非劣效性标准(图3)。方案定义的病毒学失败的受试者均未达到≥500 copies/mL的耐药检测阈值。
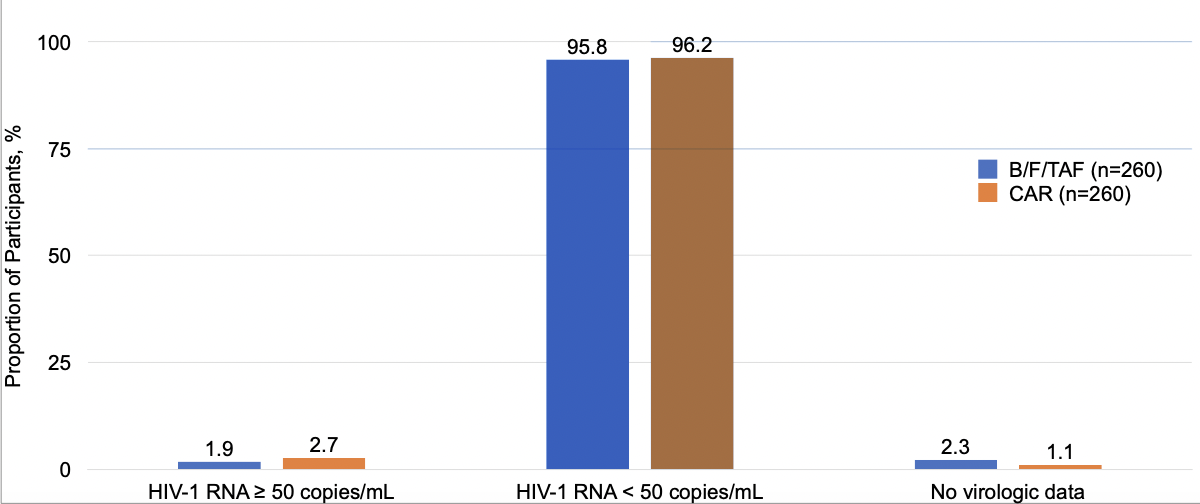
图3. 两组患者病毒学抑制率变化
腰椎BMD的平均百分比变化在B/F/TAF组为+2.17%,在CAR组为+0.61%(P=0.014,图4)。3级或4级不良事件(AE)不常见(B/F/TAF组为3.1%,CAR组为2.3%),无治疗相关的严重AE。在B/F/TAF组和CAR组中,分别有1名(0.4%)和15名(5.8%,均因肾功能下降)受试者因任何不良事件而停用研究药物。
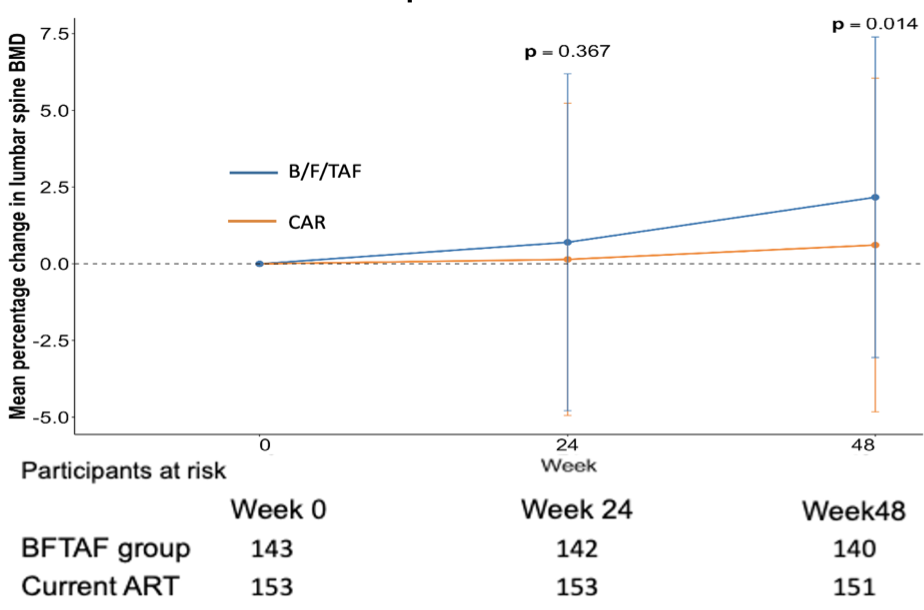
图4. 两组患者腰椎BMD变化
这项随机对照研究的样本量较大,60%的患者基线存在骨质疏松,经过B/F/TAF转换治疗后仍可维持较高的病毒学抑制率,B/F/TAF在改善患者BMD和安全性方面的优势表现突出,腰椎BMD的提升显著高于CAR方案,导致停药的肾功能下降不良事件也显著低于CAR方案。这项研究为B/F/TAF在老年人转换治疗方面提供了高质量的循证医学证据,支持其在老年人HIV感染者中的推广应用。
参考文献
1. Michelle L D'Antoni, et al. Longitudinal Analysis of Preexisting Resistance-Associated Mutations Prior to B/F/TAF Switch. CROI 2024;Abstract 695.
2. https://gskpro.com/content/dam/global/hcpportal/en_US/Prescribing_Information/Cabenuva/pdf/CABENUVA-PI-PIL-IFU2-IFU3.PDF (accessed January 31, 2024).
3. Santoro MM, et al. Virological efficacy of switch to DTG plus 3TC in a retrospective observational cohort of suppressed HIV-1 patients with or without past M184V: the LAMRES study. J Glob Antimicrob Resist. 2022 Dec;31:52-62.
4. Santoro MM, et al. Impact of M184V on the Virological Efficacy of Switch to 3TC/DTG in Real Life. CROI 2021;Abstract 429.
5. Brooks K, et al. HIV-1 variants are archived throughout infection and persist in the reservoir. PLoS Pathog. 2020 Jun 3;16(6):e1008378.
6. Cohn LB, et al. The Biology of the HIV-1 Latent Reservoir and Implications for Cure Strategies. Cell Host Microbe. 2020 Apr 8;27(4):519-530.
7. Hagins D, et al. BRAAVE2020 Investigators. Switching to bictegravir/emtricitabine/tenofovir alafenamide in black Americans with HIV-1: a randomized phase 3b, multicenter, open-label study. J Acquir Immune Defic Syndr 2021; 88:86–95.
8. Sax PE, et al. Switching to bictegravir, emtricitabine, and tenofovir alafenamide in virologically suppressed adults with Human Immunodeficiency Virus. Clin Infect Dis 2020; 73:e485–e493.
9. Molina JM, et al. Switching to fixed-dose bictegravir, emtricitabine, and tenofovir alafenamide from dolutegravir plus abacavir and lamivudine in virologically suppressed adults with HIV-1: 48?week results of a randomised, double-blind, multicentre, active-controlled, phase 3, noninferiority trial. Lancet HIV 2018; 5:e357–e365.
10. Loice A. Ombajo, et al.A Randomized Trial Switching Adults ≥ 60 Years Old From First-Line ART to B/F/TAF: Week 48 Results.CROI 2024;Abstract 643.
11. New Findings on Gilead’s Biktarvy? Presented at AIDS 2020: Virtual Include Positive Switch Data in Older Adults.https://www.gilead.com/news-and-press/press-room/press-releases/2020/7/new-findings-on-gileads-biktarvy-presented-at-aids-2020-virtual-include-positive-switch-data-in-older-adults
12. Rolle C P, et al. Real-world efficacy and safety of switching to bictegravir/emtricitabine/tenofovir alafenamide in older people living with HIV. Medicine, 2021, 100(38).
来源:感染医线
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
.png)
责任编辑:彭伟彬
相关搜索: CROI 2024