- 首页 > 正文
优案医评丨一例CRO叠加感染所致重症肺炎诊治经历
感染医线 发表时间:2024/7/5 18:11:17
编者按:碳青霉烯耐药革兰阴性菌(CRO)的广泛传播已成为全球性的公共卫生问题。CRO传播能力强,感染者预后通常较差,死亡率高。高龄患者、长时间住院、入住监护室、接受机械通气、侵入性操作、抗菌药物暴露以及严重基础疾病等因素,均为CRO等多重耐药(MDR)菌感染的高危因素。CRO通常对抗菌药物呈广泛耐药甚至全耐药,可供临床选择的抗菌药物非常有限。同时,高危患者往往伴有多种基础疾病和脏器功能不全,在有限的治疗选择下,使得治疗过程变得更加困难和复杂。本期《优案医评》由山东大学齐鲁医院杨慧医生介绍一例CRO叠加感染所致重症肺炎的患者,并特邀山东大学齐鲁医院王刚教授进行深入点评。该例患者通过采用包括新型氟环素类药物依拉环素在内的联合抗感染治疗,患者病情获得有效缓解。该病例强调了,对于多种MDR菌感染的高危患者,依据循证依据选择最佳抗菌药物联合方案的重要性。
病例介绍
患者:男,86岁。
主诉:咳嗽咳痰、间断发热9月余。
入院时间:2023-09-15
现病史:患者9月前出现咳嗽、咳痰,伴低热,就诊于当地医院,行CT示双下肺炎,给予抗感染等对症治疗后好转出院。后患者间断出现发热、咳嗽、咳痰,轻度胸闷等,多次住院行抗感染等对症治,症状仍有反复。1月前(8月14日)患者就诊于济南市某三甲医院。8月16日,痰液和尿液培养结果提示碳青霉烯耐药鲍曼不动杆菌(CRAB)阳性。给予替加环素联合甲氧苄啶/磺胺甲噁唑(SMZ)抗感染治疗,并多次纤支镜吸痰治疗,随后根据病原学结果对抗感染治疗方案进行了多次调整。住院期间,患者还接受了止咳化痰、补充白蛋白、纤支镜吸痰等对症支持治疗。尽管患者病情略有好转,但肺部感染仍较重。为寻求进一步诊治,患者转入山东大学齐鲁医院治疗。急诊以“肺部感染”收入感染病科。患者自发病以来,饮食差,睡眠差,留置导尿管,大便不规律,体重较前无明显变化。
既往史:“2型糖尿病”病史40余年,长期应用“甘精胰岛素、阿卡波糖片”降糖治疗,血糖控制尚可。“高血压病”病史3年,血压最高180/90 mmHg,现服用“硝苯地平控释片”,血压控制可。近2年内共有3次“脑梗死”病史,遗留四肢肌力减弱、行动不便等后遗症;“脑出血”病史2月余。否认乙肝、结核、艾滋、梅毒等传染病接触史。否认外伤史,2年前因前列腺增生行手术治疗,否认输血史。预防接种史不详,无药物及食物过敏史。
个人史:生于原籍,无疫区留居史,无疫水接触史,无动物饲养史,无节肢动物叮咬史,无接触生肉、无生食史,有有创操作史。生活饮食规律,无吸烟史,无饮酒史,无毒物接触史。无冶游史。
体格检查:T36.9℃,P 82次/分,R 23次/分,BP123/57 mmHg。神志模糊,精神差,营养一般,被动体位;浅表未触及肿大淋巴结,气管切开状态,颈软,无抵抗;双肺呼吸音粗,双下肺呼吸音低,可闻及干湿性啰音,心率91次/分,心律不齐,脉搏短绌,心音正常,各瓣膜听诊区未闻及病理性杂音。腹软,无压痛,无反跳痛,肝脾肋下未及,肝肾区无叩痛,移动性浊音(-);双下肢无水肿,四肢肌力查体欠合作,四肢肌张力升高,脑膜刺激征阴性,左侧病理征(+),右侧病理征未引出。
▌实验室检查:
2023-09-14
血常规:中性粒细胞百分比80.3%,淋巴细胞百分比13.2%,血红蛋白(HGB)94 g/L,血小板计数(PLT)123×109/L,白细胞计数(WBC)6.95×109/L,C反应蛋白(CRP)1.74 mg/L,降钙素原(PCT)0.892 ng/ml,红细胞沉降率(ESR)2 mm/h;
血气分析:PH 7.43,PCO2 39 mmHg,PO2 119 mmHg。
▌影像学检查:
2023-08-30胸部CT显示:(1)双肺炎性变,双侧胸腔积液。(2)心脏增大,心包积液,主动脉、冠脉钙化斑。
.png)
△外院胸部CT(2023-08-30)
2023-09-08胸部CT示双肺炎症较前减少,双侧胸腔积液较前减少,右肺部分不张,心包积液,主动脉、冠脉钙化斑。

△外院胸部CT(2023-09-08)
▌入院诊断:
- 重症肺炎
呼吸衰竭
胸腔积液(双侧)
右肺部分不张
- 脑出血后遗症
- 陈旧性脑梗死
- 2型糖尿病
- 高血压病(3级,很高危)
- 心房颤动
- 前列腺增生术后
- 轻度贫血
- 胆囊结石伴慢性胆囊炎
- 右肾结石
- 心包积液
诊治过程
▌经验性抗感染治疗
本例为高龄患者,且存在多个CRO感染高危因素,尽管既往痰培养提示CRAB阳性,但最近一次外院CT示双肺炎症及双侧胸腔积液较前减少,且入院时多项指标处于正常范围内,因此需谨慎区分感染与定植。患者初入我院时及时留取了微生物标本,9月15至18日期间未应用抗菌药物,同时给予患者高流量湿化氧疗,监测患者生命体征及体温,体温波动在37.1~37.5℃。
▌目标性抗感染治疗
9月18日,胸片示双肺炎症表现,对比院前CT进展。痰培养结果显示:CRAB,菌落计数(++++)。此外,患者体温有升高趋势,考虑CRAB可能为致病菌。根据2023年美国感染病学会(IDSA)抗微生物药物耐药革兰阴性菌感染治疗指南建议[1],结合药敏结果,并考虑患者经济负担等因素,给予患者头孢哌酮/舒巴坦(3 g,ivdrip,q6h,维持3h)+米诺环素(200 mg,po,q12h)抗感染治疗。
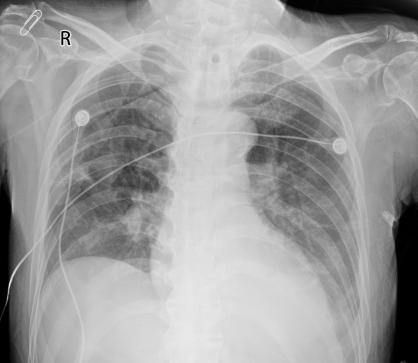
△胸片(2023-09-18)
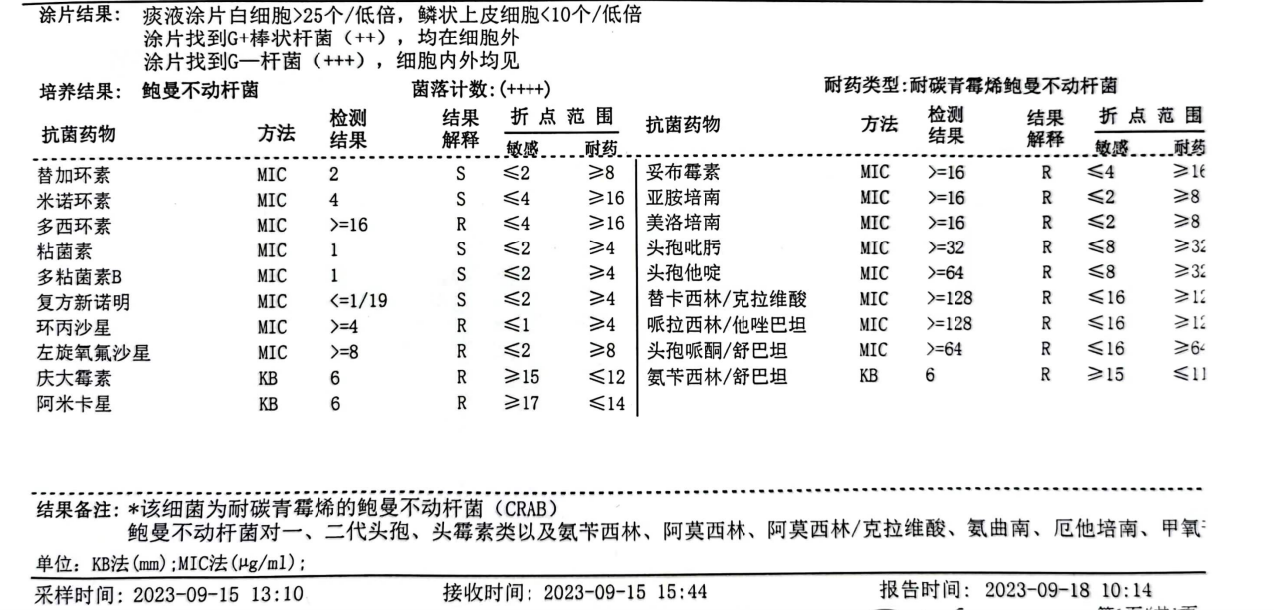
△痰培养及药敏结果(2023-09-18)
9月25日,痰培养检出碳青霉烯耐药肺炎克雷伯菌(CRKP)和碳青霉烯耐药铜绿假单胞菌(CRPA)。9月26日,患者CRP(66.43 mg/L)、ESR(49 mm/h)迅速上升;复查胸片示:双肺炎症,较前进展。考虑当前抗菌方案对CRKP及CRPA抗菌力度不足,遂根据IDSA 2023指南[1],优化抗感染方案为:依拉环素(50 mg,ivdrip,q12h,输注60min以上)+头孢哌酮/舒巴坦(3 g,ivdrip,q6h,维持3h)+头孢他啶/阿维巴坦(2.5 g,ivdrip,q8h,维持3h)。
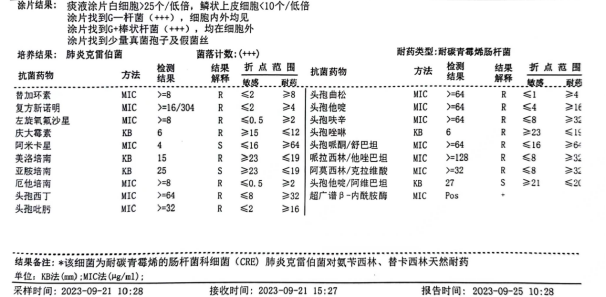
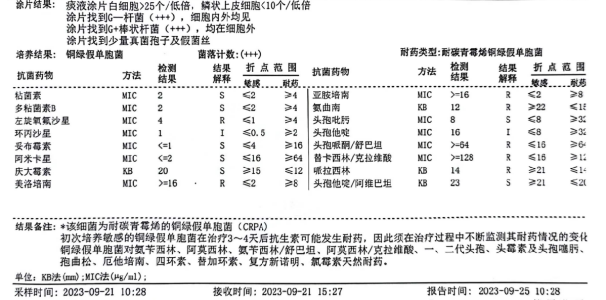
△痰培养及药敏结果(2023-09-26)
10月5日,患者炎症得到有效控制,血常规示患者CRP(1.79 mg/L)及ESR(13 mm/h)均显著下降;胸片较前缓解。遂进行降阶梯治疗,调整抗感染方案为:头孢哌酮/舒巴坦+米诺环素+头孢他啶/阿维巴坦。10月10日,复查胸片,肺部炎症面积较前减少,氧合指数较前好转,炎症指标较前降低。应用以上方案抗感染治疗2周后患者症状好转。
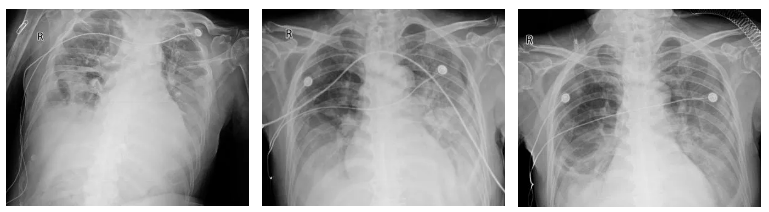
△院内治疗过程中患者胸片变化(09-26、10-05、10-10)
病例小结
患者为老年男性,有高血压、糖尿病、脑梗死、脑出血等病史,曾反复住院并接受气管插管治疗。外院病原学曾检出多种CRO,经高级别抗菌药物治疗效果较差。入院后,针对定植与感染进行排查,初始抗菌方案效果不佳。需思考如何优化抗菌方案,以降低DDD,改善预后。在本例的治疗中,尽管药敏结果显示替加环素敏感,但其MIC值偏高,需大剂量使用,存在肝损伤和凝血功能障碍风险,且存在在肺组织中分布不足等劣势。依拉环素作为全球首个氟环素类抗菌药物,可广谱覆盖多种常见革兰阳性菌、阴性菌和非典型病原体;其具有强大的抗菌活性,全球药敏数据显示,依拉环素对鲍曼不动杆菌的体外抗菌活性是替加环素的4倍,对肺炎克雷伯菌的体外抗菌活性是替加环素的2倍[2];同时,依拉环素在肺组织中有较高的组织浓度,与其他抗菌药物联用也显示出良好的协同作用。对于本例CRAB+CRKP+CRPA感染患者,依拉环素与头孢哌酮/舒巴坦、头孢他啶/阿维巴坦的联合应用,可协同加强对CRAB、CRKP的疗效,是一种较优选择,在改善患者氧合、肺部感染及全身症状方面显示出了较好的效果。
名师点评
王刚 教授
山东大学齐鲁医院
本例患者为高龄患者,存在长期住院、入住监护室、接受机械通气、侵入性操作、抗菌药物暴露以及严重基础疾病等多种耐药菌感染高危因素。住院期间出现多种CRO菌感染,对治疗提出了巨大挑战。因此临床医生在患者入院之初需精准评估微生物证据,谨慎判断定植与感染,这对有效控制感染、改善患者预后至关重要。
在本例的治疗中,临床医生并未采用MIC值偏高的替加环素。实际上,近年来关于替加环素的应用,临床存在许多值得思考的问题:
首先,折点问题尤为突出,体外药敏报告结果与临床应答不一致。目前国内仍沿用美国FDA自2005年以来一直未调整的折点标准,而随着细菌耐药性不断演变,这一标准的适用性受到了挑战。2014年,德国一项研究指出,替加环素在MIC为1 mg/L时,目标达标率不足30%[3],这表明原折点标准(S≤1,R>2)过高,难以确保治疗效果。基于此,欧洲药敏试验委员会(EUCAST)于2019年下调了MIC折点标准(S≤0.5,R>0.5)[4],以更准确地反映药物敏感性。后续的研究进一步证实了,不同MIC值下替加环素单药治疗产碳青霉烯酶肺炎克雷伯菌(CP-Kp)菌血症患者的30天死亡率存在显著差异,即MIC<0.5 mg/L时死亡率为20.0%,而MIC为0.75~2 mg/L时死亡率升至50.9%,这一结果支持了EUCAST下调折点标准的决定[5]。
其次,疗效与安全性之间的平衡问题不容忽视。替加环素在血清和肺泡上皮衬液中的分布浓度不理想,而其非线性血浆蛋白结合(PPB)的特点,使得单纯增加剂量不一定能提高治疗达标率[6],反而可能增加药物性肝损伤、凝血功能异常等不良反应风险[7]。此外,近年来关于替加环素耐药问题的讨论也日益增多。因此,我们需要重新评估替加环素的临床应用策略,以确保疗效并减少不良反应及耐药性发展。
这些问题不仅困扰临床用药,还会对患者治疗效果和临床结局产生影响,需引起临床重视。值得欣慰的是,我国已制定并发布了首个“抗菌药物体外药敏中国临床折点”。这一“中国标准”是基于我国流行病学调查的数据所建立的,因此更加符合中国人群的临床细菌感染用药需求,同时也确保药敏试验结果的准确性。随着该标准的应用,国内抗菌药物合理应用工作将步入新的发展阶段。
作为首个明确中国临床折点的药物,新型氟环素依拉环素的临床应用将得到进一步规范。依拉环素是一种新类别抗微生物药物,在真实世界研究中,其已被广泛应用于不同部位感染、不同合并症的患者当中。在一项纳入腹腔内感染、肺部感染、糖尿病足感染等多种感染类型患者的回顾性观察队列研究中[8],接受依拉环素方案治疗的患者临床缓解率达94%。在另一项包括免疫抑制患者的多中心、回顾性、队列研究中,患者的临床成功率为75.7%、30天存活率为94.7%、无微生物学复发率为94.5%[9]。
医学知识体系快速迭代,新的循证证据不断涌现,诊疗指南也在不断更新。临床医生应保持开放态度,积极吸收新知识,避免局限于传统观点和治疗药物。依拉环素作为全球首个氟环素类抗菌药物,凭借其良好的临床疗效和安全性,已被多个国内外指南和共识推荐用于治疗CRO等MDR革兰阴性菌感染。面对传统抗菌药物的局限性,依拉环素的出现为临床抗感染治疗提供了新的选择。我们期待依拉环素能够补充现有抗菌药物的不足,满足临床多样化的治疗需求,从而使更多中国患者获益。
参考文献
[1] Tamma PD, Aitken SL, Bonomo RA, Mathers AJ, van Duin D, Clancy CJ. Infectious Diseases Society of America 2023 Guidance on the Treatment of Antimicrobial Resistant Gram-Negative Infections. Clin Infect Dis. Published online July 18, 2023. doi:10.1093/cid/ciad428
[2] Hawser S, Kothari N, Monti F, Morrissey I, Siegert S, Hodges T. In vitro activity of eravacycline and comparators against Gram-negative and Gram-positive bacterial isolates collected from patients globally between 2017 and 2020. J Glob Antimicrob Resist. 2023;33:304-320. doi:10.1016/j.jgar.2023.04.017
[3] The European Committee on Antimicrobial Susceptibility Testing. Revision of Tigecycline Breakpoints for Enterobacterales and other species with an "Intermediate" category. Breakpoint Committee and General Consultation. October 2018. Available From: https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/Consultation/2018/Tigecycline_consultation_October_2018.pdf
[4] The European Committee on Antimicrobial Susceptibility Testing. Breakpoint tables for interpretation of MICs and zone diameters. Version 9.0, 2019. http://www.eucast.org.
[5] Papadimitriou-Olivgeris M, Bartzavali C, Nikolopoulou A, et al. Impact of Tigecycline's MIC in the Outcome of Critically Ill Patients with Carbapenemase-Producing Klebsiella pneumoniae Bacteraemia Treated with Tigecycline Monotherapy-Validation of 2019's EUCAST Proposed Breakpoint Changes. Antibiotics (Basel). 2020;9(11):828. Published 2020 Nov 19. doi:10.3390/antibiotics9110828
[6] Singh RSP, Mukker JK, Drescher SK, Deitchman AN, Derendorf H. A need to revisit clinical breakpoints of tigecycline: effect of atypical non-linear plasma protein binding. Int J Antimicrob Agents. 2017;49(4):449-455. doi:10.1016/j.ijantimicag.2016.12.008
[7] Shi X, Zuo C, Yu L, et al. Real-World Data of Tigecycline-Associated Drug-Induced Liver Injury Among Patients in China: A 3-year Retrospective Study as Assessed by the Updated RUCAM. Front Pharmacol. 2021;12:761167. Published 2021 Nov 2. doi:10.3389/fphar.2021.761167
[8] Van Hise N, Petrak RM, Skorodin NC, et al. A Real-World Assessment of Clinical Outcomes and Safety of Eravacycline: A Novel Fluorocycline. Infect Dis Ther. 2020;9(4):1017-1028. doi:10.1007/s40121-020-00351-0
[9] Kunz Coyne AJ, Alosaimy S, Lucas K, et al. Eravacycline, the first four years: health outcomes and tolerability data for 19 hospitals in 5 U.S. regions from 2018 to 2022. Microbiol Spectr. 2024;12(1):e0235123. doi:10.1128/spectrum.02351-23

王刚 教授
山东大学齐鲁医院
感染病科副主任
博士、副主任医师,临床副教授,硕士生导师。美国微生物学会(American Society for Microbiology)会员,山东省感染性疾病质控中心副主任,山东省医学会细菌感染与耐药防治分会副主委,山东省医学伦理学会感染性疾病分会副主委,山东省医药教育协会感染与临床微生物管理专业委员会副主委,山东省医师协会感染医师分会常委;山东病理生理学会炎症发热感染委员会秘书;山东省感染发热疾病联盟常务理事长;Infectious Medicine编委。主要从事感染性发热疾病的诊治。

杨慧 教授
山东大学齐鲁医院
感染性疾病科主治医师
主要研究方向:细菌真菌感染诊治及耐药菌诊疗
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。

责任编辑:彭伟彬
相关搜索: 重症肺炎