- 首页 > 正文
OTC滴眼液安全吗?美国多州出现CRPA爆发,源头直指人工泪液
感染医线 发表时间:2024/8/13 17:07:50
编者按:人工泪液是一种模仿天然眼泪成分的替代品,这类滴眼液通过模拟眼泪的成分和性质,为眼睛提供润滑,减轻干眼症状,如疼痛、灼热感等。然而,近日《临床感染病杂志》(Clinical Infectious Diseases)发表的一项研究介绍了一起令人关注的公共卫生事件:美国多州出现了产碳青霉烯酶、碳青霉烯耐药铜绿假单胞菌(CP-CRPA)的爆发,源头直指许多人日常使用的人工泪液。
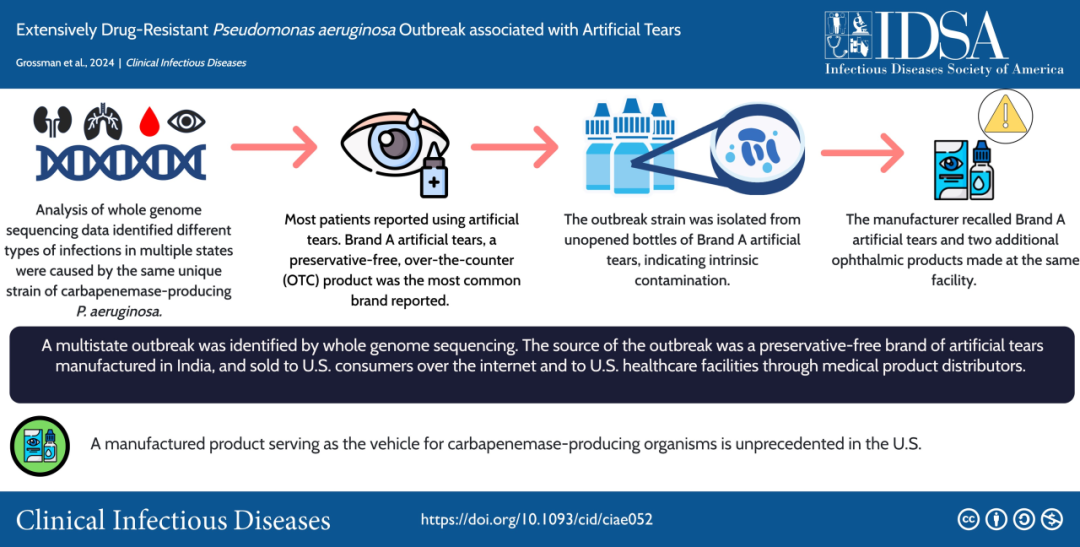
背景
产碳青霉烯酶、碳青霉烯耐药铜绿假单胞菌(CP-CRPA)是美国新兴的公共卫生威胁。这些细菌通常具有广泛的耐药性,与非CP-CRPA相比,其所导致的感染死亡率更高。在美国,尽管CRPA临床分离株中仅有约2%携带碳青霉烯酶(此比例在其他国家更高),但其引发的疫情已不仅限于单一医疗机构,或通过患者网络传播,已有报道指出,曾有一次与医疗旅游相关的跨州爆发。
为了有效监测和应对CP-CRPA,美国通过抗微生物药物耐药性实验室网络(AR Lab Network)收集临床实验室发现的CRPA分离株,并进行碳青霉烯耐药机制的检测,以支持感染控制和公共卫生决策。自2021年起,美国疾病控制和预防中心(CDC)更是将CP-CRPA分离株的全基因组测序(WGS)列为优先事项,旨在深入了解循环菌株的分子流行病学特征,并为地方疫情调查提供科学依据。
2022年9月,在对一家后期急性护理机构中CP-CRPA爆发的WGS数据进行分析时,研究人员发现了具有独特遗传特征的菌株——该菌株序列类型(ST)为1203,携带VIM变异体blaVIM-80和GES变异体blaGES-9,这两种变异体此前均未在美国分离株中报道过。随后,通过对AR Lab Network中已测序的分离株进行回顾性和前瞻性分析,研究人员从5个州发现了30株具有相同遗传特征的分离株,这些分离株均来自2022年5月以来的样本。本文详细介绍了对这一爆发源头的调查情况。
方法
初步调查
调查病例定义为:从2022年1月1日至2023年5月15日期间收集并上报给美国CDC的任何标本来源中,首次分离到携带特定基因(blaVIM-80和blaGES-9)铜绿假单胞菌ST1203的美国患者。
2022年10月,美国CDC向全美发出呼吁,要求临床实验室将对头孢他啶或头孢吡肟不敏感的CRPA分离株提交至AR Lab Network进行碳青霉烯耐药机制检测,并向公共卫生官员报告产VIM的CRPA分离株以进一步确定其特征。
初步调查纳入了2022年11月之前发现的病例。研究人员收集了病例所在医疗机构使用的医疗产品数据,以及患者的病史数据,包括留置装置和药物。为了提出关于爆发来源的假设,研究人员在一家后期急性护理机构开展了一项1:1匹配病例对照研究。对照组为CP-CRPA筛查呈阴性且无临床CRPA培养的患者,并根据科室和入院日期的重叠进行病例匹配。从病历中收集了关于医疗产品、程序和设备的信息。
病例调查
使用标准化病例报告表收集全国所有病例的数据,并填写病历,并在可能的情况下与病例或其代理人进行面谈。
考虑到医疗机构对患者接受的人工泪液品牌进行追踪的局限性以及门诊患者回忆的局限性,研究人员采用分级定义对人工泪液的暴露情况进行了分类:
确认暴露(confirmed):患者或代理人在病历中记录或报告了相关品牌的人工泪液。
很可能暴露(probable):(1)患者在住院机构接受了人工泪液治疗,而该机构同时使用了相关品牌和其他品牌的人工泪液,且未记录患者接受的具体品牌;(2)患者报告收到了公司或医疗机构的人工泪液召回通知,并且不记得召回品牌的名称,但描述了与相关品牌相匹配的产品。
可能暴露(possible):患者在一家医疗机构接受门诊医疗保健服务,而该医疗机构在临床治疗过程中使用了相关品牌的产品,并且/或者向患者提供了相关品牌的产品,但未记录每位患者使用的是哪个品牌的产品。
追溯和产品调查
州和地方卫生部门以及美国食品药品管理局(FDA)从患者家中、医疗机构、配送中心和药房收集流行病学调查中发现的已开封和未开封的人工泪液产品。对产品进行细菌培养,并对分离株进行WGS检测。
结果
初步调查
1:1匹配病例对照研究显示,调查病例无菌水暴露的可能性是对照组的15倍(粗匹配OR 15.0,95%CI:0.86~262.6;未计算调整OR[aOR]),人工泪液暴露的可能性是对照组的5倍(粗匹配OR 5.0,95%CI:1.1~22.8;aOR:4.7,95%CI:0.98~22.5,调整机械通气)。
进一步分析发现,4家机构中只有2家机构的病例使用吸入无菌水,且这2家机构报告的无菌水品牌不同。所有4个机构中的病例都使用了人工泪液;至少有2个机构报告了6种不同品牌的人工泪液。鉴于这些发现以及2个群组的眼部感染情况,研究人员将调查重点放在了人工泪液上。
病例调查
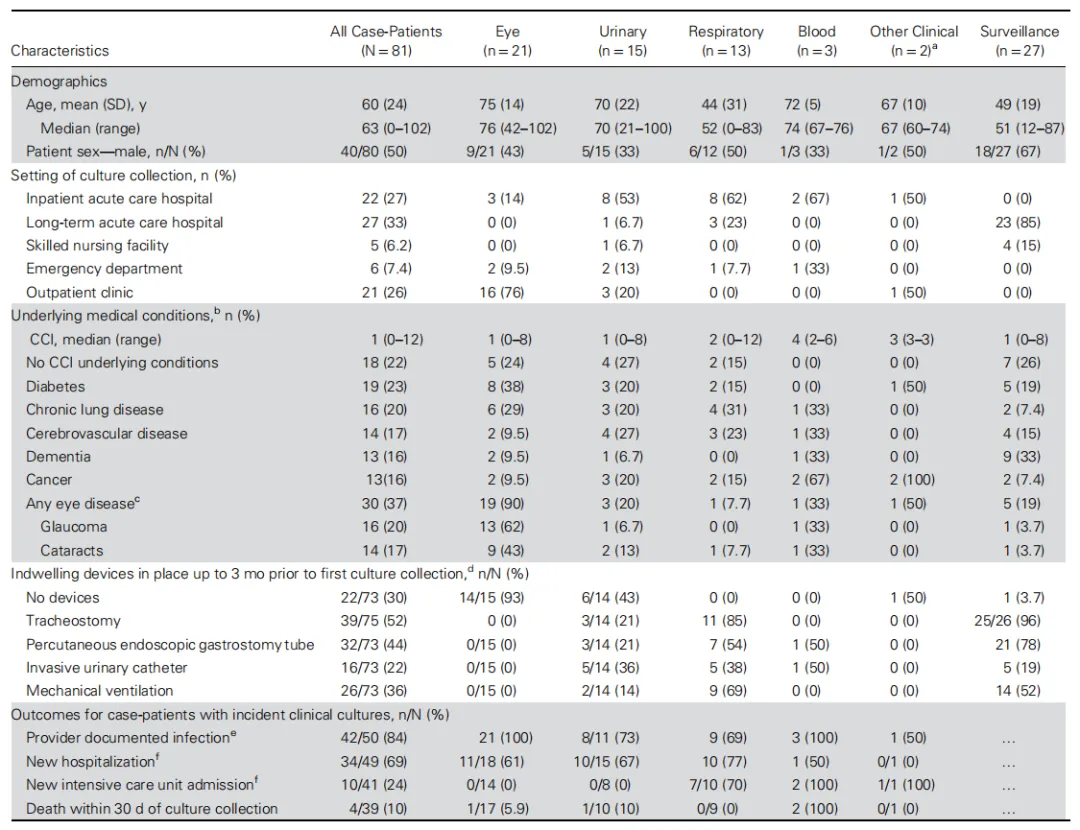
截至2023年5月15日,在18个州发现了81例患者。标本采集至病例确认的中位时间为43天(范围:14~310天)。分离株具有广泛的耐药性,美国CDC的药敏结果显示,有5株分离株仅对头孢地尔敏感。总体而言,54例(67%)患者是从眼部(n=21,39%)、泌尿道(n=15,28%)、呼吸道(n=13,24%)、血液(n=3,5%)、伤口(n=1,2%)和耳部(n=1,2%)的临床培养中发现的。从直肠拭子(n=26)和痰(n=1)的监测培养中发现了27例(33%)。
不同培养来源的患者临床特征和结局不同:
从临床培养中分离出暴发菌株的50例患者中,有42例(84%)在病例中记录了相关感染信息,包括眼部感染(n=21,50%;包括角膜炎但未发展为眼内炎,12/21,57%;角膜炎发展为眼内炎,6/21,28%;全眼球炎,2/21,9.5%;不明眼部感染,1/21,5%)、尿路感染(n=8,19%)、呼吸道感染(n=9,21%)、菌血症(n=3,7%)和中耳炎伴放射性骨坏死(n=1,2%)。
在39例临床培养且有结局信息的患者中,有4例(10%)在标本采集后30天内死亡;在18例眼部感染的患者中,有4例(22%)接受了眼球摘除术。
另有14例患者在培养采集30天后患侧眼出现视力受损:3例(23%)有中度视力障碍(最佳矫正视力[BCVA]≤20/70和>20/200),11例(77%)成为法定盲人(BCVA≤20/200或仅限于感知眼前手部的晃动或光感)。
在通过监测培养确定的27例患者中,有6例(22%)在随后的临床培养中检出了爆发菌株(血流:n=2;呼吸道:n=3;尿液:n=1),这些菌株的中位采集时间为监测培养后152天(范围:22~252天)。
表1. 81例患者的人口统计学特征、临床特征和结局
总体而言,在70例提供信息的患者中,有61例(87%)报告使用过人工泪液;在56例提供品牌信息的患者中,有43例(77%)报告使用过Y生产商生产的A品牌非处方(OTC)人工泪液,包括22例确认暴露、14例很可能暴露、7例可能暴露。另有1例患者报告了另外一种由Y生产商生产的人工泪液产品,即B品牌。
在22例未报告使用人工泪液或报告使用其他品牌人工泪液的患者中,有12例(55%)在时间和/或空间上与其他病例存在医疗机构重叠,或在使用A品牌人工泪液的医疗机构住院,可能通过机构内传播感染了爆发菌株。
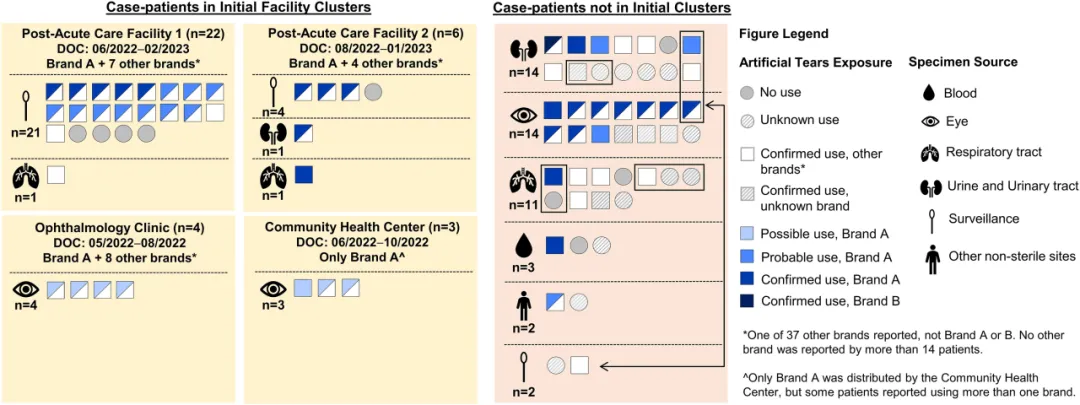
△携带blaVIM-80和blaGES-9铜绿假单胞菌ST1203患者的人工泪液使用情况
追溯和产品调查
品牌A和B人工泪液是制造商Y在印度同一地点生产的不含防腐剂的产品,采用多剂量瓶包装,通过互联网销售给美国消费者,并通过医疗产品经销商销售给美国医疗机构。
美国CDC和FDA检测了已开封(n=17)和未开封(n=18)的A品牌人工泪液;每个批次检测了1~149瓶。从6批次已开封的A品牌人工泪液、2批次未开封的A品牌人工泪液和另外2批次未开封的A品牌人工泪液的复合样本中检出了携带blaVIM-80和blaGES-9的铜绿假单胞菌ST1203。在7批次未开封的B品牌中,有5批次(71%)分离出了细菌,来自2种不同的产品:人工泪液(4批次)和人工眼膏(1批次),但未检出铜绿假单胞菌。
对来自患者(n=81)、已开封(n=21)和未开封(n=6)的A品牌瓶中的108株分离株进行系统发育分析后发现,这些样本之间存在0-110个单核苷酸多态性(SNP)差异,来自参考基因组6.5 Mb(91.8%)的克隆框架。大多数分离株(n=105)只有0~13个SNPs的差异;两个0-SNP群来自多个州的患者分离株以及已开封和未开封的A品牌产品。爆发分离株与美国和其他国家的其他铜绿假单胞菌ST1203分离株明显不同。
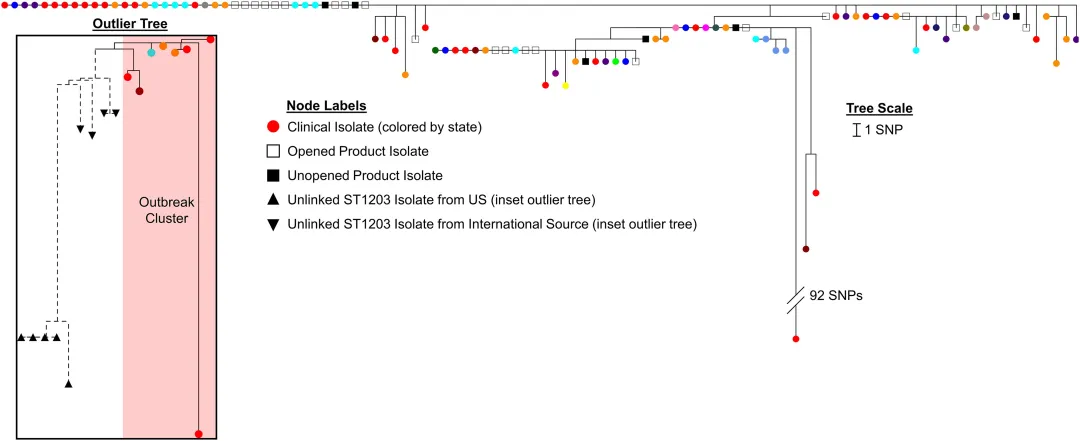
△系统发育树
结论
通过分子流行病学的方法确定,A品牌人工泪液是导致全美多州爆发CP-CRPA的源头,这一发现突显了美国在OTC产品进口商监管方面存在的不足。此外,由于爆发菌株对多数抗菌药物具有耐药性,这限制了治疗选择,增加了公共卫生风险。因此,需要改进监管措施和公共卫生响应能力,以有效遏制未来类似疫情的爆发,并减少耐药菌株在更广泛的人群中传播。
▌参考文献:
Grossman MK, Rankin DA, Maloney M, et al. Extensively Drug-Resistant Pseudomonas aeruginosa Outbreak Associated With Artificial Tears. Clin Infect Dis. 2024;79(1):6-14. doi:10.1093/cid/ciae052