- 首页 > 正文
卢洪洲教授:2024年艾滋病流行病学和治疗进展丨年度盘点·HIV治疗篇
感染医线 发表时间:2025/1/28 0:47:30
自1981年首次报告艾滋病病例以来,艾滋病一直是全球公共卫生的重大挑战。近年来,尽管在治疗和防控方面取得了显著进展,但艾滋病的流行趋势和疾病负担依然不容忽视。为实现 “2030年终结艾滋病流行”的目标,全球在筛查、诊断、治疗、监测、预防等诸多关键环节仍需不断探索和完善。本期,《感染

01
全球艾滋病流行趋势和疾病负担
自1981年首次报告艾滋病病例以来,艾滋病一直是全球关注的重大公共卫生挑战。近年来,尽管在治疗和防控方面取得了显著进展,但艾滋病的流行趋势和疾病负担依然不容忽视。根据《柳叶刀-HIV》(The Lancet HIV)发表的一项研究[1],全球艾滋病的流行趋势和疾病负担呈现出复杂的地域差异。
据统计,2021年全球约有4 000万人感染HIV,其中71.8%正在接受抗反转录病毒治疗(ART)。尽管ART覆盖率有所提高,但仍有大量人群未能获得及时有效的治疗。从1990年到2021年,全球艾滋病的流行趋势经历了显著变化。2010年至2021年间,全球新发HIV感染人数下降了21.9%,从211万例下降到了165万例。艾滋病相关死亡人数也下降了39.7%,从119万例减少到71.8万例。然而,这种下降趋势并非全球一致,部分地区甚至出现了感染和死亡人数的上升。
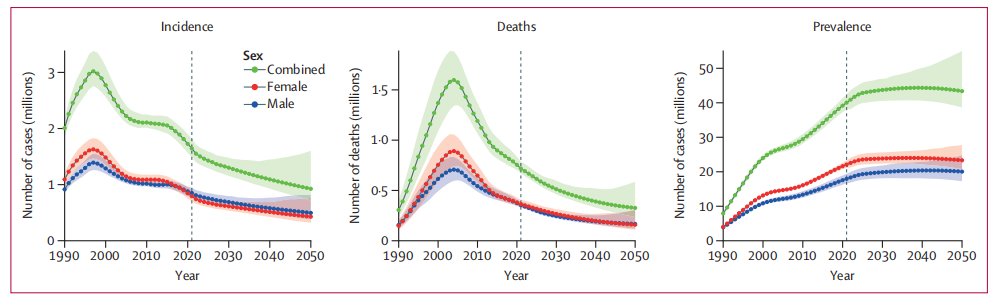
△1990-2050年HIV感染的发病率、病死率和流行率趋势
艾滋病疾病负担在全球范围内分布不均。撒哈拉以南非洲地区是受HIV影响最严重的地区,2021年该地区约有2 910万人感染HIV,占全球感染人数的72.8%。此外,该地区的艾滋病相关死亡人数也最高,2021年达51.5万例。尽管如此,该地区在降低HIV感染率和病死率方面仍然取得了显著进展,新发感染和死亡人数均大幅下降,这主要得益于大规模的ART推广和综合预防措施的实施。然而,中欧、东欧和中亚以及北非和中东地区却出现了HIV感染和病死率的上升。
2021年,亚洲地区的HIV感染人数和死亡人数虽然低于撒哈拉以南非洲地区,但仍是全球HIV疾病负担的重要地区,并在艾滋病的流行趋势中呈现出显著的地域差异。其中,中亚部分国家的HIV感染率和病死率呈现上升趋势;东南亚和东亚地区虽然整体感染率较低,但部分国家如泰国、缅甸、柬埔寨等仍面临较高的HIV流行率;在南亚地区,印度是受HIV影响最严重的国家之一,尽管近年来新发感染人数有所下降,但庞大的人口基数使得该地区HIV防治任务依然艰巨。
研究预测,尽管全球HIV感染和死亡人数将继续下降,但到2030年,全球仍将有超过4 000万人需要终身接受ART治疗。到2050年,全球HIV感染人数预计将达到4 340万。要实现“2030年终结艾滋病流行”的目标,全球仍需付出巨大努力。
02
HIV治疗与防控的权威指导
2024年,全球及我国在HIV治疗与防控领域发布了多项重要的指南、共识和政策性文件,为HIV防治工作提供了全面、科学的指导。这些文件不仅更新了艾滋病的诊断和治疗标准,还强调了综合干预、早期诊断、个体化治疗和社区参与的重要性,为实现“2030年终结艾滋病流行”的目标提供了有力支持。

这些文件和指南/共识的发布,不仅为医疗专业人员提供了最新的诊治标准,还为多部门卫生工作者提供了明确的行动方向。在这些指导性文件和专业指南/共识的推动下,全球及我国的艾滋病防治工作将更加科学、规范和有效,为最终实现终结艾滋病流行奠定了坚实的基础。
03
2024年HIV治疗研究的重要突破
治愈病例持续推进
2024年,HIV治疗领域迎来了多项重大突破,其中最引人瞩目的无疑是HIV治愈病例的持续进展。自2008年“柏林患者”首次被治愈以来,HIV治愈的案例不断增加,为全球HIV治疗带来了治愈希望和新的方向。
第7例治愈病例:杂合子干细胞移植的突破[16]
2024年7月,德国柏林夏里特医学院的研究团队在第25届国际艾滋病大会(AIDS 2024)上宣布了全球第7例HIV治愈病例——“下一个柏林患者”。这位60岁的德国男性患者于2009年被诊断为HIV感染,2015年被诊断为急性髓系白血病(AML)。在接受杂合子CCR5 Δ32/WT的干细胞移植后,患者自2018年9月停止ART,至今已超过5年未检测到HIV病毒反弹。这一病例的特殊之处在于,供体的干细胞并非传统的纯合子CCR5 Δ32/Δ32突变,而是杂合子突变。尽管如此,患者依然实现了长期的HIV缓解,这为HIV治愈提供了新的思路。
病例汇报者Christian Gaebler教授表示,这一病例的成功可能与移植后新免疫系统的快速建立有关。移植后的免疫系统迅速取代了患者原有的免疫系统,这一过程在不到30天内完成。此外,供体的免疫系统可能具有特殊的抗病毒能力,例如高度活跃的自然杀伤细胞,能够有效清除HIV病毒。
第8例治愈病例:纯合子干细胞移植的再验证[17]
2024年11月,在HIV Glasgow大会(Glasgow 2024)上,法国人体免疫和病毒感染信息中心(CISIH)研究团队报道了全球第8例HIV治愈病例。这位50多岁的女性患者于1999年确诊HIV-1感染,2010年开始接受ART治疗,并在2020年因AML接受了纯合子CCR5 Δ32/Δ32异体造血干细胞移植。移植后,患者的HIV病毒载量持续为阴性,HIV抗体滴度逐渐下降,且在停止ART治疗后的10个月内未出现病毒反弹。这一病例再次验证了CCR5 Δ32/Δ32干细胞移植在HIV治愈中的有效性。
表1. 已报道8例造血干细胞移植治愈的HIV病例
|
首次移植时间 |
患者 |
性别 |
恶性肿瘤 |
移植CCR5基因型 |
|
2007 |
柏林患者 |
男 |
AML |
CCR5 Δ32/Δ32 |
|
2016 |
伦敦患者 |
男 |
霍奇金淋巴瘤 |
CCR5 Δ32/Δ32 |
|
2011 |
杜塞尔多夫患者 |
男 |
AML |
CCR5 Δ32/Δ32 |
|
2017 |
纽约患者 |
女 |
AML |
CCR5 Δ32/Δ32 |
|
2019 |
希望之城患者 |
男 |
AML |
CCR5 Δ32/Δ32 |
|
2018 |
日内瓦患者 |
男 |
白血病/双表型肉瘤 |
CCR5 WT/WT |
|
2015 |
下一个柏林患者 |
男 |
AML |
CCR5 Δ32/WT |
|
2020 |
第8例潜在治愈患者 |
女 |
AML |
CCR5 Δ32/Δ32 |
治愈性疗法研究进展
在HIV治疗方面,尽管ART能够有效抑制HIV复制,但无法彻底清除病毒储存库,因此治愈性疗法的研究进展备受关注。2024年,多项研究在这一领域取得了显著突破,为HIV功能性治愈带来了新的希望。
PD-1抑制剂Budigalimab[18]
在2024年反转录病毒和机会性感染大会(CROI 2024)上,研究者们展示了PD-1抑制剂Budigalimab在HIV功能性治愈中的最新研究进展。Budigalimab是一种抗PD-1单克隆抗体,旨在通过增强免疫系统对HIV的控制能力,实现无ART的病毒抑制。在一项Ⅰb期随机双盲研究中,研究者对HIV-1感染者进行了Budigalimab治疗,并在分析性治疗中断(ATI)期间进行了疗效和生物标志物分析。结果显示,接受10 mg剂量治疗的受试者中,有6例实现了延迟病毒反弹和/或无ART病毒控制,其中2例在超过29周的时间内维持病毒载量低于200 copies/mL。这一结果表明,Budigalimab在促进免疫介导的病毒控制方面具有潜力,值得在Ⅱ期研究中进一步评估。
M10 CAR-T细胞疗法[19]
复旦大学、第四军医大学唐都医院和广西中医药大学的研究团队开发了一种新型嵌合抗原受体T细胞免疫治疗(CAR-T)——M10 CAR-T细胞疗法。该疗法通过设计一种特殊的CAR分子,使T细胞能够识别并攻击HIV感染细胞,同时中和潜伏病毒逆转后产生的游离病毒。在一项I期、多中心、单组、开放标签研究中,18名HIV-1感染者接受了M10细胞输注治疗。结果显示,74.3%的患者在治疗后病毒反弹得到了显著抑制,病毒载量平均下降67.1%。此外,10名患者在150天的观察期内表现出细胞相关HIV-1 RNA水平持续降低,平均下降1.15 log10。该研究证明了M10 CAR-T细胞疗法的安全性和有效性,为HIV功能性治愈提供了新的潜在治疗选择。
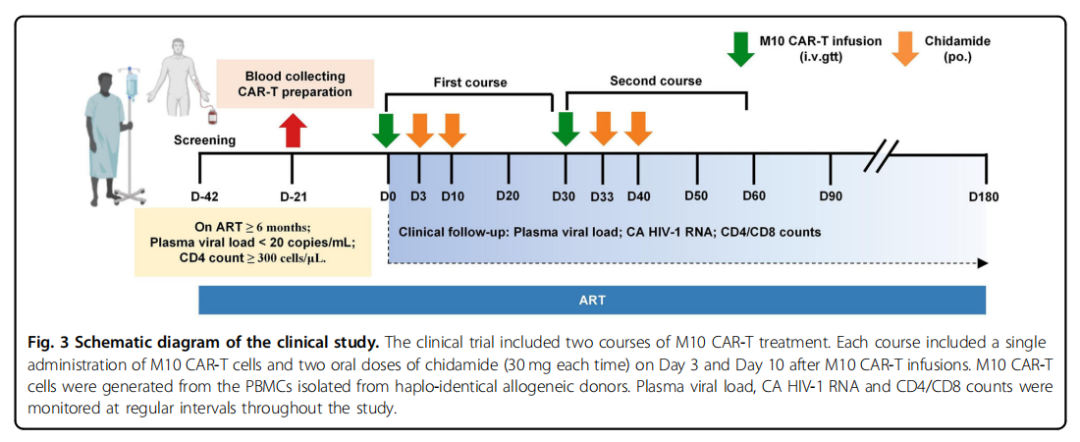
△临床研究示意图
HIV-1疫苗ICVAX[20]
2024年11月,深圳市第三人民医院与香港大学团队联合研发的艾滋病治疗性核酸疫苗ICVAX完成了Ⅰ期临床试验,并取得了积极结果。ICVAX疫苗旨在通过诱导广谱、多功能的病毒特异性T细胞,实现无需ART即可控制病毒复制的目标。在一期临床试验中,45名志愿者接种后未出现严重不良事件,且均诱导出超预期的T细胞免疫应答,显示出良好的安全性和免疫原性。该项研究计划于2025年中期启动Ⅱ期临床试验,进一步探索其在更大人群中的疗效和安全性。
HIV储存库研究的深入探索[21]
在基础研究方面,深圳市第三人民医院艾滋病研究团队在Nature子刊《信号转导和靶向治疗》(Signal Transduction and Targeted Therapy)上发表了一项重要研究,探讨了不同ART时机对HIV储存库的影响。研究通过对急性感染期启动ART组(Acute-ART组,n=54)和AIDS阶段启动ART组(AIDS-ART组,n=36)参与者的HIV前病毒整合位点测序数据进行分析,发现急性期启动ART的患者,其HIV DNA水平显著低于AIDS阶段启动ART的患者。此外,急性期启动ART能够延缓病毒整合细胞的克隆扩增,减少稳定储存库的形成。这一发现为早期干预的重要性提供了新的证据,并为未来的功能性治愈提供了依据。
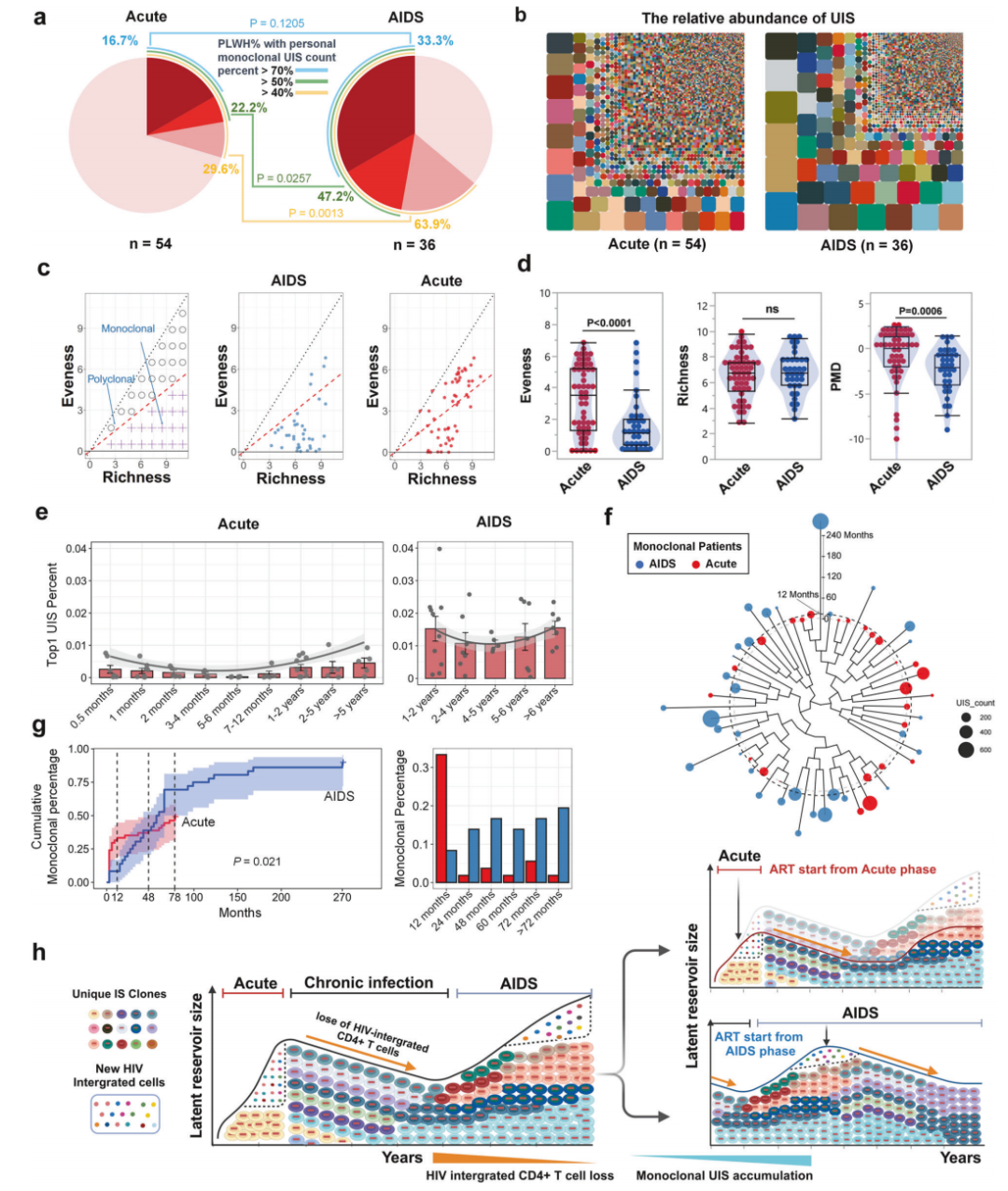
△Acute-ART组和AIDS-ART组独特整合位点(UIS)克隆的对比分析
初始ART方案
MK-8527[22]
MK-8527作为一种新型口服核苷类反转录酶易位抑制剂(NRTTI),其药代动力学特征支持每周一次或更长时间的给药频率。两项Ⅰ期单剂量单药治疗研究(NCT03615183和NCT05494736),共纳入31例初治HIV-1感染者,分别接受单剂量0.5 mg、1 mg、3 mg和10 mg的MK-8527治疗。结果显示,所有剂量组在给药后第7天的HIV-1 RNA平均降幅均≥1.0 log10 copies/mL,所有剂量水平上均表现出良好的耐受性,未报告严重不良事件或死亡,显示出良好的抗病毒活性和安全性。
GS-1720/GS-4182[23]
GS-1720是一种新型口服长效整合酶抑制剂(INSTI),GS-4182是LEN的前药。一项Ⅱ期临床试验(NCT06613685)正在开展,旨在评估每周口服GS-1720/GS-4182对比现有每日口服标准ART方案的病毒学抑制效果和耐受性。研究的主要终点为第24周HIV-1 RNA<50 copies/mL的参与者比例,次要终点包括第12和48周HIV-1 RNA<50 copies/mL的参与者比例、CD4+ T细胞计数变化、治疗期间不良事件发生率、药代动力学参数等。
病毒学抑制人群的平稳转换
多拉韦林/Islatravir(DOR/ISL)[24]
这项Ⅲ期、双盲、活性对照研究(NCT04223791)关注了DOR/ISL单片制剂在病毒学抑制人群中的应用,评估了从比克替拉韦/恩曲他滨/丙酚替诺福韦(B/F/TAF)转换至DOR/ISL的疗效和安全性。研究纳入了643名HIV-1 RNA<50 copies/mL的参与者,随机分配至DOR/ISL组或继续使用B/F/TAF组。结果显示,在48周时,DOR/ISL组和B/F/TAF组分别有0.6%和0.3%的参与者HIV-1 RNA≥50 copies/mL,表明DOR/ISL在维持病毒学抑制方面不劣于B/F/TAF。此外,DOR/ISL组未检测到治疗相关耐药性,且不良事件发生率与B/F/TAF相当。尽管DOR/ISL组的CD4+ T细胞计数有所下降,但并未导致感染相关不良事件的增加。
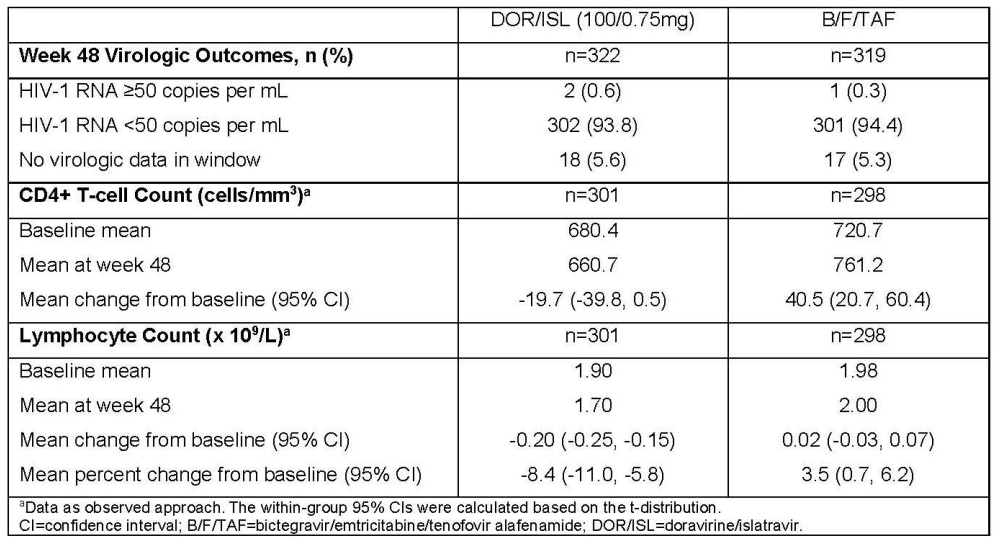
△疗效和安全性结局
来那帕韦/比克替拉韦(LEN/BIC)[25]
这项随机、开放标签研究(ARTISTRY-1)旨在评估从复杂多药方案转换至LEN/BIC的疗效和安全性。研究纳入了128例病毒学抑制的HIV感染者,随机分配至维持原方案、LEN/BIC 75/25 mg或LEN/BIC 75/50 mg。结果显示,在48周时,所有维持原方案的参与者保持病毒载量低于50 copies/mL,而LEN/BIC 75/25 mg和75/50 mg组分别有92.2%和90.4%的参与者保持病毒载量低于50 copies/mL。尽管LEN/BIC组的病毒学抑制率略低于原方案组,但差异无统计学意义。此外,LEN/BIC组的不良事件发生率与原方案相当,且未检测到治疗相关耐药性。
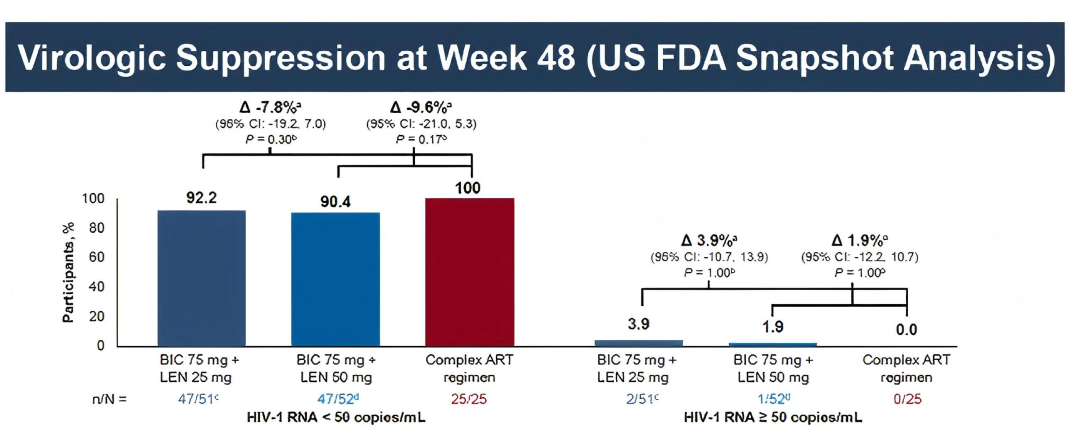
△三组病毒学抑制率对比
来那帕韦/Islatravir(LEN/ISL)[26]
这项Ⅱ期、开放标签、活性药物对照研究(NCT05052996)评估了从每日口服B/F/TAF转换至每周口服LEN/ISL的疗效和安全性。研究纳入了104例病毒学抑制的HIV感染者,随机分配至LEN/ISL组或继续接受B/F/TAF治疗。结果显示,在48周时,LEN/ISL组有94.2%的参与者保持HIV-1 RNA<50 copies/mL,与B/F/TAF组相当。LEN/ISL组未报告任何治疗相关≥3级不良事件,且CD4+ T细胞和淋巴细胞计数的变化与B/F/TAF组无显著差异。这些结果支持每周口服LEN/ISL的方案进入Ⅲ期研究。
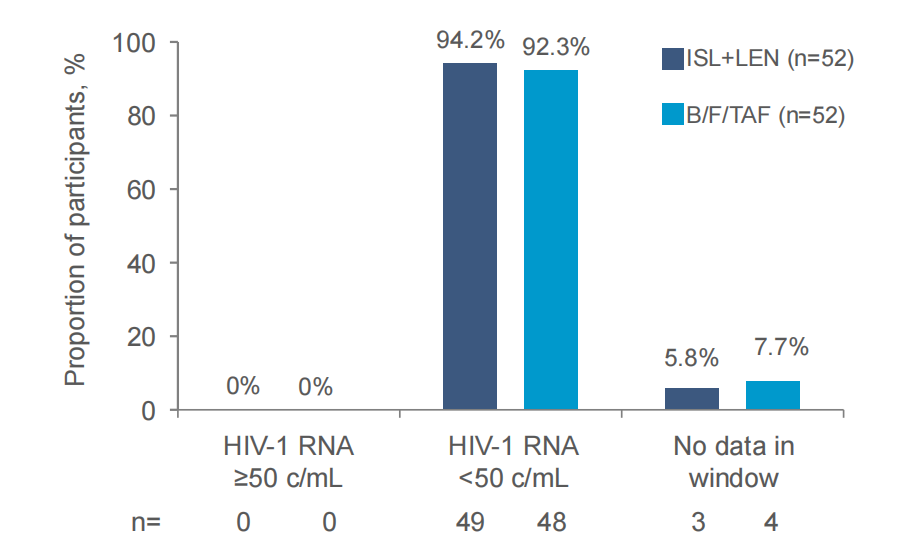
△两组患者48周时的病毒抑制情况对比
耐药HIV感染者的ART
2025年1月2日,国家药品监督管理局(NMPA)正式批准了LEN在国内上市,用于用于与其他抗反转录病毒(ARV)药物联合使用,治疗当前方案无法达到病毒学抑制的多重耐药(MDR)HIV-1感染的成人患者。
这一批准基于Ⅱ/Ⅲ期CAPELLA研究的积极结果[27]。该研究显示,LEN在多重耐药HIV-1感染者中具有较高的病毒学抑制率和良好的耐受性。在队列1中,83%的患者在第52周时HIV-1 RNA低于50 copies/mL,86%的患者HIV RNA低于200 copies/mL。尽管少数患者出现LEN耐药,但大多数在继续使用LEN的同时恢复了病毒学抑制。LEN的获批为耐药HIV感染者提供了新的治疗选择。
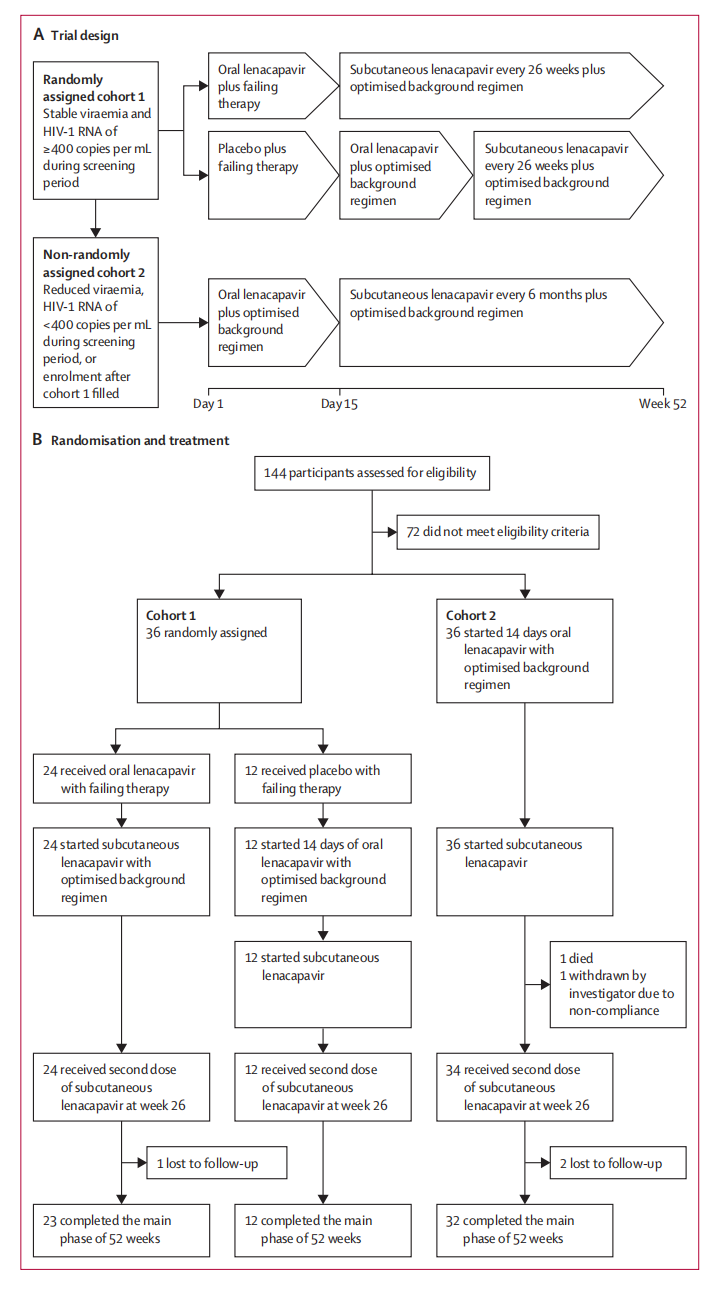
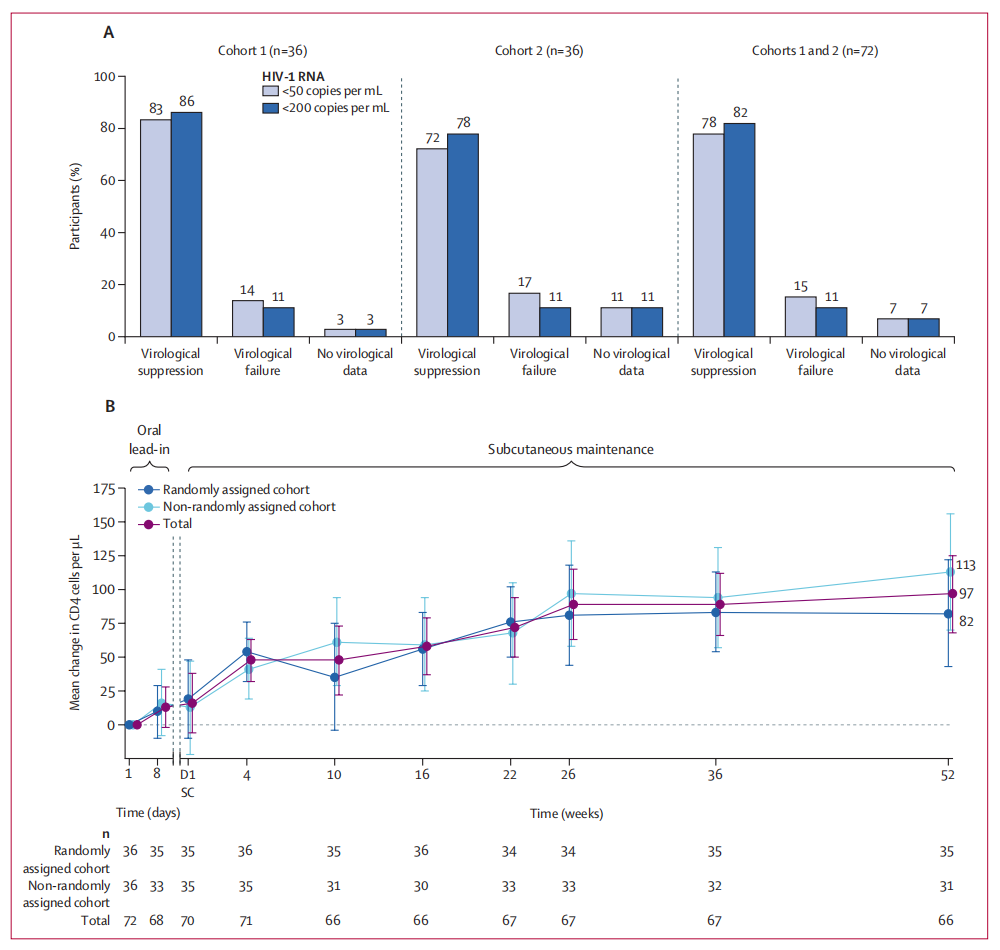
△CAPELLA研究设计(左)及52周的病毒学和免疫反应结果(右)
04
挑战与展望
2024年,HIV治疗领域取得了多项关键突破,从临床到基础,从耐药HIV感染者的治疗优化到治愈性疗法,为终结HIV流行带来了新的希望。展望未来,随着更多临床试验的开展和新型疗法的探索,HIV治疗将更加精准化和个体化。全球HIV防治工作仍需加强多部门合作,提升检测覆盖率,优化治疗方案,并持续关注耐药问题,以实现2030年终结艾滋病流行的目标。
参考文献
[1] GBD 2021 HIV Collaborators. Global, regional, and national burden of HIV/AIDS, 1990-2021, and forecasts to 2050, for 204 countries and territories: the Global Burden of Disease Study 2021. Lancet HIV. 2024;11(12):e807-e822. doi:10.1016/S2352-3018(24)00212-1
[2] Implementing the global health sector strategies on HIV, viral hepatitis and sexually transmitted infections, 2022–2030: report on progress and gaps 2024, second edition. Geneva: World Health Organization; 2024.
[3] Consolidated guidelines on differentiated HIV testing services. Geneva: World Health Organization; 2024.
[4] Updated recommendations for the treatment of Neisseria gonorrhoeae, Chlamydia trachomatis and Treponema pallidum (syphilis), and new recommendations on syphilis testing and partner services. Geneva: World Health Organization; 2024.
[5] Recommendations for the treatment of Trichomonas vaginalis, Mycoplasma genitalium, Candida albicans, bacterial vaginosis and human papillomavirus (anogenital warts). Geneva: World Health Organization; 2024.
[6] Framework for monitoring sexually transmitted infections and strengthening surveillance. Geneva: World Health Organization; 2024.
[7] Guidelines for HIV post-exposure prophylaxis. Geneva: World Health Organization; 2024.
[8] WHO implementation tool for pre-exposure prophylaxis (PrEP) of HIV infection: provider module for oral and long-acting PrEP. Geneva: World Health Organization; 2024.
[9] Supporting re-engagement in HIV treatment services. Geneva: World Health Organization; 2024.
[10] Ensuring quality health care by reducing HIV-related stigma and discrimination: technical brief. Geneva: World Health Organization; 2024.
[11] 国务院办公厅关于印发《中国遏制与防治艾滋病规划(2024—2030年)》的通知. Available from: https://www.gov.cn/zhengce/content/202412/content_6992032.htm
[12] 中国性病艾滋病防治协会HIV合并肝病专业委员会,广州医科大学附属市八医院,李凌华.中国HIV合并HBV、HCV感染诊治专家共识[J].中国艾滋病性病,2024,30(4):339-346.DOI:10.13419/j.cnki.aids.2024.04.02.
[13] 中华医学会感染病学分会艾滋病丙型肝炎学组,陈耀凯,李太生,张文宏.艾滋病合并隐球菌病诊疗专家共识(2024年更新版)[J].中国艾滋病性病,2024,30(5):447-458.DOI:10.13419/j.cnki.aids.2024.05.01.
[14] 中华医学会感染病学分会艾滋病学组,中国疾病预防控制中心,李太生.中国艾滋病诊疗指南(2024版)[J].协和医学杂志,2024,15(6):1261-1288.DOI:10.12290/xhyxzz.2024-0766.
[15] 李凌华,蔡琳,陈雅红,等.长效抗HIV药物临床应用专家共识.中国艾滋病性病,2024,30(12):1230-1239.
[16] Christian Gaebler, et al. The next Berlin patient: sustained HIV remission surpassing five years without antiretroviral therapy after heterozygous CCR5 WT/Δ32 allogeneic hematopoietic stem cell transplantation. AIDS 2024; abstract SS0402LB.
[17] Zaegel-Faucher Olivia, et al. Absence of viral rebound without antiretrovirals after CCR5Δ32/Δ32 allogeneic hematopoietic stem cell transplantation: A new case of a potential cure of HIV? HIV Drug Therapy Glasgow 2024; abstract P206.
[18] Preethi Krishnan, et al. Biomarker Signatures in Phase Ib Study With PD-1 Inhibitor, Budigalimab, in PLWH Undergoing ATI. CROI 2024; abstract 106.
[19] Mao Y, Liao Q, Zhu Y, et al. Efficacy and safety of novel multifunctional M10 CAR-T cells in HIV-1-infected patients: a phase I, multicenter, single-arm, open-label study. Cell Discov. 2024;10(1):49. Published 2024 May 14. doi:10.1038/s41421-024-00658-z
[20] 治疗用艾滋病核酸注射液(ICVAX)在ART治疗稳定的HIV/AIDS者的安全性、耐受性和免疫原性I期临床试验. Trial No.: CTR20223007. Available from: www.chinadrugtrials.org.cn
[21] Wang J, Xiao N, Zhu Z, et al. Comparing acute versus AIDS ART initiation on HIV-1 integration sites and clonal expansion. Signal Transduct Target Ther. 2025;10(1):23. Published 2025 Jan 10. doi:10.1038/s41392-024-02113-7
[22] Russ P. Carstens, et al. Single Dose Administration of MK-8527, a Novel nRTTI, in Adults With HIV-1. CROI 2024; abstract 115.
[23] Study of Oral Weekly GS-1720 and GS-4182 Compared With Biktarvy in People With HIV-1 Who Have Not Been Treated. clinicaltrials.gov; 2025 Jan. Report No.: NCT06613685. Available from: https://clinicaltrials.gov/study/NCT06613685?intr=GS-4182&rank=1
[24] Anthony M.Mills, et al. Switch To DOR/ISL (100/0.75mg) QD From B/F/TAF: Week 48 Results From A Phase 3 Trial. CROI 2024; abstract 197.
[25] Karam Mounzer, et al. Efficacy and safety of bictegravir plus lenacapavir: 48-week outcomes in virologically suppressed people with HIV-1 on complex antiretroviral regimens at baseline. CROI 2024; abstract OAB2602.
[26] Amy E. Colson, et al. Week 48 Results of a Phase 2 Study Evaluating Once-weekly Oral Islatravir Plus Lenacapavir. IDWeek 2024; abstract 577.
[27] Ogbuagu O, Segal-Maurer S, Ratanasuwan W, et al. Efficacy and safety of the novel capsid inhibitor lenacapavir to treat multidrug-resistant HIV: week 52 results of a phase 2/3 trial. Lancet HIV. 2023;10(8):e497-e505. doi:10.1016/S2352-3018(23)00113-3
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
