- 首页 > 正文
CCML2025丨赵建宏教授:临床微生物检验相关新颁行业标准介绍
感染医线 发表时间:2025/10/15 17:54:16
编者按:随着医学检验技术的快速发展和质量管理要求的不断提高,卫生行业标准在规范临床微生物检验工作中的重要性日益凸显。在中国医院协会临床微生物实验室专业委员会2025年学术年会暨临床微生物与感染新进展学习班上,河北医科大学第二医院赵建宏教授系统介绍了临床微生物检验相关新颁行业标准的最新进展。
为何要重视卫生行业标准
国家卫生健康标准管理制度
国家卫生健康委员会建立了一套完整的标准 管理制度体系。《卫生健康标准管理办法》自2019年6月26日起施行,《国家卫生健康标准委员会章程》和《卫生健康标准项目管理细则》均于2025年5月19日起实施,《卫生健康标准专业委员会考核评价办法(试行)》于2025年6月1日起施行。此外,《地方卫生标准工作管理规范》自2012年3月1日起实施,《卫生健康标准编写指南》自2021年7月7日起实施,共同构成了卫生健康标准管理的制度框架。
根据《标准化法》第二条规定,强制性标准必须执行。国家鼓励采用推荐性标准。不符合强制性标准将承担相应的法律责任,包括民事责任、行政处罚、信用记录影响甚至刑事责任。
卫生行业标准具有四个显著特点:权威性、民主性、科学性、实用性。
标准分类与体系
标准可分为政府标准和非政府标准两大类。政府标准包括国家标准(GB、GB/T约4万项)、行业标准(WS、WS/T约8万项)和地方标准(DB约7万项);非政府标准包括团体标准(T/约10万项)和企业标准(Q/约316万项)。各类标准的编号由代号、标准顺序号和年号三部分组成。标准还分为强制性标准和推荐性标准(带/T标识)。
卫生健康标准现行有效1549项(不含食品、中医),其中国家标准252项,卫生行业标准825项,国家职业卫生标准472项。按管理性质分,强制性标准402项,推荐性标准1147项。国家卫生健康委管理1252项,国家疾控局管理297项。
标准管理机构与职责
国家卫生健康委法规司负责项目、人员、强标实施评估等归口管理,承担标委会秘书处职能;业务司局负责专业标准制修订及实施。协调管理机构(统计信息中心、医管中心、疾控中心)负责协调审查、标准应用研究、综合性和跨专业领域重大标准研制、重点标准宣贯培训以及重大推荐性标准实施评估。专业委员会承担标准追踪、立项建议、基础研究、项目管理、审查、复审咨询及分析、宣贯、实施评估以及参加国际标准化活动等职责。国际标准化工作组(委卫生发展研究中心)负责组织、协调、推进卫生健康领域国际标准化活动。
标准制修订流程
标准起草需要包括内容、验证、采标、格式等方面的要求。起草人需提交项目执行计划书,修订标准需开展实施评估,秘书处将实施评估报告提供给标准起草人。常见问题包括大量搬抄其他标准条款(应引用标准号即可)和编制说明中各项技术内容的依据过于笼统(建议使用参考模板)。报批阶段协调机构在1个月内完成审查,法规司和业务司审核后报批。发布阶段行标由委通告发布并向国标委备案,国家职业卫生标准由委通告发布,国家标准由办公厅函报国标委发布。
标准结构的发展变化
标准体系结构经历了从政府主导到政府主导与市场自主相结合的发展过程。最初只有政府主导的国家标准、行业标准和地方标准,现在增加了市场自主的团体标准和企业标准,形成了更加完善的标准体系结构。
临床微生物检验相关标准体系
2024年至今,临床微生物检验领域发布了多项重要行业标准。
表1. 2024年至今微生物检验新颁布行标

(引自讲者会议幻灯)
目前还有多项微生物检验相关行业标准正在制定或修订中。
表2. 待发布的微生物检验相关行标
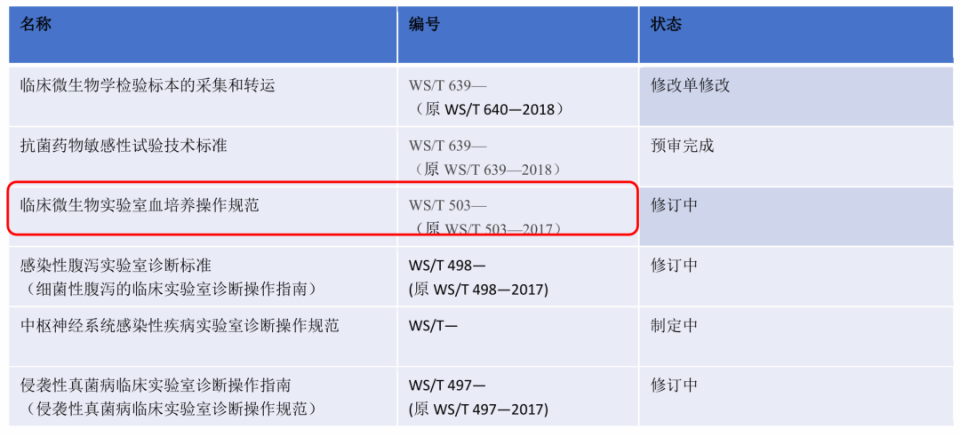
(引自讲者会议幻灯)
新近发布标准简介
临床实验室生物安全指南(WS/T 442-2024)
该标准代替WS/T 442-2014,主要变化包括:增加了规范性引用文件;增加了术语和定义,包括生物安全二级实验室、病原微生物、风险管理、风险识别、风险分析、风险评估、风险准则、风险评价、风险应对、利益相关方等;增加了附录A《临床实验室生物安全风险评估参考示例》和附录D《临床实验室工作人员个体防护装备选用原则》;删除了术语中生物因子、高效空气过滤器、危险识别等内容;删除了第五章《实验室生物安全防护水平分级》;删除了附录C《生物安全柜使用、维护及校验》和《高压灭菌器使用、维护及校验》。
起草单位包括中国医科大学附属第一医院/国家医学检验临床医学研究中心、解放军总医院第五医学中心、上海市东方医院、华中科技大学同济医学院附属同济医院、江苏省疾病预防控制中心、军事科学院军事医学研究院、北京市朝阳区疾病预防控制中心、北京医院/国家卫生健康委临床检验中心。
该标准特色是全面、系统、详实,强调了“风险”的理念,通用要求与重点突出结合,附录实用和借鉴性强。
表3.术语和定义
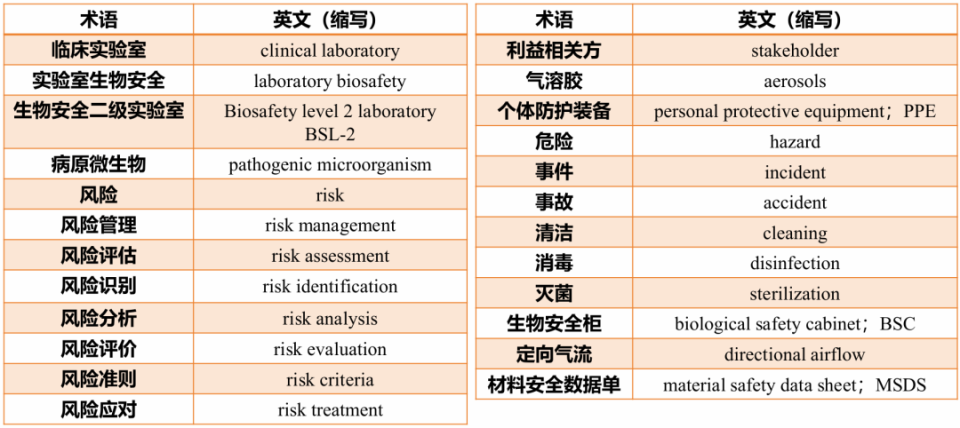
(引自讲者会议和幻灯)
标准中应特别关注的术语与定义包括:利益相关方(可以影响、被影响或自认为会被某一决策或行动影响的个人或组织);实验室生物安全(实验室的生物安全条件和状态不低于允许水平);生物安全二级实验室(符合国家标准《实验室生物安全通用要求》GB 19489-2008所规定生物安全防护水平为二级的实验室);事件(导致或可能导致事故的情况);事故(造成死亡、疾病、伤害、损坏以及其他损失的意外情况);生物安全柜(具备气流控制及高效空气过滤装置的操作柜);材料安全数据单(详细提供某材料的危险性和使用注意事项等信息的技术通报)。
风险管理部分要求生物安全风险管理应贯穿于实验室设计、建造、运行和管理的全过程。实验室应制定生物安全风险管理程序,建立良好的沟通和咨询机制,确保沟通和咨询贯穿于风险管理的全过程。风险评估应由对所涉及的病原微生物、设施设备、临床检验全流程和生物安全管理等熟悉的专业人员进行。风险评估所依据的资料及拟采取的风险应对措施、安全操作规程等应以国家法律法规及主管部门、世界卫生组织、国际标准化组织等机构或行业权威机构发布的指南、标准等为依据。风险评估报告应得到实验室设立单位的批准。
抗丝状真菌药物敏感性试验标准肉汤稀释法(WS/T 411-2024)
该标准代替WS/T 411-2013,主要变化包括:增加了术语和定义,如最低有效浓度、流行病学界值、野生型、非野生型和拖尾生长;抗真菌药物储存液使用的溶剂、稀释液和检测范围表格分为非皮肤真菌和皮肤真菌,增加了艾莎康唑、阿尼芬净、环吡酮、灰黄霉素、特比萘芬;增加了折点和流行病学界值结果解释;增加了CLSI及EUCAST两种药敏方法相应的报告结果方式;按培养基和材料质控、纯度质控、终点判读质控描述,增加了日常使用质控菌株的复苏方法;删除了质控频率和检测频率内容;明确了不适合本行标的真菌种类;更改了附录内容。
起草单位包括北京医院/国家卫生健康委临床检验中心、中国医学科学院北京协和医院、首都医科大学附属北京友谊医院、北京大学人民医院、北京大学第一医院、首都医科大学附属北京同仁医院、复旦大学附属华山医院、华中科技大学同济医学院附属同济医院。
标准范围规定适用于引起深部真菌感染的产孢丝状真菌的药物敏感性试验,包括曲霉属某些种及种复合群、镰刀菌属某些种及种复合群、根霉属某些种、毛霉目Mucorales(接合菌纲Zygomycetes)、多育节荚孢霉(原多育赛多孢霉)和申克孢子丝菌复合群的菌丝相、引起皮肤真菌感染的毛癣菌属某些种、小孢子菌属某些种、表皮癣菌属某些种。不适用于检测双相真菌如皮炎芽生菌、荚膜组织胞浆菌、粗球孢子菌属、马尔尼菲篮状菌、酵母样真菌的药敏试验,也不适用于检测棘白菌素类对皮肤真菌以及环吡酮、灰黄霉素或特比萘芬类对非皮肤真菌的药敏试验。
应特别关注的术语与定义包括:最低有效浓度(在最低浓度抗菌药物作用下,引起菌丝呈小而圆菌落、非融合生长变化的最低药物浓度,目前仅用于棘白菌素类抗真菌药);流行病学界值(基于菌株MIC值,将微生物群归类为是否含有获得性耐药和/或突变耐药表型的两个群体的界限值);野生型(通过ECV值定义的解释分类,对某种检测的抗真菌药物无获得性耐药机制或无敏感性降低的生物型)。
表4.术语和定义
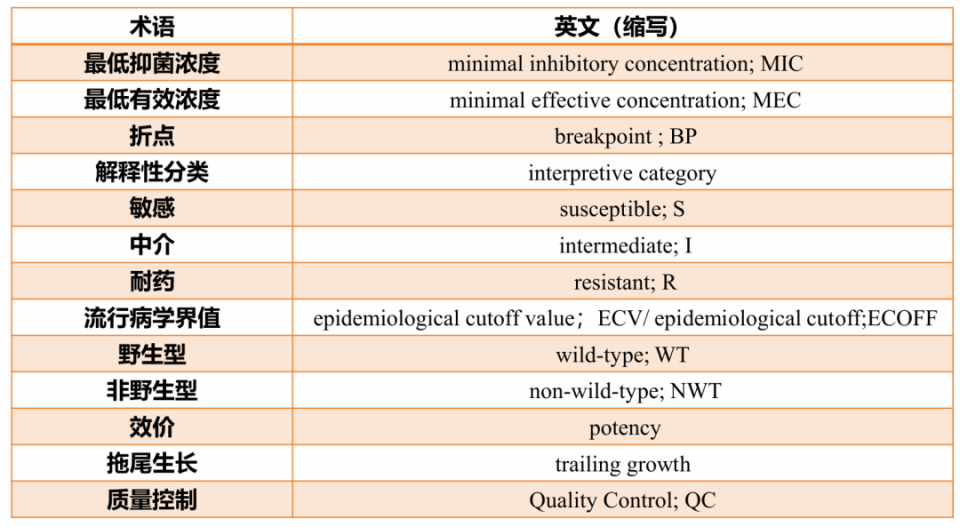
(引自讲者会议幻灯)
抗酵母样真菌药物敏感试验标准肉汤稀释法(WS/T 421-2024)
该标准代替WS/T 421-2013,主要变化包括:增加了术语和定义,如流行病学界值、野生型、非野生型和拖尾生长;抗真菌药物储存液使用的溶剂、稀释液和检测范围表格增加了瑞扎芬净、艾瑞芬净、Manogepix、艾沙康唑、酮康唑、雷夫康唑;增加了CLSI及EUCAST两种药敏方法相应的结果报告方式;按培养基和材料质控、纯度质控、终点判读和质控要求描述,增加了日常使用质控菌株的复苏方法;删除了术语定义中的"非敏感";删除了质量控制中质控频率和检测频率内容;更改了结果解释内容;调整了附录内容。
起草单位包括北京医院/国家卫生健康委临床检验中心、北京大学人民医院、首都医科大学附属北京友谊医院、中国医学科学院北京协和医院、华中科技大学同济医学院附属同济医院、上海市东方医院(同济大学附属东方医院)、北京大学第一医院、解放军总医院第一医学中心。
标准中重要术语定义包括:最低抑菌浓度(MIC);折点(BP);解释性分类;敏感(S);中介(I);耐药(R);剂量依赖性敏感(SDD);流行病学界值(ECV/ECOFF);野生型(WT);非野生型(NWT);效价;拖尾生长;质量控制(QC)。
表5.术语和定义
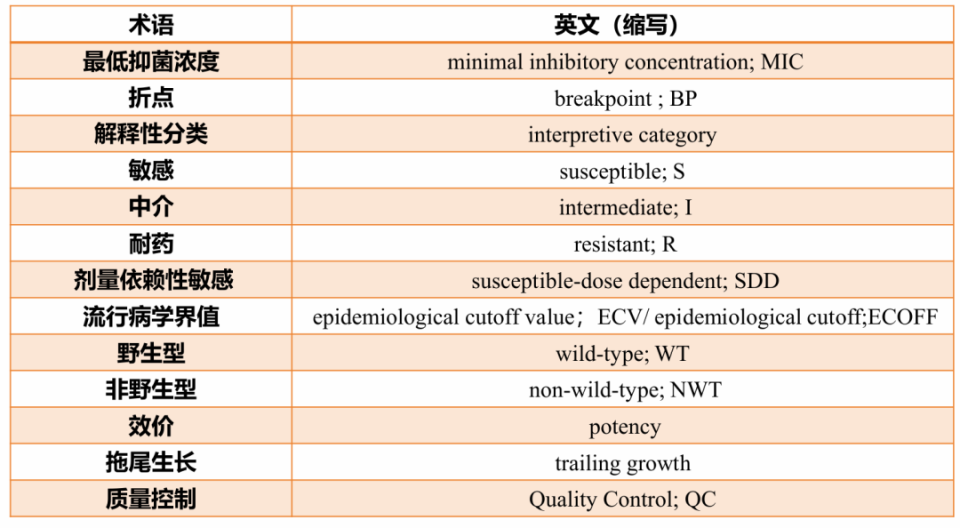
(引自讲者会议幻灯)
尿液标本临床微生物实验室检验操作指南(WS/T 489-2024)
该标准代替WS/T 489-2016,主要变化包括:增加了术语和定义“无症状菌尿”;增加了标本采集指征;增加了分枝杆菌实验室检测的尿液采集要求;更改了"尿液干化学分析"和"尿液有形成分分析"技术要求;更改了尿培养结果解释;更改了结果报告要求;更改了尿培养实验室检测流程图。
起草单位包括中国医学科学院北京协和医院、北京医院、吉林大学中日联谊医院、复旦大学附属中山医院、江苏省肿瘤医院、宁夏医科大学总医院、昆明医科大学第一附属医院。
标准特色是全面、系统、详实,强调了"系统化"的理念,从临床的视角出发,通用要求与重点突出结合。
重要术语定义包括:尿路感染(由各种病原体入侵泌尿系统引起的疾病);脓尿(新鲜未离心尿液中白细胞计数≥10个/mm³或尿沉渣镜检白细胞计数≥5个/高倍镜视野);无症状菌尿(患者尿液中有一种或多种细菌生长,定量培养菌落计数≥105 CFU/mL,但不存在尿路感染的症状或体征)。
表6.术语和定义
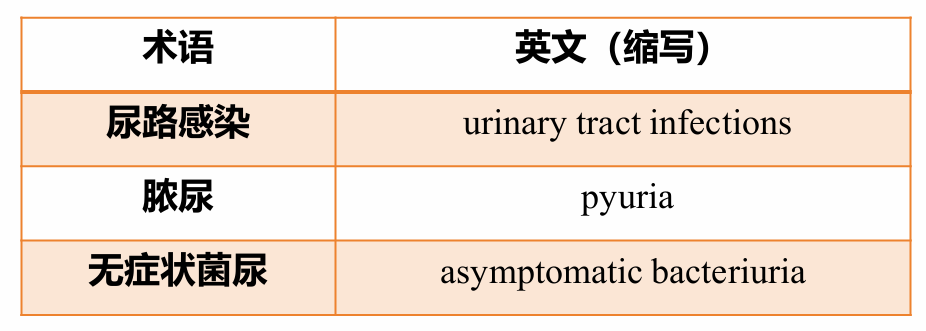
(引自讲者会议幻灯)
标本采集指征规定:尿路感染患者常出现尿频、尿急、尿痛等膀胱刺激征,可有肉眼脓尿或血尿、耻骨上区不适和腰骶部疼痛等表现。对于出现上述症状或尿液检验结果提示尿路感染,如白细胞酯酶异常、亚硝酸盐阳性等,或不明原因发热、留置导尿管患者出现发热等情况,建议采集尿液标本送检尿培养。送检尿培养同时需进行尿液常规检验,考虑合并系统感染时宜同时采集血培养。
标本采集总则要求:宜采集晨尿,嘱患者睡前少喝水或不喝水,尿液在膀胱内尽量潴留4h以上,可降低假阴性率;使用无菌广口容器采集,容器直径大于1 cm;女性可疑无症状菌尿患者应在2周内采集2次清晨清洁中段尿送检;影响尿液标本质量的因素较多,即使采用侵入性的尿液采集法仍可能被皮肤、会阴或尿道等处定植菌群污染,因此减少采样污染是保证尿液标本质量的关键。
清洁中段尿采集具体要求:清晨起床后用肥皂水或清水清洗会阴部,女性应分开大阴唇,男性应上翻包皮,仔细清洗,再用清水冲洗尿道口周围;弃去前段尿液,不中断尿流,留取中段尿液约10mL至无菌容器中,立即送检;清洁中段尿是临床最易获得的尿液标本,但中段尿液标本不能进行厌氧菌培养;女性患者应避免在月经期间采集尿标本;若尿液用于分枝杆菌培养,则连续3天分别采集清晨首次中段尿送检,每次宜采集至少40mL尿液。
标本拒收情况包括:标本标识与申请单不符,标识错误或没有标识;未提供采集时间及采集方法;标本采集时间超过2h而未在2°C~8°C冷藏或未使用含防腐剂的转运管保存;2℃~8℃冷藏或添加防腐剂但已超过24h;连续收集24h的尿液标本;导尿管尖端培养;标本取自导尿患者尿袋;标本送检时容器有渗漏;除耻骨上膀胱穿刺法外,采用其他方法采集标本申请做厌氧菌培养;尿培养采集尿量少于1mL。
实验室检查概述:尿液实验室检查是尿路感染诊断、辅助诊断、疗效观察和预后评估的主要方法;尿液干化学分析、尿液有形成分分析和尿沉渣镜检是尿路感染的筛查方法;尿培养是尿路感染的重要诊断方法,可提供感染病原菌的鉴定结果及菌落计数,并可进一步检测抗微生物药物敏感性;对于门诊单纯性尿路感染患者,尿培养不是必要检查;对于复发性的、经验治疗失败的或复杂性的门诊尿路感染患者或发生尿路感染的住院患者,尿培养是必要检查。
结果报告要求:革兰染色结果报告分阴性和阳性两种情况;抗酸染色结果报告分阴性和阳性两种情况;一般尿培养结果报告分阴性和阳性两种情况,阳性情况又分为临床意义明确进行鉴定和药敏、临床意义不明确仅进行鉴定、≥3种菌生长考虑定植菌生长三种情形。
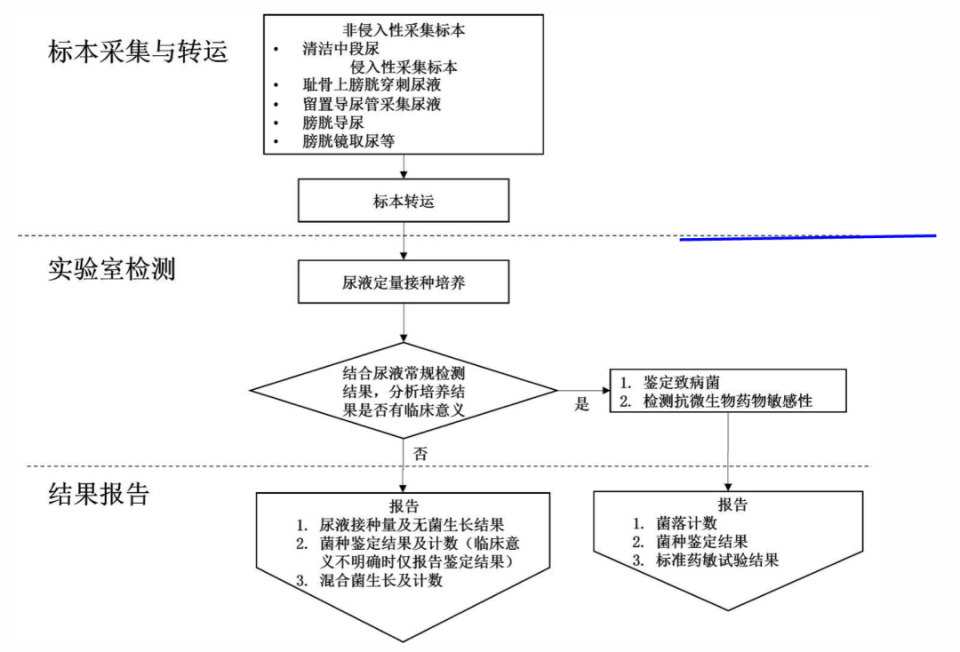
图1.尿液标本临床微生物实验室检验操作流程
(引自讲者会议幻灯)
总结
卫生行业标准在临床微生物检验工作中具有重要的指导意义和规范作用。新近发布的各项标准在术语定义、技术要求和操作流程等方面都进行了更加科学、细致的规范,体现了我国临床微生物检验标准化工作的最新进展。检验人员应当认真学习并严格执行这些标准,不断提高检验质量,为临床提供准确可靠的检测结果。
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
