- 首页 > 正文
IDWeek 2025丨俞云松教授:头孢德罗对革兰阴性菌包括CRO均显示很强的抗菌活性,且早期启动经验治疗临床治愈率更高
感染医线 发表时间:2025/11/12 23:19:34

01
应对CRO感染的挑战
头孢德罗对目前临床应用的新型β-内酰胺酶抑制剂不能抑制的碳青霉烯酶稳定
碳青霉烯耐药革兰阴性菌(CRO)已成为临床上威胁患者生命的重要病原体。最新的2025上半年CHINET监测数据[1]显示,碳青霉烯耐药肺炎克雷伯菌(CRKP)的分离率为24.6%,碳青霉烯耐药的鲍曼不动杆菌(CRAB)的分离率为76.5%,碳青霉烯耐药铜绿假单胞菌(CRPA)的分离率为24.9%,仍在高位流行。不同的CRO菌种碳青霉烯酶类型存在明显差异,且在同一株CRO菌株中可检出多种碳青霉烯酶。CHINET报道2025上半年的监测数据显示:碳青霉烯耐药的大肠埃希菌中金属酶检出率达78.4%,碳青霉烯酶肺炎克雷伯菌中KPC检出率达82.9%[1]。少数菌株同时检出KPC和NDM,碳青霉烯耐药的CRAB中OXA23的检出率高达99%,碳青霉烯耐药CRPA中KPC为主,同时有金属酶IMP和NDM被检出[2-3]。
针对CRO感染的治疗,传统抗菌药物存在明显的局限性,临床仍存在巨大的未被满足的需求。近年来,一些新型抗菌药物的临床应用为患者带来了新的希望。其中新型BL/BLI的新药最多,然而,这些新型BL/BLI中的β-内酰胺酶抑制剂的抑酶谱大多差异不大,存在少数均不能抑制的碳青霉烯酶,如美罗培南-韦博巴坦中的韦博巴坦不能抑制金属β-内酰胺酶(包括NDM、VIM、IMP等),也不能抑制D类的OXA-48酶;亚胺培南-西司他丁-瑞来巴坦中的瑞莱巴坦同样不能抑制金属β-内酰胺酶和OXA-48酶;头孢洛生-他唑巴坦中的他唑巴坦无法抑制所有的碳青霉烯酶[4-6]。
因此,新型BL/BLI在临床应用中需综合考虑细菌种类、耐药机制及是否存在复数菌感染等因素,部分患者可能需要联合其他抗菌药物以覆盖产不同碳青霉烯酶的CRO感染。头孢德罗作为一种新型铁载体头孢菌素,在C-3侧链上连接了一个儿茶酚基团,这一结构使其能够与铁离子形成螯合物,这种螯合物通过细菌的铁转运系统被主动运输进入细菌细胞[7]。由于其抗菌谱广,可覆盖产不同碳青霉烯酶的CRO,包括产KPC、MBL和OXA-48的肠杆菌目细菌和CRAB、CRPA等非发酵菌[8]。
02
从体外监测到真实世界研究
头孢德罗对新型BL/BLI不敏感的CRO菌株仍有很强抗菌活性
那么,目前对一种新型BL/BLI不敏感的CRO菌株,对其他新型BL/BLI以及其他新型抗菌药物是否也不敏感?2025年美国IDWeek大会报道了SENTRY抗菌药物耐药监测的结果[9]。该研究在2020-2024年间,在欧美国家收集了40048株肠杆菌目细菌和11757株铜绿假单胞菌菌株,根据CLSI折点评估对新型BL/BLI的敏感性,根据2025年CLSI、FDA和EUCAST折点评估头孢德罗的敏感性。研究的主要结果显示:
新型BL/BLI不敏感的革兰阴性菌分离率呈上升趋势
2020—2024年欧美国家新型BL/BLI不敏感的革兰阴性菌分离率均呈上升趋势,但总体仍维持较低水平。
在欧洲,肠杆菌目细菌对新型BL/BLI不敏感的比例:亚胺培南-西司他丁-瑞来巴坦(2.6%)、头孢他啶-阿维巴坦(1.6%)、美罗培南-韦博巴坦(2.1%);铜绿假单胞菌对新型BL/BLI不敏感的比例:亚胺培南-西司他丁-瑞来巴坦(4.7%)、头孢他啶-阿维巴坦(4.7%)、头孢洛生-他唑巴坦(5.5%)。
在美国,肠杆菌目细菌对新型BL/BLI不敏感的比例:亚胺培南-西司他丁-瑞来巴坦(0.4%)、头孢他啶-阿维巴坦(0.2%)、美罗培南-韦博巴坦(0.2%);铜绿假单胞菌对新型BL/BLI不敏感的比例:亚胺培南-西司他丁-瑞来巴坦(2.2%)、头孢他啶-阿维巴坦(3.4%)、头孢洛生-他唑巴坦(2.6%)。
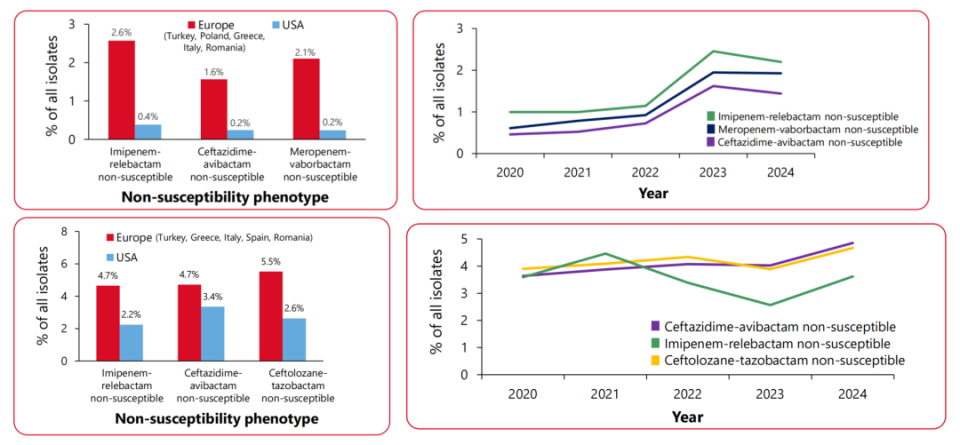
△2020-2024年欧美国家新型BL/BLI不敏感的肠杆菌目细菌(上)和铜绿假单胞菌(下)的分离率
新型BL/BLI耐药菌之间存在明显的交叉耐药,但与头孢德罗几乎无交叉耐药
这些新型BL/BLI不敏感的革兰阴性菌总体分离率很低,但在不同新型BL/BLI之间存在明显的交叉耐药。在头孢他啶-阿维巴坦不敏感的肠杆菌目细菌中,有高达84.5%的分离株对其他2种新型BL/BLI不敏感。在亚胺培南-西司他丁-瑞来巴坦不敏感的铜绿假单胞菌中,有高达54.7%的分离株对其他2种新型BL/BLI不敏感。
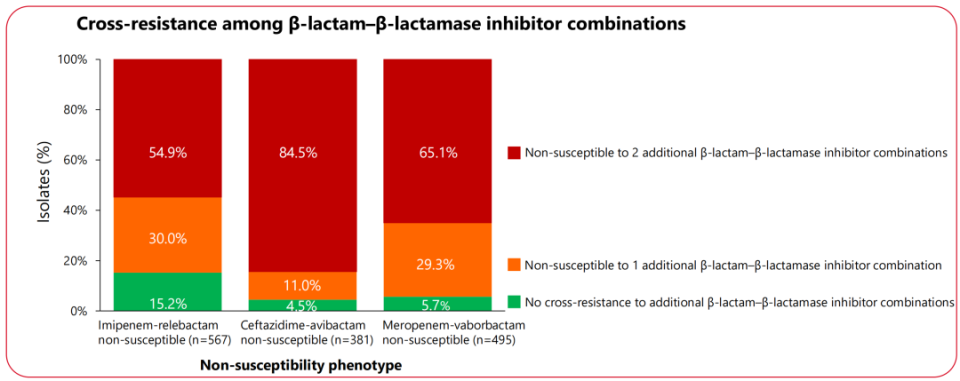
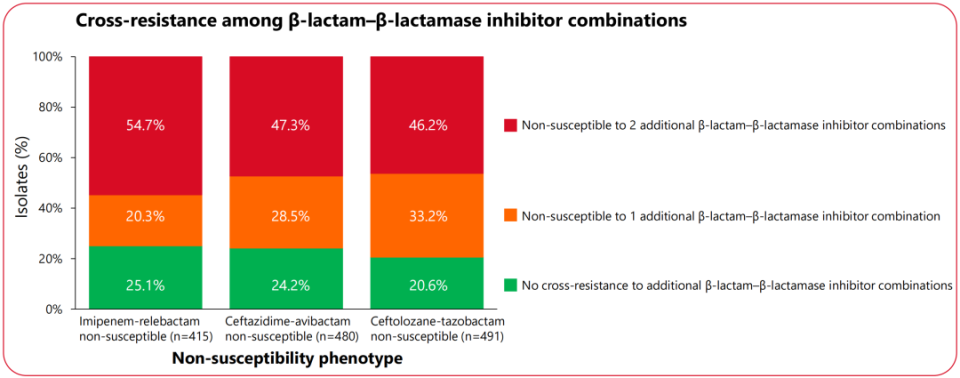
△2020-2024年欧美国家新型BL/BLI不敏感的肠杆菌目细菌(上)和铜绿假单胞菌(下)的交叉耐药
新型BL/BLI不敏感的肠杆菌目细菌和铜绿假单胞菌对新型铁载体头孢菌素头孢德罗均保持较高的敏感性,无论采用美国CLSI、FDA折点还是欧洲EUCAST折点。根据CLSI/FDA折点,亚胺培南-西司他丁-瑞来巴坦、美罗培南-韦博巴坦、头孢他啶-阿维巴坦不敏感的肠杆菌目细菌对头孢德罗的敏感性分别高达92.4%、91.5%和86.6%;根据CLSI折点,亚胺培南-西司他丁-瑞来巴坦、头孢他啶-阿维巴坦、头孢洛生-他唑巴坦不敏感的铜绿假单胞菌对头孢德罗的敏感性分别高达94.9%、94.0%和93.3%。
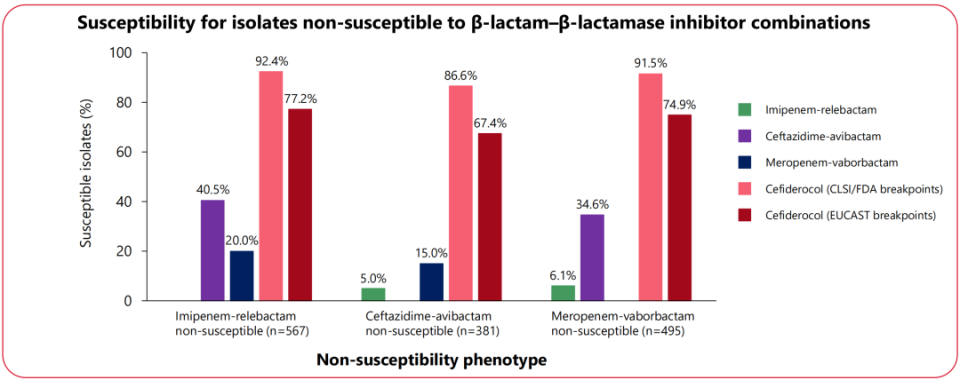
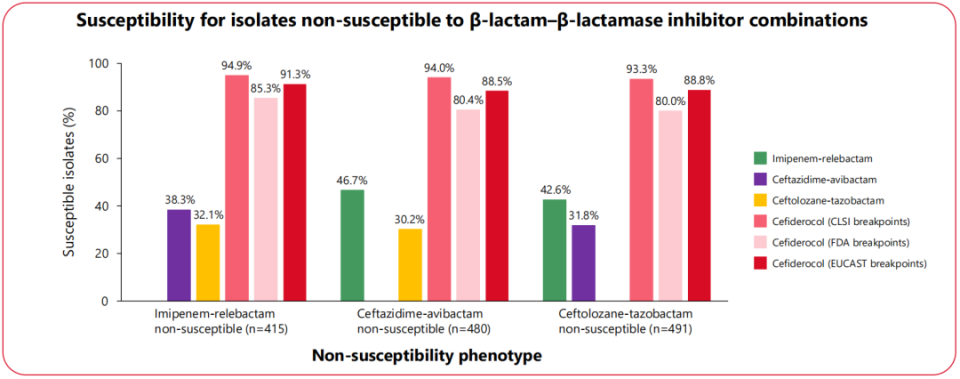
△新型BL/BLI不敏感的肠杆菌目细菌(上)和铜绿假单胞菌(下)分离株对头孢德罗的敏感性
这项大样本的SENTRY监测数据显示,在欧美国家新型BL/BLI不敏感的革兰阴性菌分离率目前仍很低,但其分离率呈上升趋势,而且在不同BL/BLI之间存在明显的交叉耐药,但与头孢德罗之间几乎没有交叉耐药。
本次IDWeek大会同时报道了PROVE研究(真实世界研究)的一项亚组分析数据,证实头孢德罗对新型BL/BLI不敏感的革兰阴性菌感染有良好的临床疗效[9]。
头孢德罗治疗BL/BLI敏感或不敏感革兰阴性菌感染均有较高的临床治愈率
PROVE研究(真实世界研究)显示:新型BL/BLI敏感的细菌,头孢德罗的敏感率为94.9%(75/79);新型BL/BLI不敏感的细菌,头孢德罗的敏感率为90.6%(281/310)。与BL/BLI敏感菌感染患者相比,敏感菌感染患者接受头孢德罗治疗时病情严重的患者的比例更高(重症监护室住院的患者更多:67.2% vs 52.6%;接受器官功能支持的患者更多:51.6% vs 39.8%),头孢德罗治疗BL/BLI敏感和不敏感细菌感染患者的临床治愈率相似(70.5% vs 70.2%)。这些真实世界研究的数据进一步证明了SENTRY的药敏结果。
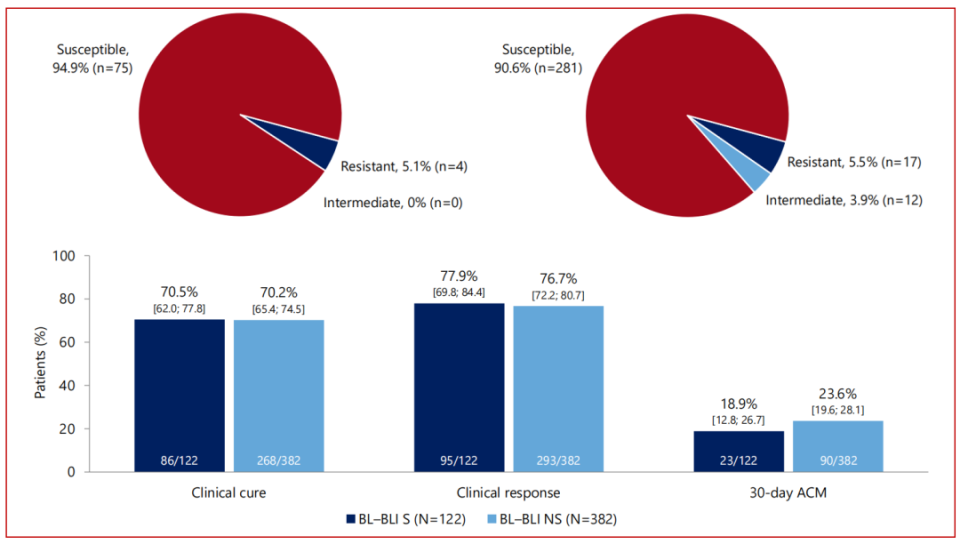
△PROVE研究:新型BL/BLI敏感(左上)或不敏感(右上)细菌对头孢德罗的敏感性,头孢德罗治疗新型BL/BLI敏感或不敏感(下)细菌感染的临床疗效。
注:临床治愈(Clinical cure)定义为治疗结束时感染体征和症状的消失或改善,且无后期复发或死亡的证据;临床缓解(Clinical response)定义为治疗结束时感染体征/症状的消失或改善,不包括治疗期间死亡的患者;全因死亡(All-cause mortality)为住院期间死亡的患者。
03
临床治疗应用时机
真实世界研究显示早期启动头孢德罗经验治疗的患者临床预后更好
“细菌-宿主-抗菌药物”的铁三角关系,是临床抗感染治疗决策的重要考虑因素。CRO抗感染治疗面临重重困境,CRO感染在重症监护患者、器官移植患者和骨髓移植患者等重症和免疫低下患者较常发生,且以医院获得性肺炎/呼吸机相关肺炎(HAP/VAP)、血流感染(BSI)、复杂性尿路感染(cUTI)等难治性感染类型常见。对于存在CRO感染高危因素的重症和免疫低下的患者,宜尽早启动经验性抗菌治疗。
本次大会上,报道了真实世界PROVE研究的多个亚组分析,一方面证实了头孢德罗在不同CRO病原体、不同感染类型的临床疗效基本相似,另一方面显示了早期启动经验性治疗的临床获益。
新型BL/BLIs敏感和不敏感细菌感染人群的疗效
在新型BL/BLI敏感细菌感染人群中,与头孢德罗挽救治疗的患者相比,经验性治疗的患者临床治愈率更高(84.6% vs 54.5%)。在BL/BLI不敏感细菌感染人群中[10],同样经验性治疗比挽救治疗的临床治愈率也更高(65.8% vs 60.0%);在BL/BLI不敏感细菌感染人群中,培养采集后5~7天启动头孢德罗治疗的临床治愈率为68.3%,>7天启动头孢德罗治疗的临床治愈率为67.4%,0~2天启动头孢德罗治疗的临床治愈率为71.7%,3~4天启动头孢德罗治疗的临床治愈率为75.0%,早期启动头孢德罗治疗的患者,临床治愈率更高。
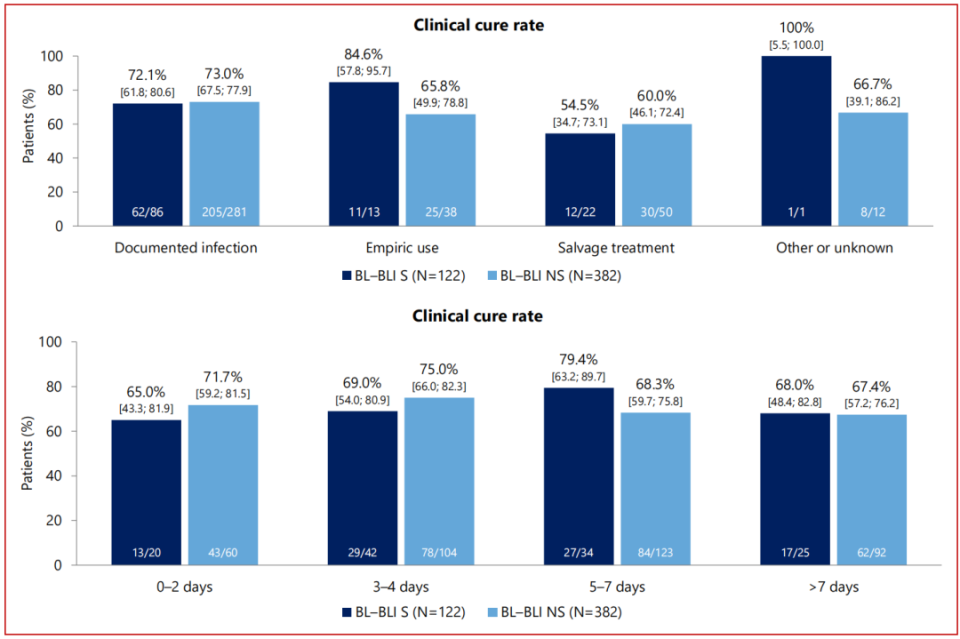
△确诊治疗/经验治疗/挽救治疗/其他治疗使用头孢德罗(上)以及采集样本培养后不同时间启动头孢德罗治疗(下)的临床治愈率
美国感染患者人群亚组分析
真实世界PROVE研究的美国感染患者的亚组数据[11],共纳入了508例感染患者,其中57.3%为ICU患者,47.6%为接受器官功能支持治疗的患者,其中93.3%的患者至少有一个感染CRO的危险因素,最常见的感染是呼吸道感染(53.5%)。
该患者人群使用头孢德罗治疗,临床治愈率、临床缓解率、30天全因死亡率分别为70.1%、77.8%和20.7%;值得注意的是,与头孢德罗挽救治疗相比,头孢德罗经验性治疗的临床治愈率更高(73.7% vs 54.3%)、临床缓解率更高(80.7% vs 68.6%),30天全因死亡率更低(14.0% vs 30.0%)。另外,该亚组分析还显示,在呼吸道感染患者中使用其临床痊愈率、临床缓解率和30天全因死亡率分别为64.7%、76.5%和25.7%。肠杆菌目细菌和铜绿假单胞菌感染患者的临床治愈率分别为79.3%和70.4%,30天全因死亡率分别为17.2%和20.4%。
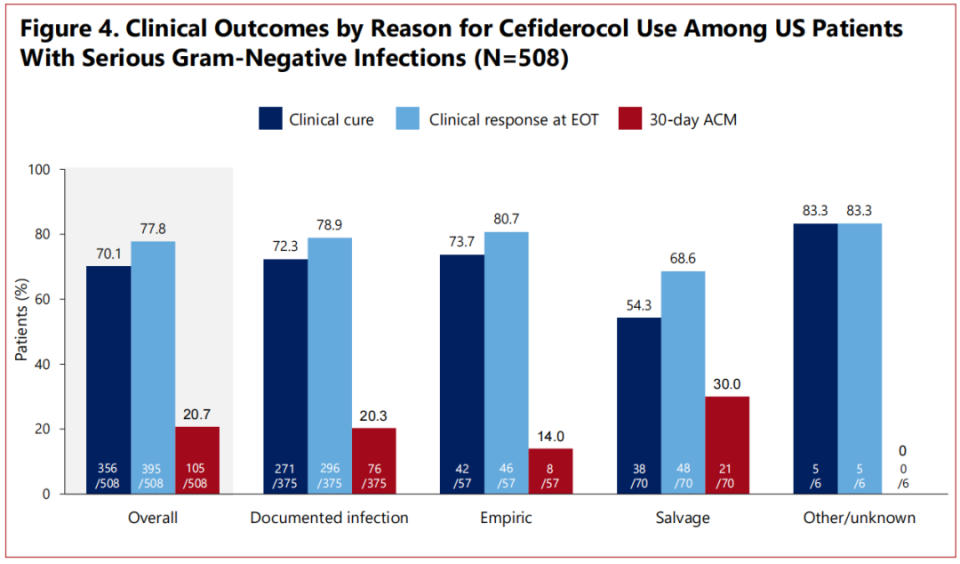
△美国感染患者人群数据:不同时机使用头孢德罗治疗患者的临床治愈率、临床缓解率和30天全因死亡率
血流感染(BSI)患者人群亚组分析
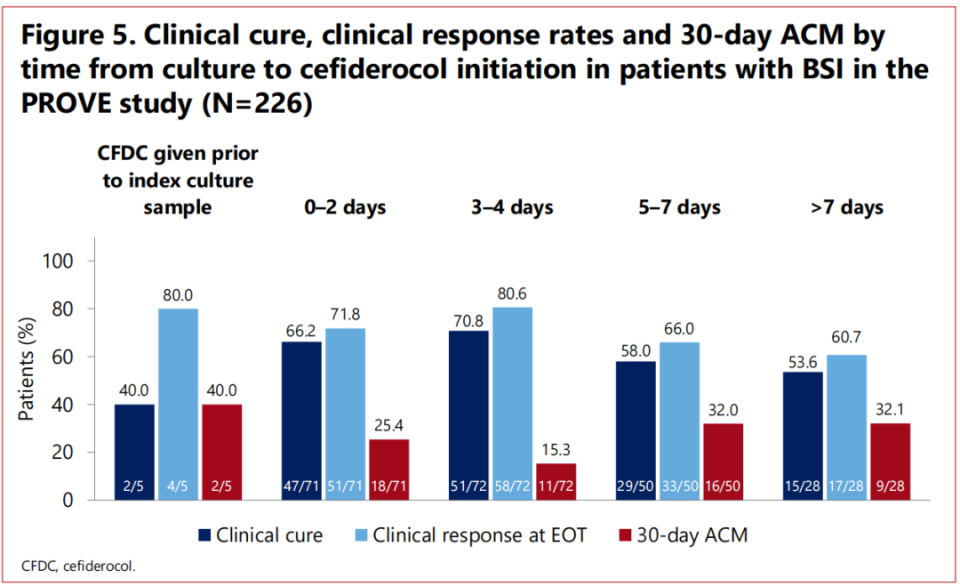
该研究[12]共纳入226例血流感染患者(其中原发感染47.8%),超过一半(55.3%)的患者来自ICU,近一半(46.0%)的患者接受了器官支持治疗。较为常见的病原体是:铜绿假单胞菌(35.8%)、鲍曼不动杆菌(20.8%)和肠杆菌目细菌(20.8%);其中有89.9%(179/199)的分离株对碳青霉烯类抗生素不敏感。
研究结果显示,在采集培养标本后的3-4天启动头孢德罗治疗的临床治愈率高于≥5天启动头孢德罗治疗的患者,其全因死亡率则更低(15.3% vs 32.1%)。另外,亚组分析还指出,BSI患者的总体临床治愈率为63.7%,30天全因死亡率为24.8%。头孢德罗经验性治疗患者的临床治愈率高于挽救治疗的患者,30天全因死亡率低于挽救治疗。
本次IDWeek大会报道了感染领域的最新研究,SENTRY体外监测数据显示,新型BL/BLI目前仍保持很强的抗菌活性,耐药率低。但新型BL/BLI不敏感的革兰阴性菌,在不同新型BL/BLI之间存在明显的交叉耐药,而与头孢德罗几乎无交叉耐药。PROVE研究证实了头孢德罗用于新型BL/BLI不敏感的细菌感染仍可取得较好的临床疗效,而且在不同感染类型、不同患者人群中的更多亚组分析显示,尽早启动头孢德罗经验性治疗的患者相较于挽救治疗的患者,其疗效和生存预后更好。希望有更多新型抗菌药物在国内上市,改善CRO感染患者的预后,也期待有更多基于中国患者人群的CRO感染治疗的真实世界研究,为临床应用提供更多指导。
参考文献
[1]《CHINET 2025年上半年细菌耐药监测结果》.www.chinets.com
[2]Wang M, Ge L, Chen L, et al. Clinical Outcomes and Bacterial Characteristics of Carbapenem-resistant Acinetobacter baumannii Among Patients From Different Global Regions. Clin Infect Dis. 2024;78(2):248-258. doi:10.1093/cid/ciad556.
[3]Reyes J, Komarow L, Chen L, et al. Global epidemiology and clinical outcomes of carbapenem-resistant Pseudomonas aeruginosa and associated carbapenemases (POP): a prospective cohort study. Lancet Microbe. 2023;4(3):e159-e170. doi:10.1016/S2666-5247(22)00329-9
[4]Castanheira M, Doyle TB, Kantro V, Mendes RE, Shortridge D. Meropenem-Vaborbactam Activity against Carbapenem-Resistant Enterobacterales Isolates Collected in U.S. Hospitals during 2016 to 2018. Antimicrob Agents Chemother. 2020;64(2):e01951-19. Published 2020 Jan 27. doi:10.1128/AAC.01951-19
[5]Heo YA. Imipenem/Cilastatin/Relebactam: A Review in Gram-Negative Bacterial Infections. Drugs. 2021;81(3):377-388. doi:10.1007/s40265-021-01471-8
[6]Wi YM, et al. Activity of Ceftolozane-Tazobactam against Carbapenem-Resistant, Non-Carbapenemase-Producing Pseudomonas aeruginosa and Associated Resistance MechanismsAntimicrob Agents Chemother. 2017 Dec 21;62(1):e01970-17
[7] Dobias J, Dénervaud-Tendon V, Poirel L, Nordmann P. Activity of the novel siderophore cephalosporin cefiderocol against multidrug-resistant Gram-negative pathogens. Eur J Clin Microbiol Infect Dis. 2017;36(12):2319-2327. doi:10.1007/s10096-017-3063-z
[8] Shortridge D, Streit JM, Mendes R, Castanheira M. In Vitro Activity of Cefiderocol against U.S. and European Gram-Negative Clinical Isolates Collected in 2020 as Part of the SENTRY Antimicrobial Surveillance Program. Microbiol Spectr. 2022;10(2):e0271221. doi:10.1128/spectrum.02712-21
[9]DeJonge B L M, et al. β-Lactam–β-Lactamase Inhibitor Combinations Show a High Degree of Cross-Resistance in Gram-Negative Bacteria, but Not to Cefiderocol. Results from the SENTRY Antimicrobial Surveillance Program (2020–2024). IDWeek 2025; Abstract 627.
[10]Shields R K, et al. Outcomes of Patients Treated With Cefiderocol For Infections Caused by β-Lactam–β-Lactamase Inhibitor Non-Susceptible Bacteria: Subgroup Analysis of the PROVE Study. IDWeek 2025; Abstract 1354.
[11Clancy C J, et al. Earlier Cefiderocol Use Was Associated with Better Outcomes for Challenging Gram-Negative Bacterial Infections: US Results From the Global Observational PROVE Study. IDWeek 2025; Abstract 1353.
[12]Drwiega E, et al. Clinical Outcomes of Cefiderocol for Treatment of Bloodstream Infections Caused by Gram-Negative Bacteria: Subgroup Analysis of the PROVE Study. IDWeek 2025; Abstract 1352.

俞云松 教授
感染病学教授、主任医师
浙江大学求是特聘教授、博士研究生导师
浙江省卫健委领军人才
浙江大学医学院附属邵逸夫医院感染病学科带头人
中国医药教育协会感染疾病专业委员会名誉主任委员
中华医学会细菌感染与耐药防治专业委员会候任主任委员
浙江医学会细菌感染和耐药防治专业委员会主任委员
国家卫健委抗菌药物合理应用和耐药评价专业委员会副主任委员
浙江省微生物技术与生物信息研究重点实验室主任
中华预防医学会医院感染控制委员会常务委员
中华医学会感染病学分会常务委员
浙江省预防医学会医院感染控制专业委员会主任委员
浙江省医学会感染病专业委员会副主任委员
以第一作者和通讯作者发表SCI收录论文145篇
连续四年入选爱思唯尔“中国高被引学者”(2021-2024年)
先后主持国家自然科学基金10项(重点项目2项、国际合作1项、区创项目1项)
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
