- 首页 > 正文
3rd One Health丨陈云波教授:当艰难梭菌走出医院:One Health揭示的隐藏传播网络
感染医线 发表时间:2025/11/6 18:17:37

编者按:艰难梭菌感染(Clostridioides difficile infection,CDI)是由肠道正常菌群破坏后,产毒素艰难梭菌过度增殖并释放毒素引起,以腹泻为主要表现的感染性疾病,临床表现可从轻度自愈性腹泻到严重的伪膜性肠炎、脓毒综合征、中毒性巨结肠甚至肠穿孔,其曾长期被视为典型的医院内感染问题,然而近年来,其流行病学特征发生显著变化,社区相关性感染日益增多。在近期举行的第三届One Health微生物耐药控制大会上,浙江大学医学院附属第一医院陈云波教授在报告中,从“One Health”视角系统阐述了艰难梭菌在医疗机构、社区家庭、农业食品链及自然环境中的传播网络,揭示了其跨区域、跨物种传播的复杂机制,并提出了多部门协同防控的策略方向。
艰难梭菌问题的演变
艰难梭菌(Clostridioides difficile,CD)是一种专性厌氧的革兰阳性芽孢杆菌,属于人体肠道正常菌群的一部分。当肠道菌群因抗菌药物使用等原因遭到破坏后,产毒素的艰难梭菌过度增殖并释放毒素,引发艰难梭菌感染。其主要临床表现为腹泻、发热、腹痛,严重者可发展为暴发性CDI、伪膜性肠炎、中毒性巨结肠甚至死亡。CDI的诊断包括临床诊断和确诊病例,前者需符合危险因素与临床表现并排除其他肠道疾病,后者需结合内镜检查或病原学证据。
传统上,CDI被认为是一个典型的“医院内”问题。其经典危险因素包括抗菌药物使用、高龄、免疫抑制、质子泵抑制剂(PPI)使用及长期住院等,这些危险因素形成了以“感染源-传播途径-易感宿主”为核心的三角流行病学模式。然而,近年来这一认知正发生根本性转变。荷兰的研究显示,医院相关性CDI病例已降至50%以下;美国明尼苏达州的数据进一步表明,社区获得性CDI占比超过50%,医院相关性CDI的比例进一步压缩[1-2]。这一变化提示,CDI正在“走出医院”,成为更广泛的公共卫生问题。
随着社区相关性CDI病例的显著上升,一个关键问题浮现:那些没有传统感染危险因素的感染者,究竟从何而来?这一问题亟待从更广阔的视角进行探索。在此背景下,“One Health”理念为我们提供了重要的分析框架。该理念强调人、动物与环境健康的互联互通,主张采用跨学科、跨部门的视角应对复杂健康问题。在关注院内感染的同时,必须将社区感染纳入整体防控体系,才能全面理解并有效遏制CDI的传播[3]。
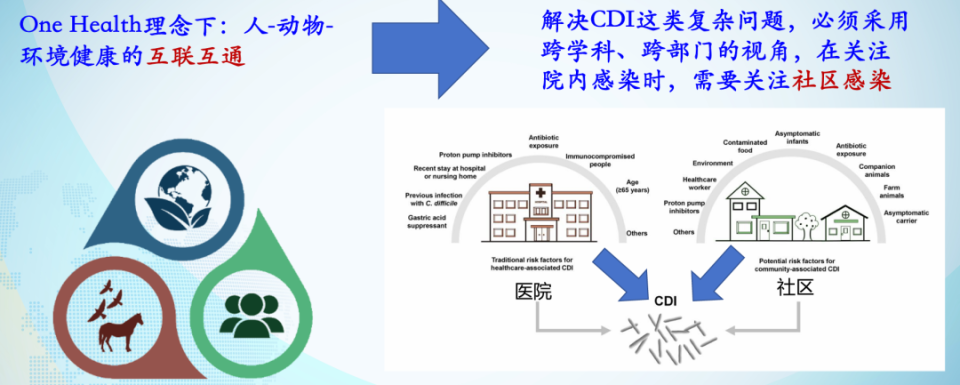
图1. “One Health”的透镜
(引自讲者会议幻灯)
艰难梭菌的隐形世界
在One Health的透镜下,艰难梭菌的传播网络可概括为四大枢纽:医疗机构作为“放大器”、社区与家庭作为“隐秘桥梁”、农业与食品链作为“潜在源头”,以及自然环境作为“最终的汇与源”[4]。这些枢纽相互连接,构成了复杂而隐蔽的传播循环。
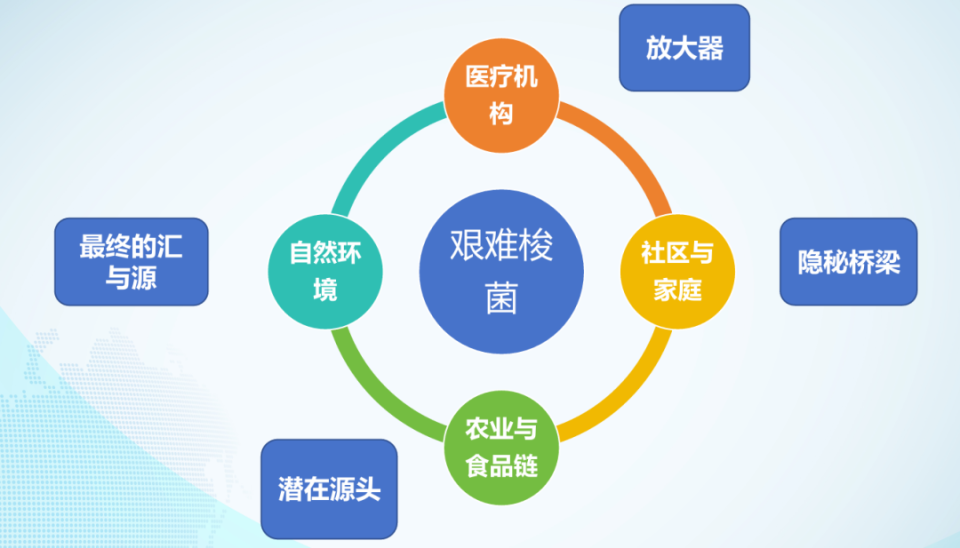
图2. 艰难梭菌传播网络的四大枢纽
(引自讲者会议幻灯)
医疗机构是CDI传播的关键放大器
医院环境中易感人群高度集中,包括手术患者、免疫低下者及长期住院患者,且抗菌药物使用频繁,医疗操作和护理活动增加了传播风险。
研究表明,抗菌药物使用天数与CDI发生率之间存在显著关联,抗菌药物的选择性压力是驱动CDI发生的核心因素;其中,GyrA的Thr82→Ile突变不仅介导了对氟喹诺酮类药物的耐药性,更赋予菌株显著的适应性优势,通过修饰DNA旋转酶并协同上调其他生命进程,推动其适应性进化[5-7]。
此外,无症状携带者作为“移动的储存库”出院,将耐药菌株带入社区,成为新的传播源。美国家庭传播研究显示,近期有家庭成员住院的家庭,其CDI发病率显著高于无暴露家庭[8]。
社区与家庭构成了连接人与环境的隐秘桥梁
人类通过日常活动连接动物、食物与环境,驱动整个传播网络的运行。在社区中,部分核糖体型如RT002、RT005、RT014等更为流行。与医院相关性菌株相比,社区相关性菌株对四环素、克林霉素、红霉素等药物的耐药性较弱[9]。
宠物作为人兽共患的潜在来源受到关注,全球多国研究显示,犬、猫等宠物中艰难梭菌携带率在4%至17%之间,其中50%至70%为产毒素菌株,腹泻宠物中携带率可达25%[10]。这些研究数据来自美国、巴西、德国、瑞典、瑞士、印度、尼日利亚、马拉维、加拿大等地,表明宠物在CDI传播中可能扮演重要角色。
农业与食品链是艰难梭菌的潜在源头
在农场动物中,艰难梭菌的流行呈现明显的动态分布特征,存在显著的种属差异,分离率高低不一,流行情况随动物生长阶段变化,并具有一定的时间聚集性,随季节更替而波动。跨国研究显示,艰难梭菌已从多国宠物及动物中分离得到。基因分析进一步揭示,这些散布于不同国家的动物源菌株间存在显著的系统发育相关性[11]。此外,分析显示,人源与动物源菌株在进化上高度接近,提示存在跨物种传播[12-13]。
自然环境是艰难梭菌的最终汇与源
艰难梭菌芽孢具有强大的环境抵抗力,其生命周期包括营养细胞、芽孢起始、不对称分裂、皮质合成、外壳组装及母细胞裂解等多个阶段。芽孢的结构使其能够抵抗热、乙醇、酶和化学损伤,在环境中长期存活。
研究表明,从污水处理厂至再生灌溉水等多种水体中均可分离出具有遗传相关性的艰难梭菌;基于基因组溯源分析,发现从犬类、自然环境中分离的艰难梭菌菌株之间,存在显著的基因组重叠,这一发现为揭示其跨宿主传播路径与生态适应性提供了关键分子证据[14-15]。
城市环境,如公园与公共绿化带,也成为其传播的“混合器”。在西澳大利亚的研究中,公园土壤中艰难梭菌的分离率在绿地规模、区位、季节及新旧属性等维度上无显著差异,老草坪为47%,新草坪为65%,不同面积和区域的分离率在49%至62%之间,南北区位及秋冬季节的分离率也较为接近[16]。多项研究证实,城市各类绿地中的艰难梭菌菌株具有相似性,共同指向其作为传播混合器的角色[17]。
基于One Health框架,可以清晰地看到艰难梭菌的多元传播循环:肠道内的定植与产毒、芽孢通过粪便排放至环境、在环境中存活与传播、通过食物链或直接接触再次进入人体或动物体。这一循环受到人口增长与流动、多药并用、饮食结构、抗菌药物不合理使用、耐药性增加等多种因素的驱动,构成了一个复杂的生态系统[18]。
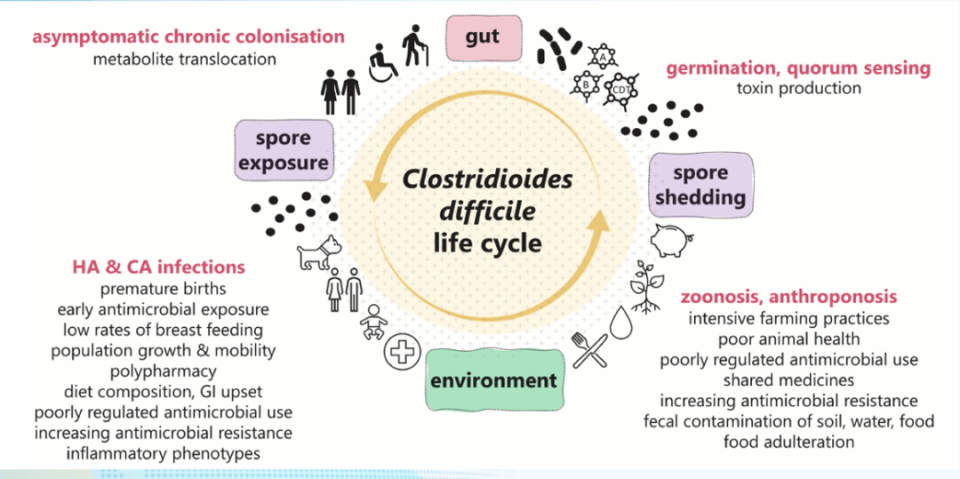
图3. One Health框架下的艰难梭菌传播网络图
(引自讲者会议幻灯)
如何应对艰难梭菌
应对艰难梭菌的传播,必须依靠精准的溯源工具与多部门协同的策略。分子流行病学为揭示传播链提供了关键技术支持。目前主要方法包括基于SNP的分析,如Snippy、CFSAN ParSNP,适用于高分辨率溯源,特别是医院内暴发和短周期疫情的精确追踪;基于cgMLST的方法,如EnteroBase、chewBBACA,适用于中长期监测与全球比对,结果标准化便于实验室间比较;基于k-mer的工具,如PopPUNK、SKA,适用于大规模初步筛查,快速分群锁定暴发集群。这些工具共同构成了“侦探的工具箱”,助力揭示隐藏的传播网络。
表1. 侦探的工具箱:分子流行病学

(引自讲者会议幻灯)
应用这些工具,多项研究成功揭示了艰难梭菌的跨物种传播路径。系统发育分析显示,不同国家的人源与动物源菌株在进化上具有高度亲缘关系。例如,ST11谱系在全球范围内实现了多次跨大陆的社区性克隆传播,其庞大的泛基因组携带丰富的耐药基因与噬菌体,驱动了这一具有One Health意义的克隆崛起[19-20]。
针对RT146菌株的研究发现,2015-2016年人源菌株与2012年猪源菌株为同一克隆,SNP差异≤2,且环境与猪源菌株的传播距离最远达200公里[21]。k-mer分析进一步表明,srtB基因在ST37的进化中扮演关键角色,该基因编码一种由SrtB酶锚定的胶原蛋白结合黏附素,增强了菌株的环境适应能力[22]。
对宠物、农场与患者之间传播链条的研究也证实,犬源菌株与当地人源株遗传相近,cgMLST等位基因差异数较小;ST35菌株在四院多场中存在跨宿主克隆传播;养殖场环境、养殖人员与患者之间形成了完整的传播链[3-25]。英国一家医院及水源分离株的系统进化树显示,临床分离株与废水分离株分布紧密,进一步证实环境在传播中的作用[26]。
耐药性的One Health循环同样不容忽视。抗菌药物的不合理使用,不仅在医疗机构,也在畜牧业中驱动了耐药菌株的产生与扩散,并通过环境完成循环。系统发育分析表明,四环素耐药性正驱动艰难梭菌RT078等谱系的克隆扩张与全球传播,其选择压力是导致该病原体出现及沿食物链扩散的关键因素[27]。
艰难梭菌作为One Health概念下的病原体,唯有协同才能应对
面对艰难梭菌的传播挑战,我们面临多重困境:临床医生对社区获得性CDI认知不足,诊断率低;系统监测网络尚未完善,缺乏整合人‑动物‑环境数据的主动监测体系;单一部门的干预措施效果有限,存在明显的短板效应。
为有效应对,必须建立多部门联合的协同机制。医疗机构应强化抗生素管理,识别和管理无症状携带者,并改进终末消毒,尤其关注芽孢的清除。疾控系统需建立整合人-动物-环境的主动监测网络,将CDI纳入食源性疾病监测体系,并开展基于精准溯源的调查研究。环境与农业部门应加强养殖业抗生素监管,研究优化污水处理工艺以有效去除病原体,并评估农业用水和有机肥料的生物安全风险。最终,应建立常态化的“CDI One Health工作组”,定期共享数据、评估风险、协调行动,实现从“单兵作战”到“联合作战”的转变。
结语
艰难梭菌已成功“走出医院”,其传播是一个典型的One Health问题。我们揭示了一个由医疗机构、社区、农业食品链和自然环境构成的复杂、隐藏的传播网络。任何单一领域的努力都无法切断这个网络,碎片化的应对注定失败。应对艰难梭菌的挑战,没有“他们”的问题,只有“我们”的共同责任。让我们携手,用One Health的智慧,关闭这个隐藏的传播网络。



参考文献
[1] https://www.health.state.mn.us/diseases/cdiff/statistics.html
[2] Open Forum Infect Dis 2019; 6(12): ofz501.
[3] Clin Infect Dis. 2025;80(1):37-42.
[4] Foods. 2024;12(5):1094.
[5] Nat Genet. 2013;45(1):109-13.
[6] JAMA Network Open. 2025;8(8):e2525252.
[7] J Antimicrob Chemother. 2019;74(4):877-884.
[8] Emerg Infect Dis. 2022;28(5):932-939
[9] APMIS. 2022;130(11):661-670.
[10] Expert Rev Anti Infect Ther. 2021;19(12):1543-1552
[11] Adv Exp Med Biol. 2024;1435:273-314.
[12] Emerg Microbes Infect. 2024;13(1):2427804.
[13] Emerg Infect Dis. 2021;27(9):2294-2300.
[14] Microbiol Spectr. 2023;11(1):e0358222.
[15] Microb Genom. 2023;9(6):mgen001046
[16] Sci Rep. 2017;7:41196.
[17] Environ Microbiol Rep. 2020;12(6):672-680.
[18] Hyg Environ Health Adv. 2024; 12: 100108
[19] BMC Vet Res. 2024;20(1):479.
[20] mBio. 2019;10(2):e00446-19.
[21] PLoS One. 2020;15(12):e0244227
[22] BMC Genomics 2025; 26(1): 659
[23] Anaerobe. 2021;67:102317.
[24] Emerg Microbes Infect. 2024;13(1):2408322.
[25] Emerg Microbes Infect. 2021;10(1):2244-2255.
[26] MicrobGenom. 2018;4(3):e000162.
[27] mBio. 2019;10(2):e02790-18.

陈云波 教授
医学博士,主任技师
浙大一院传染病重症诊治全国重点实验室细菌学平台负责人
中华医学会感染病学分会第十二届委员会青年学组委员
中国医师协会感染科医师分会第五届委员会学组成员
中国初级卫生保健基金会病原检测专业委员会委员
浙江省预防医学会微生态专业委员会委员兼秘书
浙江省转化医学学会公共卫生与生物安全分会委员等
浙江省病原微生物实验室生物安全研究质量控制中心专委会委员等
从事感染性疾病的临床诊断;研究方向:艰难梭菌分子流行病学及致病机制。主持国家自然基金面上项目、国家科技重大专项等5项;主参“传染病防治”科技重大专项等5项;担任《Infectious Microbes & Diseases》、《国外医药抗生素分册》等的编委;近3年来,以第一或通讯作者累积发表SCI论文25篇,曾获三项浙江省科技进步二等奖。
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
