- 首页 > 正文
深三院结核之窗丨相分离赋能精准诊断!超灵敏呼吸道病毒检测技术破解低载量漏检难题
感染医线 发表时间:2025/12/26 18:23:19
编者按:在即时检测需求日益增长的今天,如何提升低病毒载量样本的检测灵敏度仍是生物医学领域的核心挑战。传统富集技术因操作复杂、通用性差等问题,难以适配快速、精准的诊断场景。本期“深三院结核之窗”栏目中,卢水华教授团队分享了一项研究,该研究介绍了一项创新性预富集方法——相分离辅助预富集(PSAP)技术,它通过巧妙调控双水相系统的界面性质,实现病毒抗原与核酸的高效同步富集。研究表明,该方法无需改造现有商业检测平台,即可显著提升多种呼吸道病原体的检测灵敏度。PSAP技术为突破低载量样本检测瓶颈提供了新思路,兼具高效性与兼容性,有望推动精准诊断技术的进一步发展。
研究简介
一、研究背景
在生物医学检测中,
当前主流诊断工具同样存在短板:快速抗原检测(RATs)虽操作简便、成本低,但病毒蛋白浓度不足时易漏检;金标准RT-qPCR需复杂样本处理才能达到检测阈值,难以满足去中心化诊断需求。为此,本研究提出相分离辅助预富集(PSAP)技术,核心目标是开发一种通用、高效、可直接集成于商业诊断平台的预富集方法,同时提升病毒抗原与核酸的检测灵敏度,解决低载量样本诊断难题。
研究内容
1. PSAP技术原理及操作流程
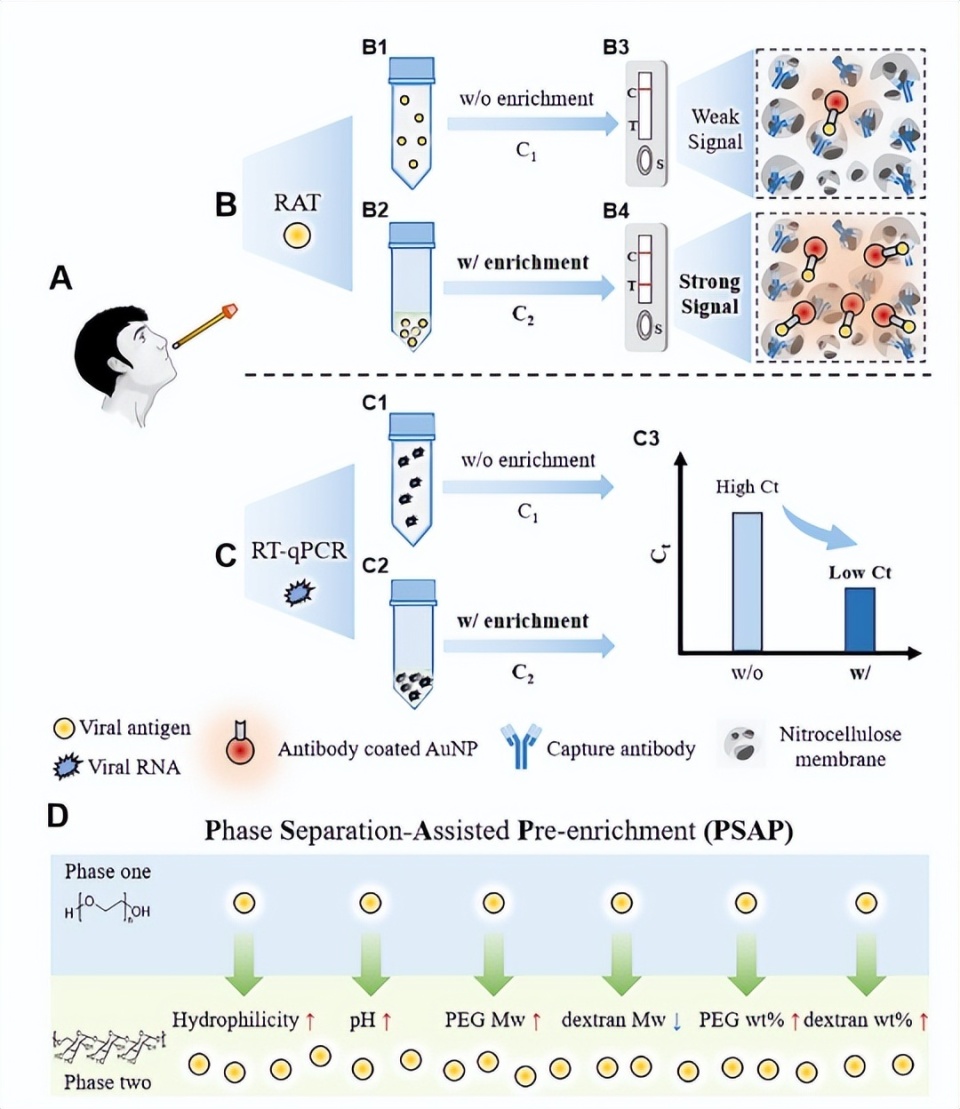
图1. PSAP技术用于富集病毒抗原及RNA
2. PSAP关键组份优化
为最大化富集效率与兼容性,研究对ATPSs体系进行了系统性优化:
ATPSs体系选择:对比PEG-葡聚糖、PEG-Ficoll、PEG-盐三种体系,发现PEG-葡聚糖体系对病毒核衣壳(N)蛋白的分配效率最高,原因是亲水的N蛋白与葡聚糖相的氢键相互作用更强。
界面化学调控:①pH值:pH7.4(接近生理环境)时,N蛋白与带负电的葡聚糖间静电吸引力最强;②聚合物分子量:PEG分子量越高、葡聚糖分子量越低,抗原分配至葡聚糖相的比例越高;③质量分数:增加葡聚糖质量分数、降低PEG质量分数,可强化抗原富集偏好。
体积比优化:通过扩大PEG富集相(上相)与葡聚糖富集相(下相)的体积比,压缩下相体积实现二次富集:当体积比为50:1时,抗原富集倍数达47.7倍;体积比为59:1时,RNA富集倍数达44.51倍。
流动性能适配:为兼容RATs侧流条的毛细管流动,需控制葡聚糖浓度低于其重叠浓度(21.26%w/w),避免溶液粘度过高或膜孔堵塞,确保15分钟内液体覆盖整个检测条。
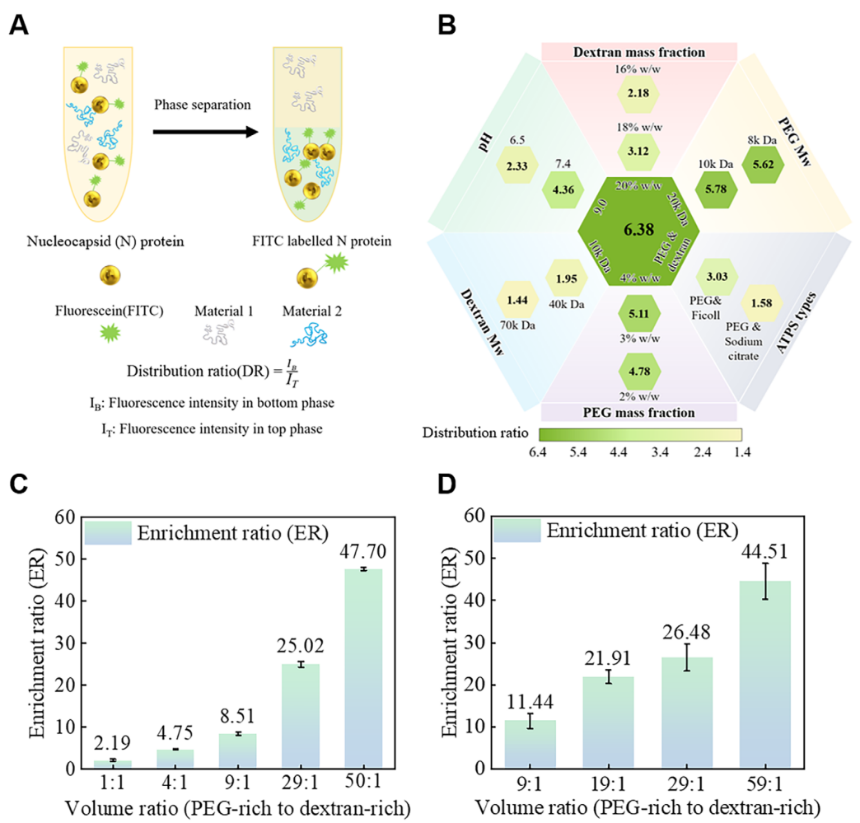
图2. 通过筛选ATPSs的组成和两相体积比来调节抗原富集
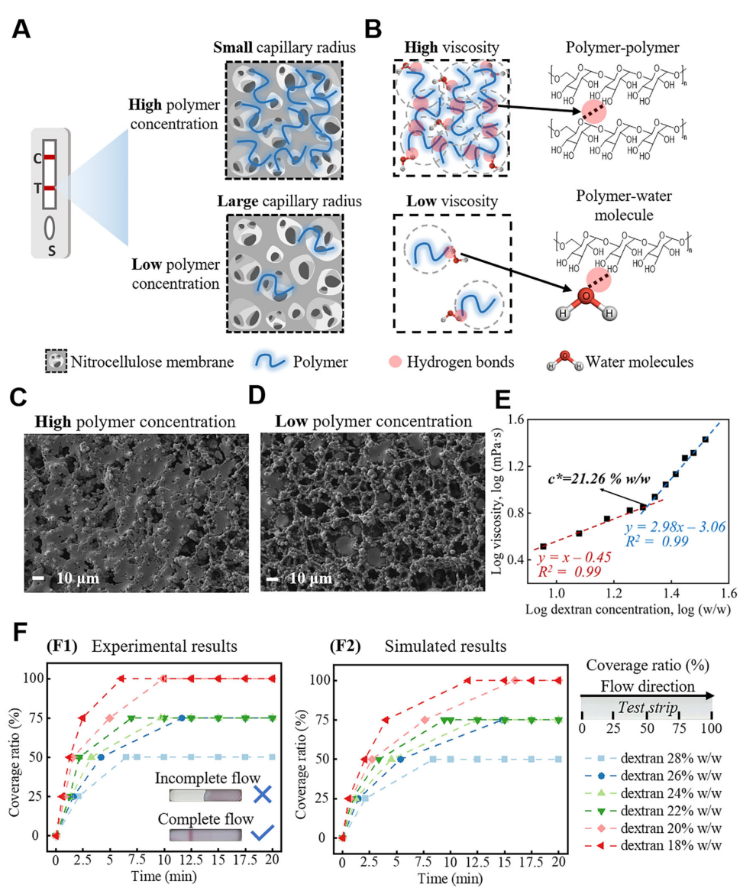
图3. 应用富集抗原于RATs条带时的流动性能优化
3. 商业诊断平台适配性验证及临床验证
PSAP技术可直接集成于现有商业RATs试剂盒,显著提升检测灵敏度:
针对SARS-CoV-2:在Genrui、Banitore、HighTop三种试剂盒中,检测下限(LOD)分别从80 pg/μL、400 pg/μL、200 pg/μL降至8 pg/μL、40 pg/μL、20 pg/μL,灵敏度均提升10倍。
针对流感A/B病毒:LOD提升5倍,如流感A病毒从200 pg/μL降至40 pg/μL,证实技术对多种呼吸道病毒的适用性。
对53份临床鼻咽拭子样本(40份RT-qPCR阳性,13份阴性对照)的检测结果显示:
抗原检测:低病毒载量组(27<Ct<31)中,传统RATs阳性率为0,而PSAP-RATs阳性率达50%;高载量组(Ct<27)阳性率从30%提升至90%。
RNA检测:PSAP-RT-qPCR在各载量组均优于传统方法,低载量组(27<Ct<31)阳性率从43.75%提升至62.5%,高载量组从60%提升至100%。
特异性:在高Ct值样本(31<Ct<40)和阴性对照(Ct>40)中,PSAP方法未出现假阳性,保持了良好的特异性。
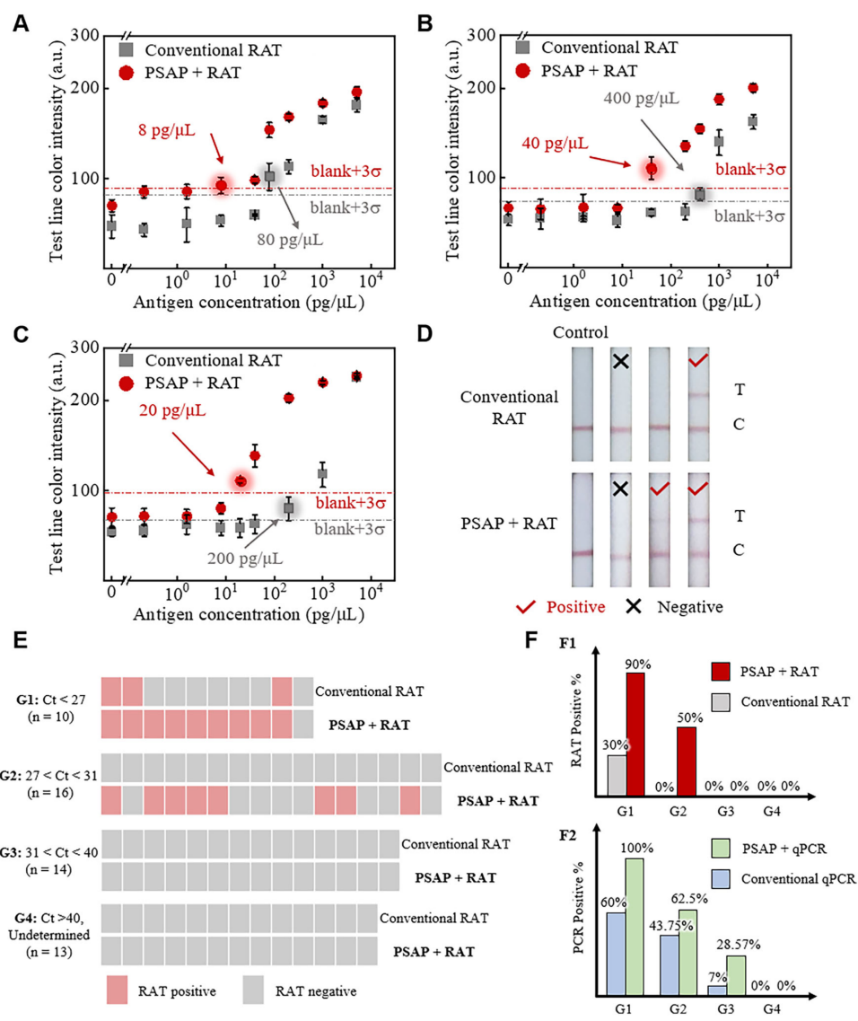
图4. PSAP方法在SARS-COV-2检测中的普适性与临床验证
4. PSAP检测的普适性验证
本研究进一步验证了PSAP检测其他病毒的潜力(如甲型/乙型流感病毒,图5)。采用与SARS-CoV-2相同的方案,发现甲型(图5A)和乙型(图5B)流感病毒的检出限均提升5倍。为解释流感病毒富集倍数较低的现象,通过液相色谱-质谱联用(LC-MS)分析不同抗原在同一ATPS中的分配(图5C)。根据抗原在上下相的峰面积比(图5D),SARS-CoV-2抗原的相亲和性比甲型/乙型流感病毒高4.5%(SARS-CoV-2的Ratio=0.93,甲型/乙型流感的Ratio=0.89),这源于聚合物-抗原界面相互作用的差异,导致富集效果不同。
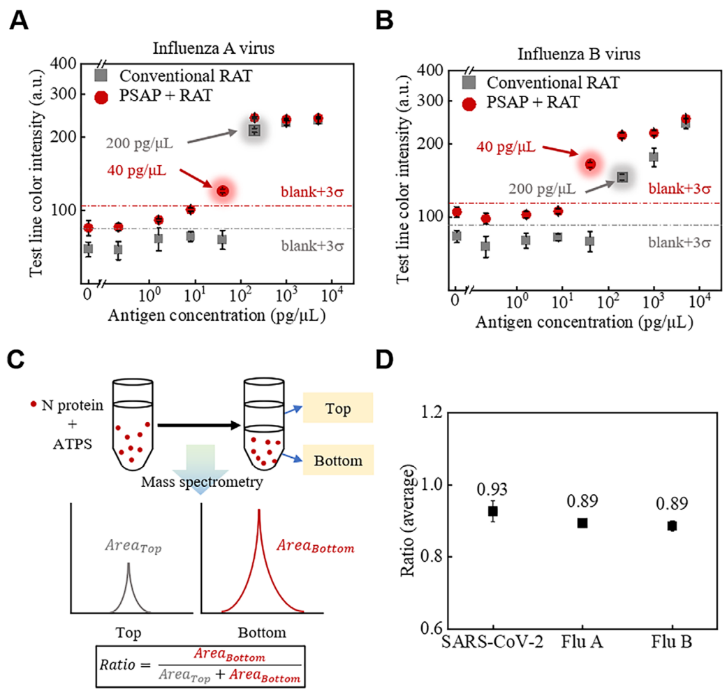
图5. PSAP方法检测甲/乙型流感病毒,及其与SARS-CoV-2的LC-MS定量比较分析
研究总结
1. PSAP技术通过可调谐双水相系统实现了病毒标志物的高效富集,对病毒抗原及RNA的富集率均能提高超过40倍。
2. 临床验证通过分析53份临床样本,证明PSAP能显著提高病毒抗原及RNA的检测准确性,尤其是针对低载量样本。
3. PSAP兼具通用性、简便性和兼容性,为解决呼吸道病原体检测中的灵敏度瓶颈提供了创新方案,为POCT的开发奠定基础。
研究点评
研究亮点
突破传统方法“单一标志物适配”的瓶颈,首次实现病毒抗原(47倍)与RNA(44倍)的同步高效富集,适用于SARS-CoV-2、流感A/B等多种呼吸道病原体。
无需改造现有商业诊断平台(RATs、RT-qPCR),可直接集成使用;采用低成本、商业化可得的聚合物(PEG、葡聚糖),符合工业规模化生产需求。
研究局限
PSAP对不同病毒的富集倍数存在差异(如流感病毒为5倍,SARS-CoV-2为10倍),需针对特定病原体优化ATPS参数;其次,高粘度聚合物可能延长快速抗原检测的反应时间(目前需15分钟,传统方法为10分钟);最后,临床样本中的复杂成分(如高浓度蛋白质)可能影响相分离效率,需进一步优化裂解液配方。
▌参考文献:
Cao Y, Lau PN, Chin AWH, et al. A Phase Separation-Assisted Pre-Enrichment Method for Ultrasensitive Respiratory Virus Detection. Adv Sci (Weinh). 2025 Sep;12(36): e06578. doi: 10.1002/advs.202506578.

更多精彩内容,请扫码订阅“深三院结核之窗”专栏

卢水华 教授
教授,主任医师,二级教授,博士生导师
国家感染性疾病临床医学研究中心副主任,深圳市第三人民医院肺病医学部主任

东亚娟
复旦大学病原生物学2023级博士研究生
主要研究方向:基于CRISPR技术分子诊断法的开发与应用。累计发表学术论文5篇,其中一作3篇,共同一作1篇(Nature communications)。参与多项国家级自然科学基金项目。
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
