- 首页 > 正文
B/F/TAF持续治疗的安全性好于转换为DTG/3TC,长效CAB+RPV转换为B/F/TAF则仍可保持高效抑制和高依从性
感染医线 发表时间:2025/12/3 22:47:45

编者按:随着抗反转录病毒治疗的不断发展,HIV管理已进入个体化与多元化的新阶段。如何在确保病毒学抑制的同时提升患者生活质量,成为临床关注的核心议题。在2025年10月19日至22日于亚特兰大召开的美国感染病周(IDWeek 2025)上,两项重要研究为比克替拉韦/恩曲他滨/丙酚替诺福韦(B/F/TAF)三药方案提供了新的循证支持:DYAD研究96周数据显示,与持续应用B/F/TAF相比,尽管转换为DTG/3TC可获得非劣效病毒学抑制,但并未减少不良反应,相反不良反应有所增加[1];EMPOWER研究证实从注射CAB+RPV治疗转换至B/F/TAF,仍可维持病毒学抑制,而且从长效治疗转换为B/F/TAF这种单片复方制剂口服方案后,感染者仍可保持高治疗满意度和依从性[2]。
01
DYAD研究96周结果
持续B/F/TAF治疗的安全性优于转换为DTG/3TC,且肾功能保持稳定
在随机DYAD研究中,研究者既往已证明,对于病情稳定的病毒学抑制成人患者,换用多替拉韦/拉米夫定(DTG/3TC)相较于继续使用比克替拉韦/恩曲他滨/丙酚替诺福韦(B/F/TAF),至第48周的疗效具有非劣效性[3]。DYAD的患者报告结局数据显示,换用DTG/3TC与继续使用B/F/TAF在症状负担和治疗满意度方面相似[4]。目前关于从B/F/TAF换用DTG/3TC的长期影响数据仍然有限。本文报告DYAD研究96周观察性延长期的真实世界疗效、安全性和持续用药情况。结果表明,与转换DTG/3TC相比,持续B/F/TAF治疗的不良事件更少,停药率更低。
DYAD(NCT04585737)是一项在病毒学抑制的成人中开展的开放标签随机临床试验。研究的主要终点是使用FDA快照算法在意向治疗人群中评估第48周时HIV-1 RNA≥50 c/mL的患者比例。研究结束时,获得受试者的知情同意,通过电子病历收集和报告截至第96周和第144周的病毒学疗效、安全性和持续用药情况。使用两样本t检验比较治疗组间在第96周时肌酐、肾小球滤过率、血脂参数、体重和BMI的平均变化。
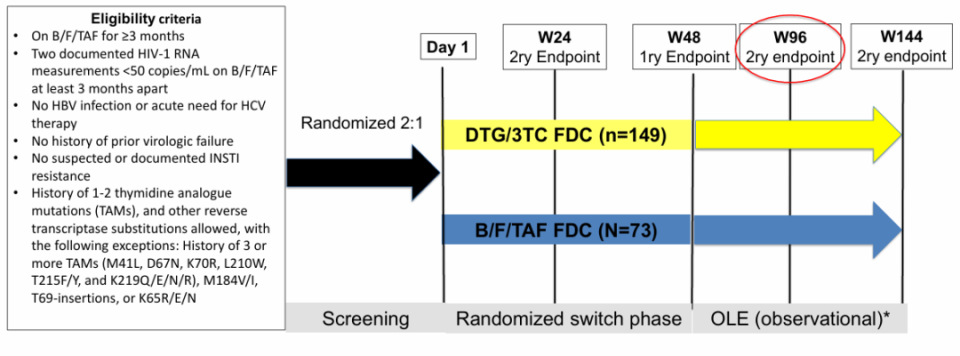
△DYAD研究方案
研究关键结果如下:
1. 病毒学抑制下实现平稳转换,B/F/TAF持续治疗疗效稳定
第48周时,DTG/3TC转换组134例和B/F/TAF持续组65例患者完成研究。其中,DTG/3TC转换组124例和B/F/TAF持续组63例患者同意参与观察性延长期。
第96周时,DTG/3TC转换组3例(2%)和B/F/TAF持续组1例患者(1%)出现HIV-1 RNA≥50 c/mL(调整后治疗差异0.6%,95%CI -4.6%至5.5%)。
表1. 96周研究结果

截至第96周,DTG/3TC转换组13例和B/F/TAF组6例患者符合确认的病毒学失败标准;DTG/3TC组2例和B/F/TAF组1例患者观察到耐药。在第48周至第96周期间,DTG/3TC组有1例受试者经历确认的病毒学失败,且未出现治疗引发的耐药证据。
2. B/F/TAF持续组的治疗持续性高于DTG/3TC转换组
治疗持续性方面,B/F/TAF持续组展现出更优的长期治疗稳定性:第96周时,B/F/TAF持续组80%的患者仍在继续原方案治疗,在数值上高于DTG/3TC转换组的75%。
表2.DTG/3TC与B/F/TAF治疗持续情况对比(至第96周)

3. DTG/3TC转换组24周不良事件增加20倍,96周增加5倍
在安全性方面,截至第24周,B/F/TAF持续组与DTG/3TC转换组中报告药物相关不良事件的受试者比例分别为1%和21%;至第96周,该比例分别为5%和28%。在整个研究期间,B/F/TAF持续组仅有少数症状的个案报告,如恶心、抑郁加重和失眠(均为1例),未见疲劳、腹泻、头痛、体重增加或头晕等不良反应。
DTG/3TC转换组中上述不良事件的发生率高于B/F/TAF持续组,报告的不良事件包括:分别为恶心(5%)、疲劳(4%)、腹泻(4%)、失眠(4%)、头痛(3%)、抑郁加重(2%)和头晕(2%)。
4. B/F/TAF持续组96周内没有药物相关不良事件导致的停药,DTG/3TC转换组为7%
此外,B/F/TAF持续组中无受试者因药物相关不良事件停药,而DTG/3TC转换组在第24周和96周因药物相关不良事件停药的比例分别为4%和7%。在严重不良事件方面,第96周时B/F/TAF持续组与DTG/3TC转换组药物相关严重不良事件的发生率分别为0%与0.7%,整体严重不良事件发生率分别为5%与9%。
表3. 第96周不良事件

5. B/F/TAF转换组肾功能稳定,DTG/3TC转换组eGFR有所下降
肾脏安全性方面,第96周时B/F/TAF转换组估算肾小球滤过率(eGFR)保持稳定(较基线升高1 mL/min/1.73m²),而DTG/3TC组eGFR有所下降(降低4.5 mL/min/1.73m²)。两组间其他代谢参数变化无显著差异。
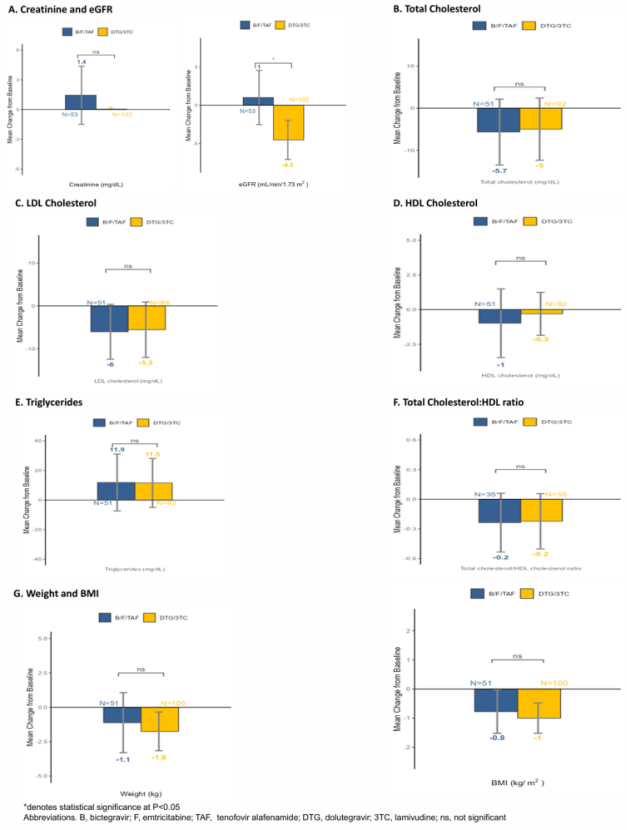
△第96周肾脏与代谢参数相对基线的平均变化
在DYAD研究96周观察性延长期中,尽管DTG/3TC在病毒学抑制下实现平稳转换,但B/F/TAF持续治疗在安全性和耐受性方面展现出显著优势。与DTG/3TC转换治疗相比,B/F/TAF持续治疗的药物相关不良事件发生率显著更低(5% vs 28%),并且全程无患者因药物相关不良事件而终止治疗(停药率:0% vs 7%)。此外,B/F/TAF组的药物相关副作用种类更少、发生率极低。
第96周时,两组间eGFR的平均变化持续存在差异,B/F/TAF持续治疗的eGFR保持稳定,而DTG/3TC转换治疗的eGFR有所下降。总体而言,这些长期数据表明,在B/F/TAF转换为DTG/3TC治疗时,需注意不良反应增加及治疗持续性降低的风险。
02
EMPOWER研究
长效CAB+RPV转换至B/F/TAF三药方案显著提升患者满意度并维持高效病毒学抑制[4]
长效注射用抗反转录病毒疗法的优势在于用药间隔长,减少HIV感染者反复往返医院,理论上可能更有助于提升感染者长期治疗的依从性和满意度。但真实世界中长效方案的应用仍面临诸多挑战,包括可及性、可支付性、注射部位反应等。部分使用卡替拉韦+利匹韦林(CAB + RPV)注射剂的患者因各种原因转回口服治疗方案。B/F/TAF是是基于新一代整合酶抑制剂(INSTI)联合两种强效核苷类反转录酶抑制剂(NRTI)的单片复方制剂,具有高效抑制病毒、高耐药屏障、安全性好、用药简便等治疗优势,已被国内外指南推荐并广泛应用于HIV感染者的初始和转换治疗。
EMPOWER(Evaluating Many PeOple With HIV aftER switching from CAB + RPV to B/F/TAF)是一项Ⅳ期、单臂、开放标签、前瞻性、多中心研究,旨在评估因不耐受、不良事件或个人偏好而停用CAB+RPV的病毒学抑制HIV感染者使用B/F/TAF的安全性、药代动力学和疗效。本研究目的包括评估(1)转换后的治疗满意度,(2)从CAB+RPV转换至B/F/TAF的原因,以及(3)了解HIV感染者对注射和口服治疗的体验。
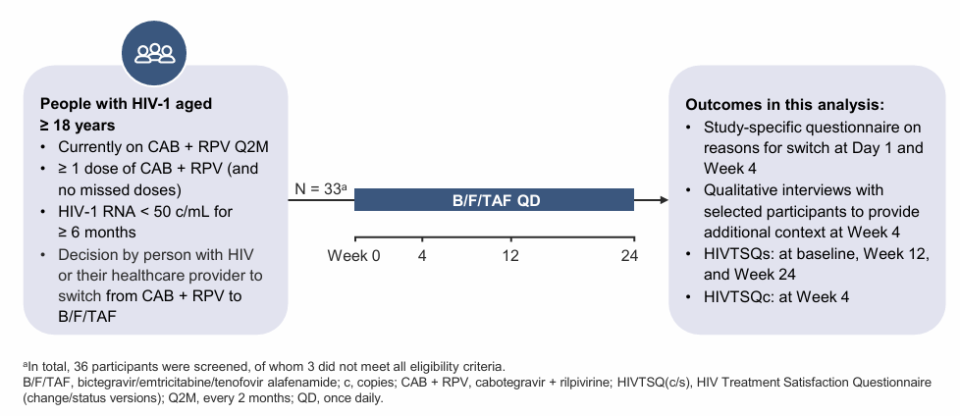
△EMPOWER研究设计
本分析报告了从CAB+RPV转换至B/F/TAF的受试者的治疗满意度和转换原因。受试者使用HIV治疗满意度问卷(HIVTSQ;变化版和状态版)自我报告治疗满意度。作为主要试验的一部分,对一小部分受试者进行了半结构化个体深度访谈,询问其决定停用CAB+RPV的原因。
研究关键结果如下:
1. B/F/TAF转换治疗24周病毒学抑制率100%
所有可获得数据的受试者均在第4周(n=32)、第12周(n=30)和第24周(n=29)实现HIV-1 RNA < 50 copies/mL(缺失数据被排除)。在可获得数据的受试者中,25/29(86%)截至第12周依从性≥95%,23/32(72%)截至第24周依从性≥95%(基于回收药瓶计算)。在9例总体依从性<95%的受试者中,至第24周的依从率范围为69%至93%。
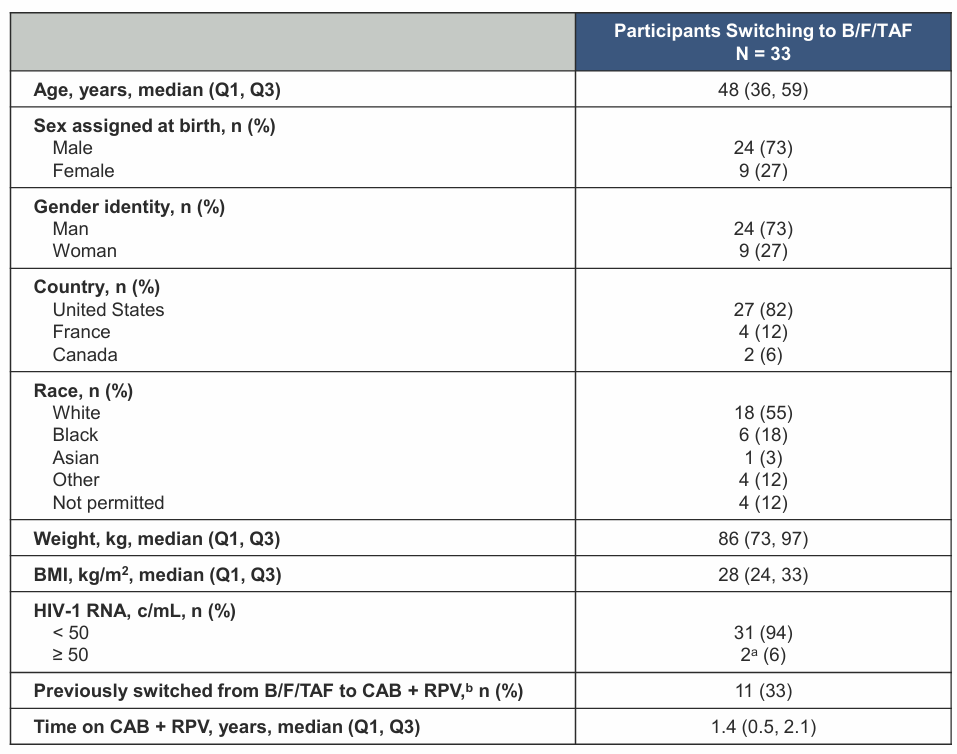
表4.基线人口学与临床特征
2. 第4周从CAB+RPV转换至B/F/TAF的治疗满意度变化
受试者报告在第4周时治疗满意度(HIVTSQ变化版)平均增加27(9.0)分。治疗满意度的所有方面均有所改善。
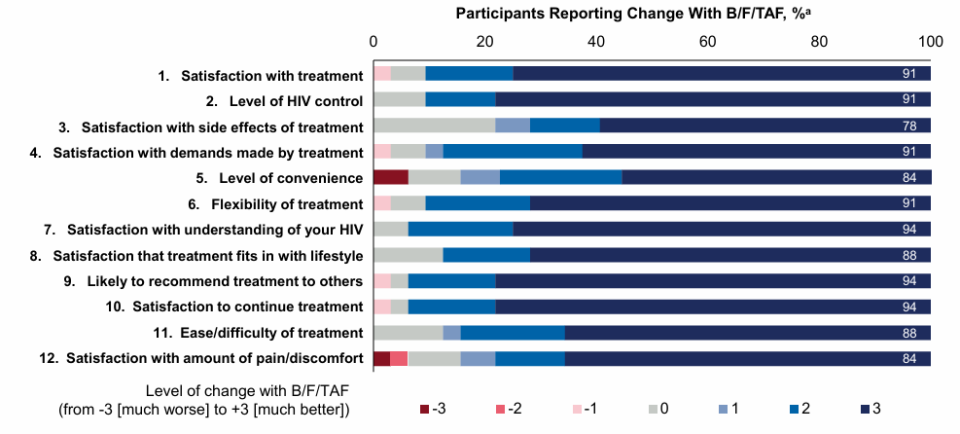
△受试者自CAB+RPV转换至B/F/TAF后第4周治疗满意度变化(基于HIVTSQc问卷)
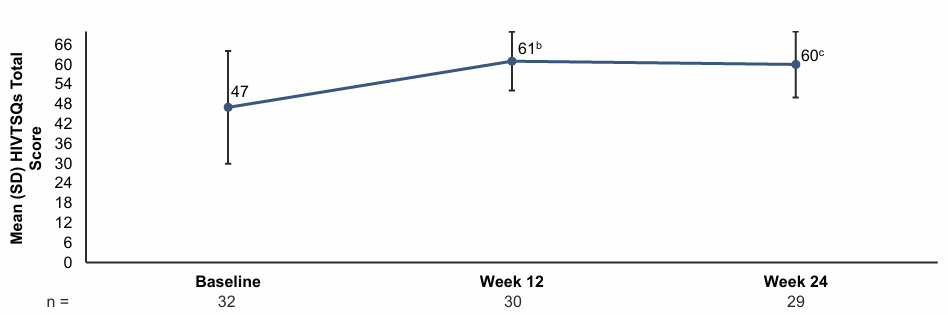
△CAB+RPV转换为B/F/TAF前后HIVTSQs总分的平均变化
治疗满意度(HIVTSQ状态版)在第12周改善,并在转换至B/F/TAF后第24周保持稳定。
3. 转换原因与副作用比较
CAB+RPV最常见的不良反应与注射部位相关:酸痛(82%)、疼痛(73%)、肿块/结节(55%)、肿胀(55%)、瘙痒(27%)和发红(24%)。受试者还报告肌肉酸痛(70%)、头痛(21%)、睡眠问题(18%)、恶心/胃部不适(9%)和腹泻(6%)。
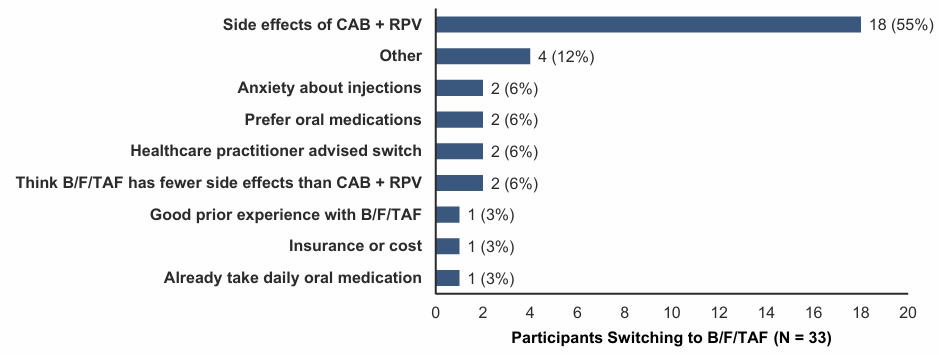
△研究特定问卷(第1天):从CAB+RPV转换为每日口服B/F/TAF的主要原因
所有受试者均表示对使用B/F/TAF成功治疗其HIV感染感到非常有希望(79%)或抱有希望(21%)。
第4周时,23/32受试者(72%)报告未经历任何B/F/TAF的副作用。报告的副作用包括恶心/胃部不适(n=6)、头痛(n=3)、腹泻(n=3)、疲劳/疲倦(n=3)、睡眠问题(n=1)、头晕(n=1)、腹部肿胀/腹胀(n=1)或其他副作用(n=1)。
在这项从CAB+RPV转换至B/F/TAF的研究中,副作用是受试者选择转换的主要原因,最常见的是注射部位酸痛、注射部位疼痛和肌肉酸痛。大多数选择停用CAB+RPV并开始使用B/F/TAF的受试者在第4周时报告未经历任何副作用。受试者报告转换后治疗满意度显著提高。B/F/TAF是希望从CAB+RPV转换至每日口服方案的HIV感染者的有效选择。提供多种抗反转录病毒治疗方案对于支持可能不偏好或无法耐受长效注射治疗方案的患者至关重要。
写在最后
本次IDWeek 2025公布的两项研究为B/F/TAF三药方案提供了充分的循证医学支持。DYAD研究96周数据证实,B/F/TAF持续治疗的病毒学抑制疗效稳定,且在安全性和耐受性方面更具优势,支持其作为病毒学抑制患者的长期治疗选择。EMPOWER研究显示,从注射治疗转换至B/F/TAF可快速显著提升治疗满意度,72%的患者在转换后第4周报告无任何副作用,同时维持高效的病毒学抑制和良好的治疗依从性。这些研究结果进一步确立了B/F/TAF在HIV长期管理中的重要地位,为不同治疗需求的患者提供了优质的治疗选择,为临床治疗决策提供了有力的证据支持。
▌参考文献:
[1]. Charlotte-Paige Rolle et al. Real-world efficacy, safety and persistence of dolutegravir/lamivudine vs. bictegravir/emtricitabine/tenofovir alafenamide among virologically suppressed adults with HIV-results from the 96-week observational extension phase of the DYAD study.IDWeek 2025 .P-348
[2]. Evaluation of Treatment Satisfaction and Experiences Among People With HIV When Switching to Bictegravir/Emtricitabine/Tenofovir Alafenamide From Cabotegravir + Rilpivirine: Results From the Phase 4 EMPOWER Study.IDWeek 2025.P-387
[3]. Rolle CP et al. Open Forum Infect Dis. 2024 Sep 26;11(10):ofae560.
[4]. Rolle CP et al. Poster EP0169. IAS 2025, Kigali, Rwanda.
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
