- 首页 > 正文
鲁俊锋教授:慢乙肝临床治愈研究进展
感染医线 发表时间:2025/12/5 17:09:54
编者按:慢乙肝的临床治愈是当前肝病领域的研究热点与终极目标,随着研究的深入和治疗策略的优化,这一目标正逐步成为现实。在2025第十一届北京感染病学术会议上,首都医科大学附属北京佑安医院鲁俊锋教授在主题报告中,系统阐述了慢乙肝临床治愈的最新研究进展,重点分析了PEG IFNα在不同人群中的疗效、停药策略优化以及临床治愈的持久性等关键问题。
慢乙肝临床治愈现状
整体情况
聚乙二醇干扰素α(PEG IFNα)治疗方案及治疗疗程对临床治愈率至关重要。各类慢乙肝人群基于PEG IFNα治疗的临床治愈研究仍在不断探索中,包括免疫耐受期人群、不确定期人群等。
最新发表的一项系统综述和荟萃分析纳入了接受PEG IFNα治疗的慢性HBV感染人群获得HBsAg清除或血清学转换的研究,共包含134篇文章(121项研究),20,608名受试者,结果显示,PEG IFNα能提高不同慢性HBV感染人群的HBsAg清除率,尤其是NAs经治患者(21%)、IHCs(57%)和儿童患者(22%)[1]。
NAs经治优势人群
珠峰项目纳入NAs治疗>1年、HBV DNA<100 IU/mL、HBeAg阴性且HBsAg≤1500 IU/mL的慢乙肝患者,接受PEG IFNα单药或联合NAs治疗48周。7年中期数据分析显示,改良意向治疗人群15896例,符合方案集人群12260例,治疗48周时的HBsAg清除率达33.8%,停药24周时的HBsAg清除率达35.63%,倾向性评分加权后PEG IFNα单药或联合治疗无显著性差异[2]。
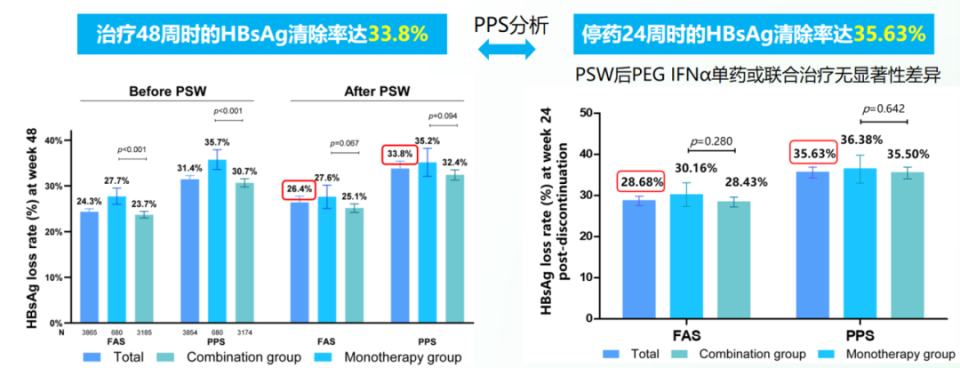
图1. 珠峰项目7年中期数据(引自讲者会议幻灯)
慢乙肝儿童
萌芽项目纳入27例HBeAg阳性、ALT正常的慢乙肝儿童,接受PEG IFNα联合恩替卡韦治疗,疗程不超过96周[3]。结果显示,总体随访24个月的HBsAg清除率为48.15%,免疫耐受期和灰区患儿分别为47.37%和50%,3-7岁患儿的HBsAg清除率更高,达64.3%。 另一项回顾性研究纳入306例慢乙肝儿童,接受干扰素α/PEG IFNα单药,或恩替卡韦单药,或两者联合治疗(占80.1%),干扰素α疗程为24-48周,PEG IFNα疗程为48周。中位随访26个月的结果显示,随访结束时慢乙肝儿童的累积HBsAg清除率为67.8%[4]。
IHCs
IHCs仍有疾病进展风险,多项研究显示IHCs基于PEG IFNα单药或联合治疗的HBsAg清除率高,若HBV DNA阴性或HBsAg低水平,疗效更佳:基线HBsAg<1000 IU/mL且HBV DNA<2000 IU/mL(约50%)、基线HBsAg<1000 IU/mL且HBV DNA阴性(50%~60%)、基线HBsAg<20 IU/mL且HBV DNA阴性(约80%)的患者均能获得较高的HBsAg清除率[5-14]。
LLV
一项研究纳入127例恩替卡韦治疗超48周的低病毒血症慢乙肝患者,分为NAs组(换用替诺福韦艾拉酚胺,76例)和NAs+干扰素组(恩替卡韦加用PEG IFNα,51例)[15]。总体基线HBsAg为3.42 (2.98, 3.81) log10 IU/mL,HBeAg阳性占63.2%。结果显示,NAs组和NAs+干扰素组第24周时的完全病毒学应答率分别为56.6%和49.0%,48周时分别提升至68.4%和66.7%,两组均无显著性差异。然而,NAs+干扰素组在第24周和第48周HBsAg较基线降幅均显著大于NAs组,且48周HBsAg清除率显著高于NAs组(8.9% vs. 0%)。
HBsAg低水平患者
对于HBsAg<100 IU/mL的NAs经治慢乙肝患者的临床治愈策略,目前存在多种观点[16-18]。
国际性多中心多种族RETRACT-B队列研究显示,NAs停药后4年的HBsAg清除率总体为13%,但停药时HBsAg<100 IU/mL患者的HBsAg清除率更高,且高加索人的HBsAg清除率显著高于亚洲人,HBsAg<100 IU/mL的亚洲人NAs停药4年的HBsAg清除率约30%[19]。德国多中心随机对照研究纳入158例NAs治疗的HBeAg阴性慢乙肝患者,HBV DNA<172 IU/mL ≥4年,患者按1:1随机分为NAs停药组和继续治疗组,随访96周。结果显示继续治疗组HBsAg清除率为0%; NAs停药组HBsAg清除率10%,HBsAg清除组的中位停药时HBsAg显著低于未清除者(72 IU/mL vs. 2046 IU/mL),对于基线HBsAg水平<100 IU/mL的患者,5/10实现HBsAg清除[20]。
然而,荟萃分析显示HBsAg<100 IU/mL患者NAs停药后仍存在复发风险(病毒学复发定义为HBV DNA>2000 IU/mL;生化学复发定义为ALT>2 ULN)。该分析纳入24项研究,3732例患者,纳入标准为NAs治疗>1年,NAs停药时HBV DNA检测不到,治疗开始时HBeAg阴性,停药后随访时间范围为9.8-111.6个月。结果显示停药时HBsAg<100 IU/mL总体的HBsAg清除率为41.8%,其中亚洲人的HBsAg清除率为28.3%,而非亚洲人为63.3%。HBsAg<100 IU/mL组的合并病毒学和生化学复发率分别为33.4%和17.3%,显著低于HBsAg≥100 IU/mL组[21]。
进一步的研究证实HBsAg<100 IU/mL患者NAs停药后仍存在较高的临床复发风险。一项RCT研究纳入90例NAs经治HBsAg<200 IU/mL、HBV DNA检测不到≥12个月,且HBV RNA或HBcrAg检测不到的亚洲慢乙肝患者,按2:1随机分为NAs停药组(60例)或NAs继续治疗组(30例)。不同亚组HBsAg清除率与临床复发率见下表。
表1. 不同亚组HBsAg清除率与临床复发率
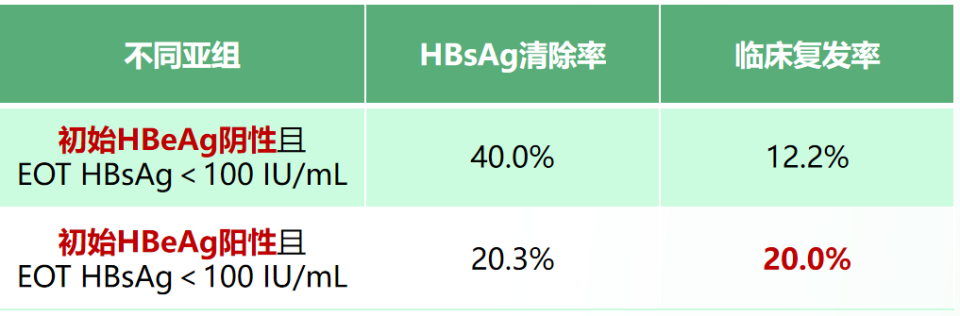
(引自讲者会议幻灯)
一篇系统综述指出,关于NAs停药实现HBsAg清除的策略仍存在较大的争议,需标准化指南,未来研究方向应整合多标志物模型优化个体化停药,以提升临床治愈率,同时确保安全性和最小化复发风险[22]。
PEG IFNα治疗组相比于NAs停药组的HBsAg清除率更高,复发率更低。一项RCT研究纳入中国四个中心的NAs经治的HBeAg阴性慢乙肝患者180例。意向性治疗分析显示,PEG IFNα治疗组中HBsAg≤100 IU/mL患者第96周时的累积病毒学复发率显著低于NAs停药组(11.1% vs. 24.1%)。PEG IFNα治疗组第96周的累积HBsAg清除率为21.5%,显著高于NAs停药组的9.0%。HBsAg为10-100 IU/mL者接受PEG IFNα治疗的HBsAg清除率高于NAs停药组(37.5% vs. 0%)[23]。
综上,基于PEG IFNα治疗策略能够更快实现临床治愈且安全停药。
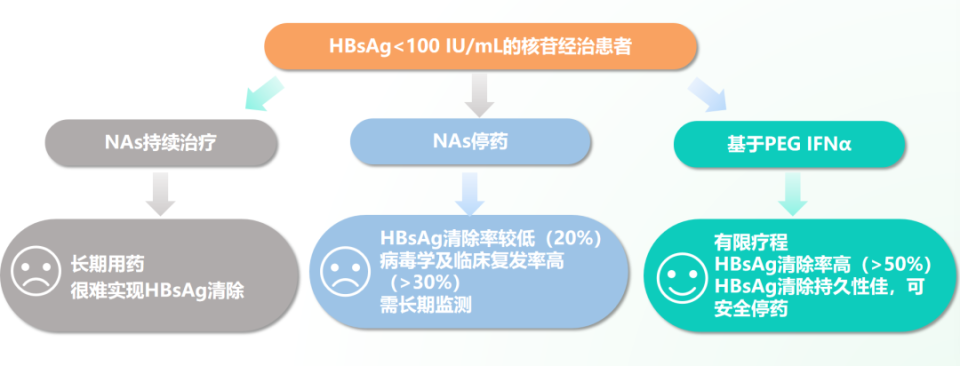
图2.HBsAg<100 IU/mL的NAs经治慢乙肝患者的临床治愈策略
(引自讲者会议幻灯)
HBsAg清除的持久性与长期获益
慢乙肝患者获得HBsAg清除后持久性佳。多项研究显示,无论是自发清除、(聚乙二醇)干扰素α或联合NAs治疗,HBsAg清除后随访1-12年的HBsAg清除率约维持在82%-95%[24-40]。获得HBsAg清除且停药的患者长期随访发生肝脏不良事件的风险极低。一项回顾性研究纳入456例接受PEG IFNα治疗后实现HBsAg清除、HBV DNA阴性、HBeAg阴性的患者,HBsAg清除且停药后的中位随访时间为70(11-173)个月,总体肝脏不良事件发生率为2.30%;随访结束时患者的APRI评分显著改善(0.53 vs. 0.25, P < 0.001);肝硬化(APRI≥2)的患者比例从5.70%显著降低至0.88%(P < 0.001)[41]。
HBsAg清除可最低化慢乙肝患者的肝癌发生风险。多项研究显示,HBsAg清除可将慢乙肝患者远期不良结局发生风险最小化,5年肝癌累积发生率低至1%左右[42-53]。
表2.HBsAg清除可将慢乙肝患者远期不良结局发生风险最小化的相关研究
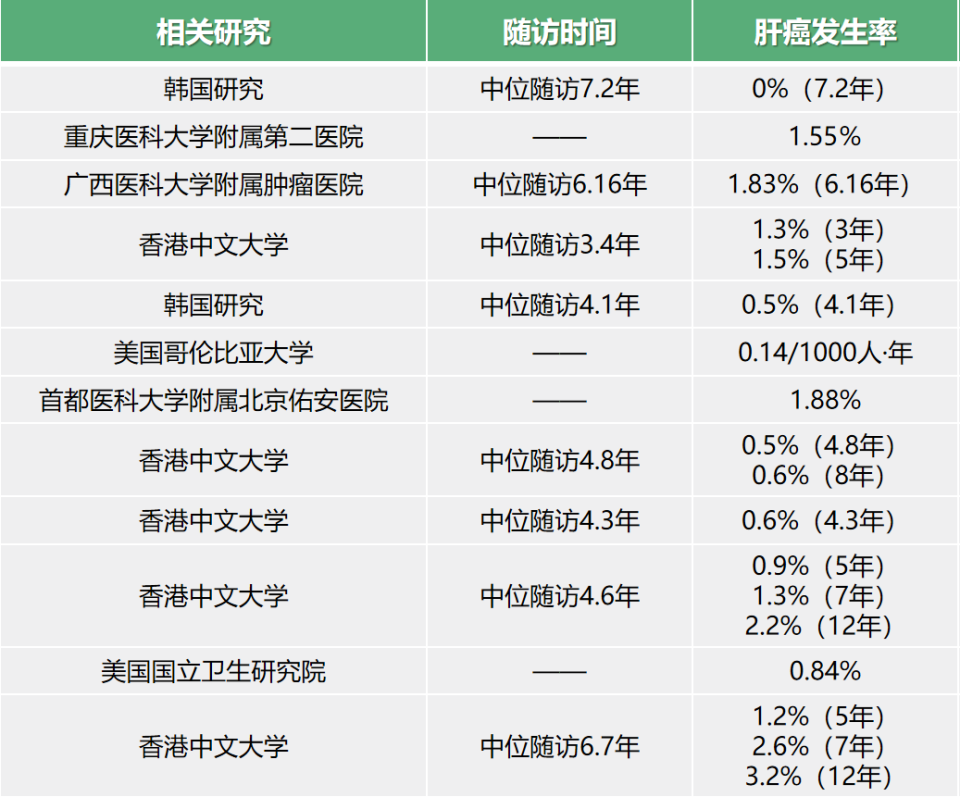
(引自讲者会议幻灯)
关于慢乙肝患者HBsAg清除持久性的预测因素,联合多个因素的预测效果更佳,包括HBsAb水平、停药时HBcAb水平、巩固治疗时间、停药时HBcrAg水平、HBeAg阴性、基线HBsAg水平等。
乙肝临床治愈理念的发展与未来展望
从2015年开始,乙肝临床治愈理念经历了逐步发展[54-57]。
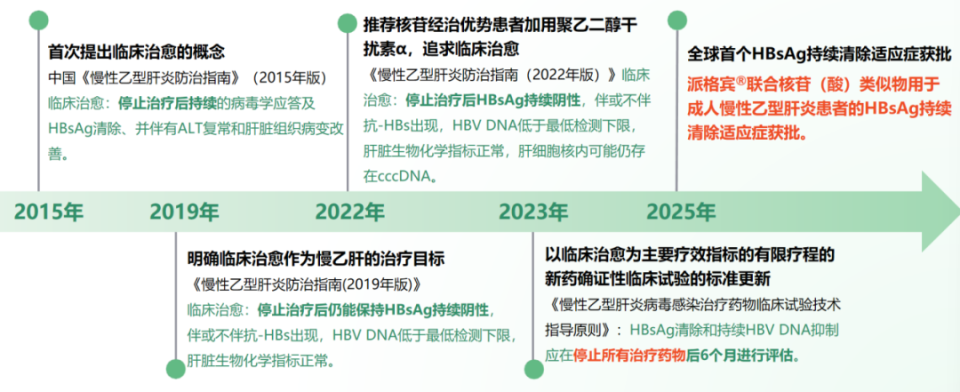
图3. 乙肝临床治愈理念的发展
(引自讲者会议幻灯)
2019年,全球首个以临床治愈为目的的多中心3期注册临床研究[58]结果显示,PEG IFNα-2b 180μg/周联合替诺福韦治疗组治疗实现HBsAg清除且HBV DNA检测不到的患者比例达31.4%,停止所有药物后24周的维持率超90%。从治疗结束到停药随访24周,PEG IFNα-2b 180μg联合替诺福韦组和PEG IFNα-2b 90μg联合替诺福韦组的HBsAg清除且HBV DNA检测不到维持率也为90.2%和96.8%。
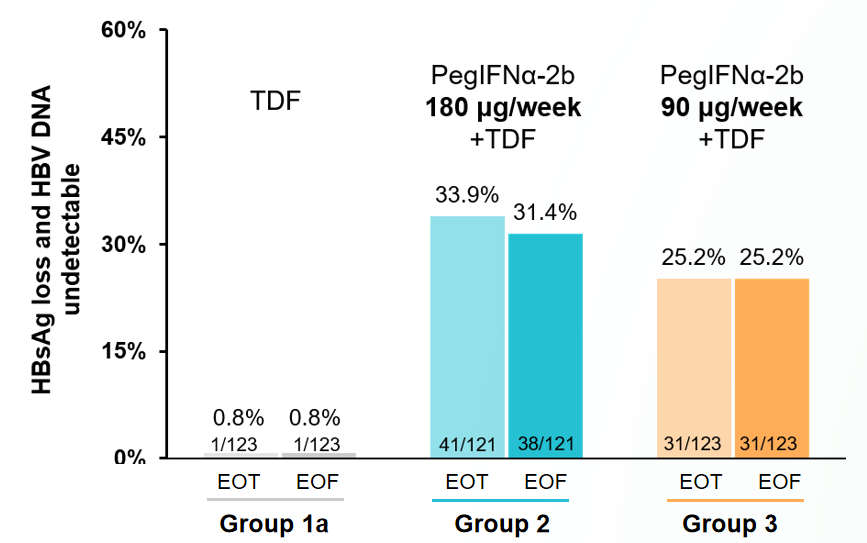
图4. NAs经治患者在EOT和EOF时实现HBsAg清除且HBV DNA检测不到的患者比例 (FAS分析)
(引自讲者会议幻灯)
此外,在基线HBsAg<100 IU/mL的患者中,HBsAg清除率达67%,更低的基线HBsAg水平与更高的HBsAg清除率显著相关。
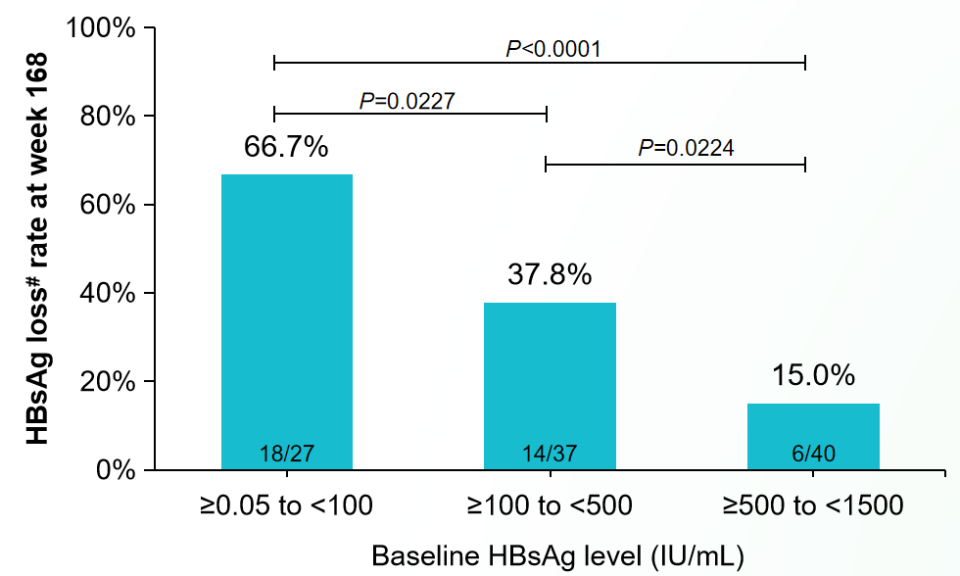
图5. 组2中不同基线HBsAg水平受试者在EOF时的HBsAg清除率
(引自讲者会议幻灯)
2025年公布的PEG IFNα-2b 3期延长随访研究[59]纳入88例实现临床治愈的患者,显示真正临床治愈的患者继续延长随访104周的维持率约90%:在104周延长随访时,各组分别有90.6%、87.0%、89.7%和100%的患者维持临床治愈。
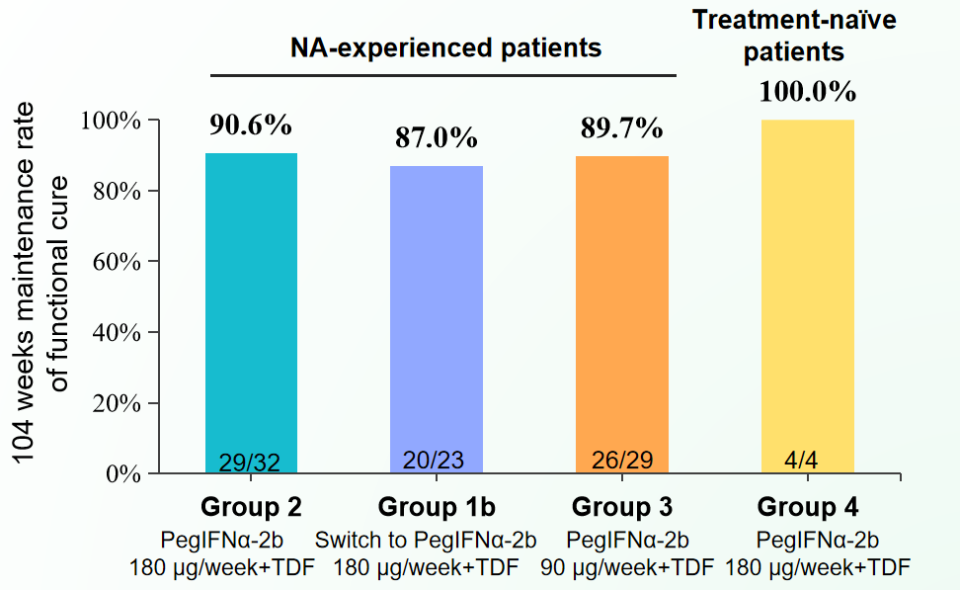
图6. 各组在延长随访104周的临床治愈维持率
(引自讲者会议幻灯)
此外,PEG IFNα间歇治疗有利于宿主免疫功能的恢复,以追求临床治愈。多项研究显示,HBsAg下降进入平台期与HLA-DR+CD38+CD8+ T淋巴细胞、自然杀伤细胞及树突状细胞的功能受损有关,但在12-24周的间歇期后,这一趋势可逆转[60-62]。
总结
提升各人群的临床治愈率:乙肝临床治愈循证证据等级提升,PEG IFNα提高不同慢性HBV感染人群的HBsAg清除率,尤其是NAs经治患者、IHCs、慢乙肝儿童,其他人群的探索研究热度提升。HBsAg<100 IU/mL的NAs经治患者基于PEG IFNα治疗策略能够更快实现临床治愈且安全停药。
实现真正临床治愈的策略:临床治愈定义重点为停止所有治疗后HBsAg持续清除和HBV DNA检测不到,目前PEG IFNα-2b正式获批用于“成人慢乙肝的HBsAg持续清除”适应证,其3期随机对照研究证实NAs经治人群的临床治愈率达31.4%。
HBsAg清除后远期不良结局的发生风险极大降低,更多新型预测HBsAg清除持久性的模型正不断丰富中,为提升各人群的临床治愈率、实现真正临床治愈的策略以及临床治愈持久性的提升提供了有力支持。
参考文献
[1]. Song CR, et al. EASL 2025, Abstract (WED-028)
[2]. Xie C, et al. APASL2025, Abstract(OP0368).
[3]. Wang X, et al. Emerg Microbes Infect, 2025, 2516173
[4]. Li SJ, et al. Liver Int, 2025, 45(4): e16134.
[5]. Huang Y, et al. Infect Dis Ther, 2021, 10(4): 2323-2331.
[6]. Chen XB, et al. Clin Res Hepatol Gastroenterol, 2021, 45(5): 101723.
[7]. Song A, et al. Front. Immunol, 2021, 12: 779347.
[8]. Zhang WC, et al. J Viral Hepat, 2022, 30(5):427-436.
[9]. Wen C, et al. Front Cell Infect Microbiol, 2023, 13: 1332232.
[10]. Cao Z, et al. Hepatology, 2017, 66(4): 1058-1066.
[11]. Ren S, et al. AASLD 2024, Abstract (311).
[12]. Mo ZS, et al. APASL2025, Abstract (OP0395).
[13]. Zeng QL, et al. Open Forum Infect Dis, 2020, 7(6): ofaa208.
[14]. 赵海东,等. 肝脏,2020,25(09):937-939.
[15]. Wang L, et al. Front Med. 2025, 12: 1642961.
[16]. Ghany MG, et al. Hepatology. 2025 Nov 4.
[17]. European Association for the Study of the Liver. J Hepatol. 2025.
[18]. 中华医学会肝病学分会, 中华医学会感染病学分会. 中华肝脏病杂志, 2022, 30(12): 1309-1331.
[19]. Hirode G, et al. Gastroenterology. 2022, 162(3):757-771.e4.
[20]. van Bömmel F, et al. J Hepatol. 2023, 78(5):926-936.
[21]. Lim SG, et al. Clin Gastroenterol Hepatol. 2024, 22(12):2403-2412.
[22]. Maung ST, Chaiteerakij R. J Viral Hepat. 2025, 32(7):e70040
[23]. Li F, et al. J Hepatol, 2024, S0168-8278(24)02426-7.
[24]. Wu Y, et al. Clin Gastroenterol Hepatol, 2020, 18(2): 514-516 e512.
[25]. Liu Y, et al. J Viral Hepat, 2019, 26 Suppl 1: 69-76.
[26]. Lok AS, et al. Hepatol Commun, 2020, 4(1): 8-20.
[27]. Li MH, et al. J Viral Hepat, 2019, 26 Suppl 1: 32-41.
[28]. Pan CQ, et al. Liver Int, 2021.
[29]. Li M, et al. Virol Sin, 2022.
[30]. Gao N, et al . J Viral Hepat, 2022, 29(10): 899-907.
[31]. Song AX, et al. J Viral Hepat, 2021.
[32]. Alawad AS, et al. Clin Gastroenterol Hepatol, 2020, 18(3): 700-709 e703.
[33]. Guo Y, et al. Front Cell Infect Microbiol, 2023, 13: 1120300.
[34]. Lu R, et al. World J Gastroenterol, 2024, 30(44): 4725-4737.
[35]. Zhang W, et al. Virol J, 2024, 21(1): 243.
[36]. Chang LJ,et al. Virol J. 2025, 19;22(1):146.
[37]. Wang T, et alFront Immunol. 2025,16:1518048.
[38]. Han L, et al. Sci Rep. 2025, 15(1):13873.
[39]. Chen J, et al. J Infect Dis. 2025, jiaf198.
[40]. Chang LJ, et al. Virol J. 2025, 22(1):146.
[41]. Li MH, et al. Virol Sin, 2025, 40(4): 579-586
[42]. Lee SK, et al. Liver Int, 2020.
[43]. Liu F, et al. Aliment Pharmacol Ther, 2016, 43(12): 1253-1261.
[44]. Jiang JF, et al. Aliment Pharmacol Ther, 2017, 45(9): 1286-1288.
[45]. Yip TC, et al. J Hepatol, 2017, 67(5): 902-908.
[46]. Kim GA, et al. J Hepatol, 2015, 62(5): 1092-1099.
[47]. Anderson RT, et al. Clin Gastroenterol Hepatol, 2020.
[48]. Song A, et al. J Viral Hepat, 2021, 28(4): 601-612.
[49]. Yip TC, et al. J Hepatol, 2019, 70(3): 361-370.
[50]. Yip TC, et al. Aliment Pharmacol Ther, 2021, 53(2): 321-331.
[51]. Yip TC, et al. J Hepatol, 2022.
[52]. Vittal A, et al. Aliment Pharmacol Ther, 2022, 55(1): 8-25.
[53]. Lee HW, et al. Aliment Pharmacol Ther, 2024, 59(10): 1223-1235.
[54]. 慢性乙型肝炎防治指南(2015年更新版) . 中华肝脏病杂志,2015,23(12):888-905.
[55]. 慢性乙型肝炎防治指南(2019年版). 中华肝脏病杂志, 2019, 27(12): 938-961.
[56]. 慢性乙型肝炎防治指南(2022年版). 中华肝脏病杂志, 2022, 30(12): 1309-1331.
[57]. 慢性乙型肝炎病毒感染治疗药物临床试验技术指导原则[EB/OL].2023: https://www.cde.org.cn/main/news/viewInfoCommon/5bebddb98aae85a980181683a980910788e
[58]. Wang GQ, et al. AASLD2024, Abstract (276).
[59]. Wang GQ, et al. AASLD2025, Abstract(1245).
[60]. Li MH, et al.AASLD2025, Abstract (1173).
[61]. Li MH, et al. AASLD2025, Abstract (1272).
[62]. Li MH, et al. AASLD2025, Abstract (1356).

鲁俊锋 教授
首都医科大学附属北京佑安医院肝病中心一科
博士,主任医师,副教授,硕士生导师
中国老年保健协会消化疾病诊疗分会副主任委员
北京医学会肝病学分会委员
北京预防医学会肝病专委会委员
北京医学会临床流行病学和循证医学分会青年委员会委员
中国医药教育协会肝病专业委员会委员
《中华肝脏病杂志》第七届青年编委会编委
《中国肝脏病杂志》编委会编委
《新疆医学》编委会常委
Frontiers系列、Liver International等杂志审稿专家
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
