- 首页 > 正文
CROI 2025丨B/F/TAF转换治疗:无惧耐药,不影响代谢和炎症,力克HIV/HBV共感染
感染医线 发表时间:2025/3/25 17:32:51

编者按:以比克替拉韦/恩曲他滨/丙酚替诺福韦片(B/F/TAF)为代表的,基于新一代整合酶抑制剂(INSTI)的抗反转录病毒治疗(ART)方案,已经成为国内外指南推荐的HIV/AIDS治疗方案,无论是初诊患者的快速启动治疗,还是病毒学抑制患者的转换治疗,B/F/TAF均展现了高耐药屏障、高病毒学抑制率和低毒副作用的治疗优势。近日举行的第32届反转录病毒和机会性感染大会(CROI 2025),报道了多项B/F/TAF转换治疗的相关研究。这些研究表明B/F/TAF转换治疗受到基线NRTI耐药性的影响极小,转换治疗后对HIV感染者的体重、血脂和全身炎症也几乎没有影响,而且在HIV/HBV共感染者中也展现了良好的病毒学和血清学疗效。
01
基线高比例NRTI耐药的HIV感染者二线治疗由PI/r转换至B/F/TAF的疗效[1]
在资源有限的环境中,使用基于蛋白酶抑制剂/利托那韦(PI/r)方案的患者具有较高的核苷类反转录酶抑制剂(NRTI)耐药性,但耐药性检测很少可及。一项在海地开展的开放标签前瞻性试验,对接受以PI/r为基础的ART方案治疗且达到病毒学抑制的成年HIV感染者,随机分配至继续当前PI/r方案或转换为比克替拉韦/恩曲他滨/丙酚替诺福韦片(B/F/TAF)。研究的主要终点是使用FDA snapshot计算第48周时HIV-1 RNA≥200 copies/mL的HIV感染者比例。对B/F/TAF组所有参与者的基线样本进行前病毒DNA基因型检测(GenoSure Archive,Monogram Biosciences),对病毒学失败(VF)的参与者进行HIV RNA基因分型,并使用IAS-USA耐药性突变(RAMs)和Stanford HIVdb版本9.6进行结果解释。
该研究在2020年10月至2023年4月期间,共筛选入组了301名(B/F/TAF:153;PI/r:148)参与者;中位年龄48岁(IQR:40,56),58%为女性。入组前使用的药物包括:180例(60%)洛匹那韦/利托那韦(LPV/r),121例(40%)阿扎那韦/利托那韦(ATV/r);234例(78%)富马酸替诺福韦酯(TDF),54例(18%)齐多夫定(AZT),13例(4%)阿巴卡韦(ABC);所有人均服用拉米夫定(3TC)或恩曲他滨(FTC)。研究结果显示:
B/F/TAF组感染者在基线时存在较高比例的NRTI相关耐药突变:在B/F/TAF组的153名参与者中,149名有基线前病毒基因型结果。基因检测结果显示携带NRTI RAMs的情况很常见;76例(51%)携带对FTC、3TC和ABC耐药性的M184V/I突变,24例(16%)携带对TDF耐药性的K65R/E/N突变,21例(14%)携带M184V/I+K65R/E/N突变。在基线时,有108例(72%)至少携带一种主要ARV类别(NRTI、NNRTI、PI或INSTI)相关的RAMs,其中67例(45%)携带2种(2-class)耐药性突变,9例(6%)携带有3种(3-class)耐药性突变。
表1. B/F/TAF组参与者基线存在的NRTIs相关突变
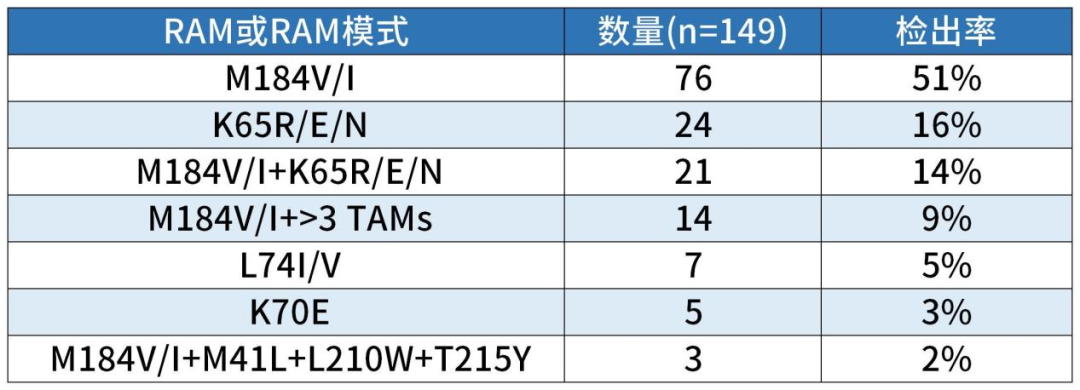
在基线NRTI耐药突变率较高的情况下,转换B/F/TAF治疗具有高病毒学抑制率:在第48周时,B/F/TAF组和PI/r组的HIV-1 RNA≥200 copies/mL感染者比例分别为0.7%(1/153)和4.1%(6/148);两组分别有145例(95%)和132例(89%)的感染者达到48周HIV-1 RNA <200copies/mL。
B/F/TAF治疗组未发现治疗中出现的耐药突变:B/F/TAF组中有1例在治疗48周时为病毒学失败且有基因检测结果,但基线和治疗失败时均未检测到RAMs;PI/r组中有4例治疗48周时为病毒学失败,其中3例有基因检测结果,1例携带针对NRTI和NNRTI的RAMs(D67D/G、M184V、K103S、P225H),2例携带针对NNRTI的RAMs(K103N;V179V/D)。
这项前瞻性研究结果显示,将病毒学抑制的成年HIV感染者从二线PI/r方案转换至B/F/TAF,无论是否预存NRTI耐药性,转换B/F/TAF治疗的疗效都不逊于继续使用PI/r方案。这些结果表明,在INSTI耐药性不常见的地区,使用二线PI/r达到病毒学抑制的成年HIV感染者可以在没有基线或历史耐药检测的情况下转换B/F/TAF治疗。
02
从DTG/3TC转换至B/F/TAF对HIV感染者体重、胆固醇和炎症的影响[2]
多替拉韦/拉米夫定(DTG/3TC)和B/F/TAF是HIV指南中主要推荐的ART方案。然而,关于从DTG/3TC转换至B/F/TAF的代谢和炎症效应的数据很少。这项来自西班牙的随机化、开放标签、多中心INSTINCT研究(GESIDA10918),纳入了经DTG/3TC治疗48周并达到病毒学抑制的HIV感染者,评估从DTG/3TC转换至B/F/TAF对比继续DTG/3TC对体重、胆固醇和系统性炎症的影响,最长随访达96周。炎症评估主要通过高灵敏度ELISA检测从基线到第96周的白介素-6(IL-6)变化。
研究纳入了141名参与者,其中135人完成了随访;14%为女性,平均年龄45±11岁;78%为白人;58%为男男性行为者;11%既往诊断过艾滋病(AIDS);中位CD4+ 细胞计数为368 cells/μL。基线CD4+ 细胞计数为789/μL,HIV抑制的平均持续时间为6.5年,基线体重为77kg,平均IL-6水平在正常范围内(1.72 pg/ml;95%CI:1.46~1.99)。两组之间的基线特征没有观察到差异。研究结果显示:
首先,从DTG/3TC转换至B/F/TAF仍可保持较高的、持久的病毒学抑制疗效:在第96周,DTG/3TC组和B/F/TAF组之间的病毒学疗效没有差异(风险差异0.01%,95%CI:-0.07~0.04)。
转换至B/F/TAF对感染者的代谢没有影响:所有参与者的总体平均体重增加1.22kg(95%CI:0.31~2.13),两组之间没有显著差异(P=0.875)(图1A)。两组的总胆固醇(-4.7 mg/dL)、HDL胆固醇(0.9 mg/dL)和LDL胆固醇(-2.3 mg/dL)变化相似。
转换至B/F/TAF对感染者的系统性炎症没有影响:调整后两组的IL-6变化没有显著差异(P=0.106),DTG/3TC组中位增加2.0倍(1.3-2.7);B/F/TAF组中位增加1.2 倍(1.0-1.4)(图1B)。
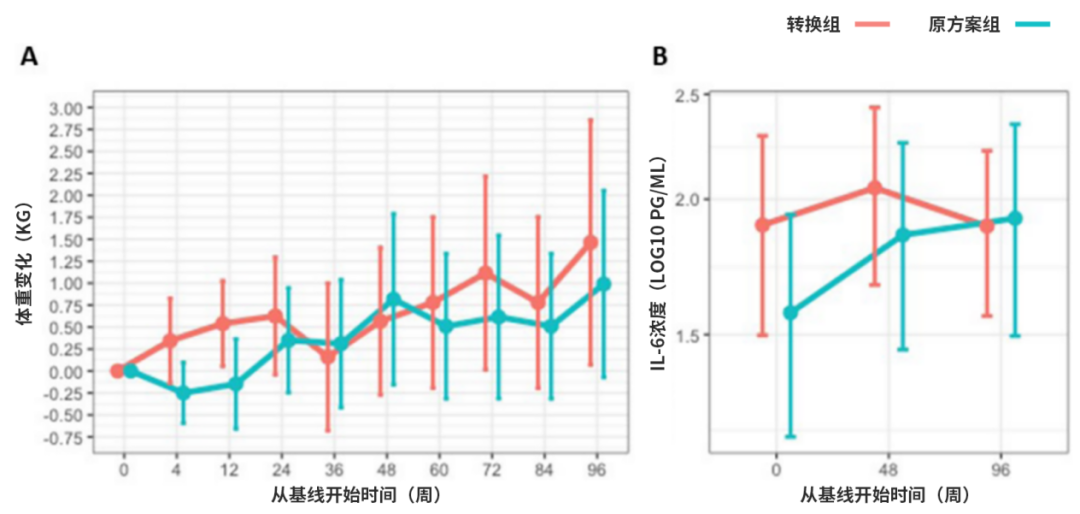
图1. DTG/3TC(原方案组)和B/F/TAF(转换组)之间的体重(A)和IL-6(B)变化
对于目前临床较为关注的体重增加、血脂异常等代谢性问题,和继续使用DTG/3TC组相比较,在达到病毒学抑制的HIV感染者中,从DTG/3TC转换至B/F/TAF对体重、胆固醇水平和系统性炎症(IL-6)的影响与继续使用DTG/3TC相当。
03
ALLIANCE研究OLE阶段:HIV/HBV共感染者B/F/TAF转换治疗[3]
III期ALLIANCE研究(NCT03547908)显示,在初治的成年HIV-1/HBV共感染者中,B/F/TAF相较于多替拉韦+恩曲他滨/富马酸替诺福韦酯(DTG+F/TDF)的48周HIV RNA病毒学抑制率达到非劣效性,对HBV DNA的病毒学抑制则显著更优,且疗效持续至96周[4-5]。然而,对于经治HIV/HBV共感染者,B/F/TAF转换治疗的疗效和安全性尚未明确。ALLIANCE研究在随访96周后对DTG+F/TDF组的感染者进行额外的48周开放标签扩展治疗(OLE),由DTG+F/TDF转换为B/F/TAF治疗。
此次OLE阶段共有89名感染者参与转换治疗,97.8%的参与者为男性,94.4%为亚洲人,中位年龄(范围)为34岁(22-61岁),30.3%的参与者ALT水平高于正常上限(ULN),58.4%为HBeAg阳性,96.6%的参与者HIV-1 RNA<50 copies/mL,83.1%的参与者HBV DNA<29 IU/mL。共有88名参与者(98.9%)转换为B/F/TAF并完成了48周的OLE治疗。研究结果显示:
B/F/TAF转换治疗对HIV和HBV均有较高的病毒学抑制疗效:在OLE第48周时,95.4%的参与者HIV-1 RNA<50 copies/mL,86.6%的参与者HBV DNA<29 IU/mL。
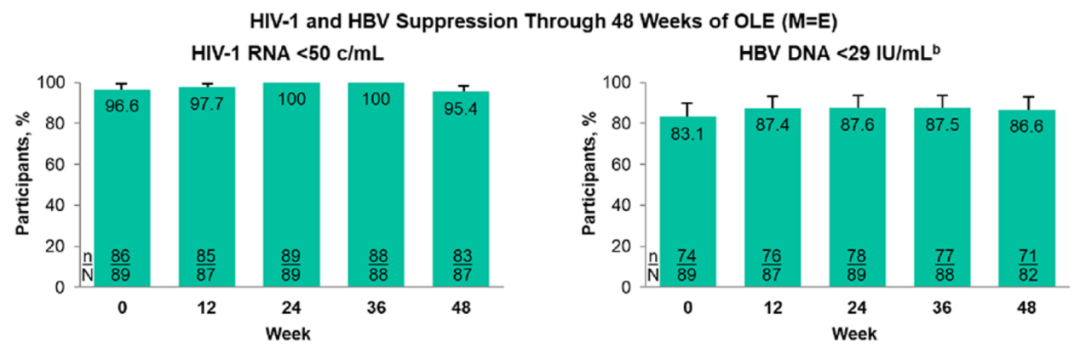
图2. OLE第48周时达到HIV-1和HBV抑制的感染者比例
肝脏相关指标改善:在基线ALT异常的感染者中,有51.9%的感染者在B/F/TAF转换治疗12周内实现ALT恢复正常,且该获益持续至48周;此外,HBeA消失率和血清学转换率分别为17.0%和12.8%;HBsAg消失率和血清学转换率分别为4.3%和0%。
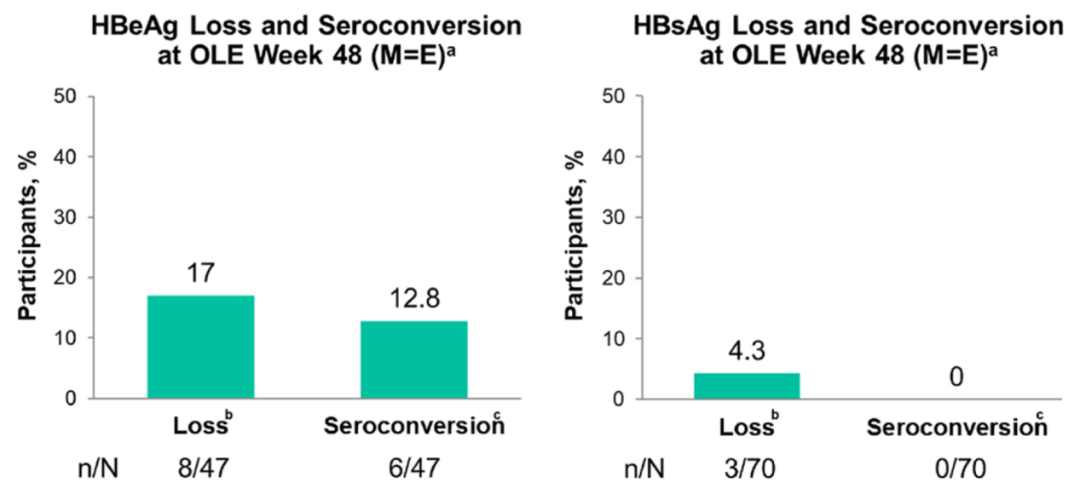
图3. OLE第48周时HBeAg消失/血清学转换和HBsAg消失/血清学转换的感染者比例
B/F/TAF的安全性和耐受性良好:截至OLE第48周,共有17名参与者(19.1%)发生研究药物相关的治疗期间不良事件(TEAE),其中3名(3.4%)为3级或4级,没有严重不良事件,没有感染者因研究药物相关不良事件而停药或死亡;转换为B/F/TAF后,感染者的中位eGFR提升6.6mL/min,印证了该治疗方案的肾脏安全性优势。
上述研究结果表明,从DTG+F/TDF转换为B/F/TAF后,B/F/TAF维持了高水平的HIV-1和HBV病毒抑制,并进一步改善了HBV相关的关键临床结局,包括HBeAg消失/血清转换、HBsAg消失以及ALT正常化。总体而言,B/F/TAF耐受性良好,没有发生因TEAE导致的研究药物停用。当前及既往结果证实了B/F/TAF在初治或经治的HIV-1/HBV共感染者中,均展现强效的病毒抑制和良好的治疗安全性、耐受性。
▌参考文献:
[1]Jean Bernard Marc, et al.High Prevalence of Baseline NRTI Resistance in PWH Switched From Second-Line PI/r to B/F/TAF.CROI 2025;abstract 729
[2]Sergio Serrano-Villar, et al.Impact of Switching From DTG/3TC to BIC/FTC/TAF on Weight,
Cholesterol, and Inflammation in HIV.CROI 2025;abstract 668
[3]Anchalee Avihingsanon,et al.ALLIANCE OLE: Switch to B/F/TAF in People With Both HIV-1 and HBV.CROI 2025;abstract 666
[4]Avihingsanon A, Lu H, Leong CL, et al. Bictegravir, emtricitabine, and tenofovir alafenamide versus dolutegravir, emtricitabine, and tenofovir disoproxil fumarate for initial treatment of HIV-1 and hepatitis B coinfection (ALLIANCE): a double-blind, multicentre, randomised controlled, phase 3 non-inferiority trial. Lancet HIV. 2023;10(10):e640-e652. doi:10.1016/S2352-3018(23)00151-0
[5]Avihingsanon, A, et al.Week 96 results of alliance, a phase 3, randomized, double-blind study comparing bictegravir/emtricitabine/tenofovi r alafenamide (b/f/taf) versus dolutegravir + emtricitabine/tenofovi disoproxil fumarate (dtg+f/tdf) in treatment-naïve hiv-1/hepatitis b (hbv) coinfection.IAS 2023;LBEPB13
来源:《感染
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
