- 首页 > 正文
华孝挺教授:从核糖体突变到院内传播,探索鲍曼不动杆菌耐药性演化丨ESCMID Global中国之声
感染医线 发表时间:2025/4/13 21:58:40

编者按:鲍曼不动杆菌作为医院感染的重要病原体,其耐药性问题尤其是碳青霉烯类耐药性,已成为全球公共卫生的重大挑战。近年来,随着耐药菌的快速演化与传播,如何破解防控困局成为科学界关注的焦点。在近日举行的2025年欧洲临床微生物学与感染病学会大会(ESCMID Global 2025)上,浙江大学医学院附属邵逸夫医院华孝挺教授团队的两项研究备受瞩目。团队不仅分析了核糖体突变如何介导鲍曼不动杆菌对新型抗菌药物奥马环素的耐药性,还通过长期基因组监测分析了医院鲍曼不动杆菌的流行病学特征及传播机制。《感染医线》在大会现场对华孝挺教授进行了深入采访,探讨了耐药菌的环境传播风险、核糖体突变的耐药机制以及院内防控策略的优化方向。
研究简介
01
核糖体突变介导鲍曼不动杆菌对奥马环素的敏感性降低
摘要号:P1609
鲍曼不动杆菌是医院感染中重要的革兰阴性病原体。其对现有抗菌药物的耐药性日益增强,凸显了开发新一代治疗方法的紧迫性。奥马环素是一种新型氨甲基环素类抗菌药物,通过结合30S核糖体亚基抑制细菌蛋白质合成。然而,关于鲍曼不动杆菌对奥马环素耐药机制的研究仍鲜有报道。
以ATCC17978为亲本菌株进行体外进化实验,获得了奥马环素耐药菌株XH1952。使用Illumina HiSeq和Breseq进行全基因组测序及突变鉴定,并通过等位基因替换技术原位重建突变。通过药敏试验、适应性实验及氧化杀伤实验评估突变的影响,同时采用冷冻电子断层扫描(cryo-ET)进行核糖体图谱分析。
主要结果:
与野生型菌株XH1529相比,携带两种核糖体突变的进化菌株XH1952可在512倍最低抑菌浓度(MIC)条件下生长。其中,rpsJ V57D突变通常与四环素类抗菌药物耐药性相关。另一突变为rplN c.-55T>G。原位互补实验证实,这两种突变均可提高奥马环素耐药性。
表1. 奥马环素对野生株、进化株与核糖体突变体重建株的体外活性

rplN基因间区的突变导致全局转录组发生变化,差异表达基因达339个,包括234个上调基因和105个下调基因。

图1. rplN基因间突变株中与野生株的差异表达基因
核糖体图谱分析与适应性实验表明,多聚核糖体丰度与菌株在Mueller-Hinton肉汤(MHB)中的生长速率呈正相关。
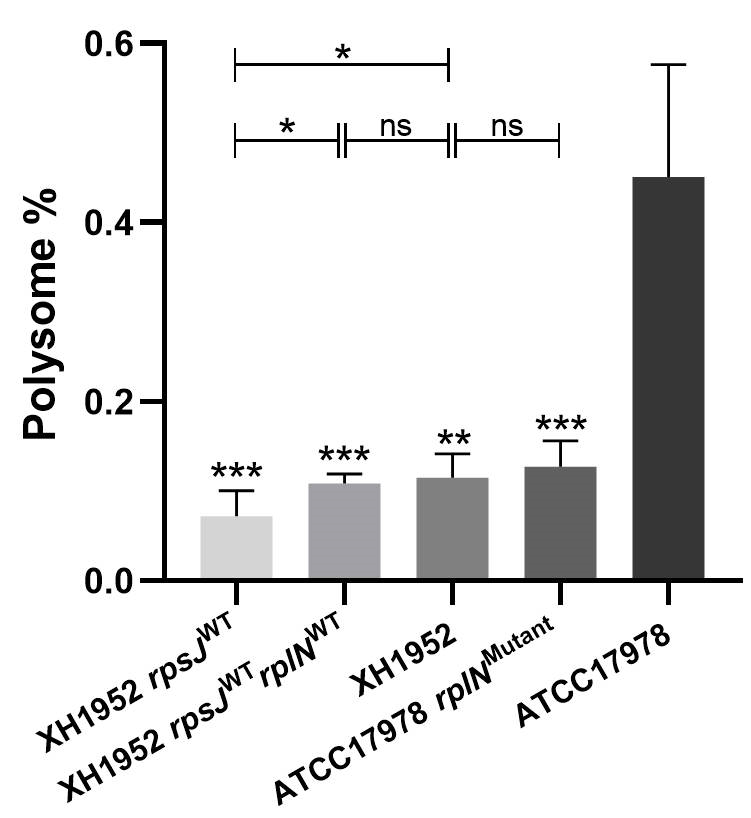
图2. 野生株、进化株与核糖体突变株中多聚核糖体的相对丰度
此外,突变菌株在40 mM过氧化氢处理下的存活率高于野生型,提示其氧化应激耐受能力更强。
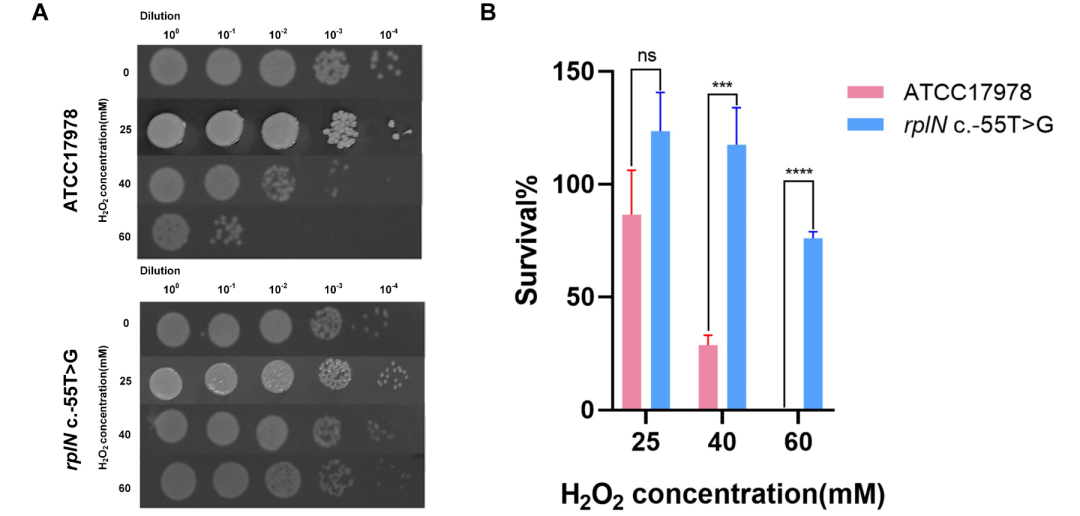
图3. 瞬时高浓度H2O2暴露后野生株和rplN基因间突变株的细菌存活率。(A)菌落总数计数结果,(B)存活率比较。
结论:本研究通过体外实验直接证明,两种核糖体突变与鲍曼不动杆菌的奥马环素耐药性相关。进一步发现,核糖体突变可导致细菌核糖体亚基及多聚核糖体分布的全局性改变,进而影响细菌生长速率和氧化应激耐受能力。
02
浙江某医院鲍曼不动杆菌流行病学及基因组特征研究(2015-2020年)
摘要号:E0592
碳青霉烯耐药鲍曼不动杆菌(CRAB)被列为全球优先研发及公共卫生防控的关键优先级病原体。鲍曼不动杆菌的种群结构反映了其随时间推移的多样化、选择及传播模式。然而,对于医院环境中临床分离株长期基因组与表型特征的认识仍有很大差距。
本研究纳入2015至2020年间杭州某医院分离的184株鲍曼不动杆菌。采用药敏试验分析耐药性,并通过全基因组测序分析菌株系统发育。结合基因组数据,比较不同簇的耐药率、耐药岛分布及院内传播事件,同时通过血清抑制实验和大蜡螟(G. mellonella)毒力实验评估菌株表型。
主要结果:
- 184株分离株主要来源于康复医学科(61.4%)和重症监护室(ICU)(12.0%)。
- 碳青霉烯类耐药率达78.8%,148株CRAB中93.1%(135/145)携带碳青霉烯酶基因blaOXA-23,3.4%(5/145)携带blaNDM-1,其中2株同时携带blaOXA-58和blaNDM-1。
- 菌株分为两簇:Cluster1(27.2%)包含ST40Pas、ST46Pas等序列型;Cluster2以全球流行克隆ST2Pas(72.8%)为主,与69起跨科室和时段的院内传播事件相关。Cluster2较Cluster1表现出更高耐药率、更多样化的耐药岛。
- 表型分析显示,ST208-KL2型菌株的毒力及血清抗性均高于ST208-KL7型。
结论:本研究分析了某医院内鲍曼不动杆菌的流行病学与基因组特征,其碳青霉烯耐药水平高且传播事件多样。此外,研究结果解释了ST208-KL2菌株在全球的流行率高于ST208-KL7的可能原因。
研究者说
01
《感染医线》:鲍曼不动杆菌的耐药性尤其是碳青霉烯类耐药性,已成为全球公共卫生危机。您和团队长期关注其传播与致病机制,能否从“同一健康”角度,谈谈环境中的不动杆菌如何成为临床耐药性传播的潜在“桥梁”?
华孝挺教授:当前,鲍曼不动杆菌的碳青霉烯类耐药率已接近70%,但其传播主要在医院环境中。我们近期发表的一项研究关注制药生产环境(非临床环境)中的不动杆菌属细菌,发现其携带编码碳青霉烯酶的质粒。由于同属细菌间的基因转移效率较高,此类质粒更易向鲍曼不动杆菌转移,从而加速耐药性扩散,最终对人类健康构成威胁。这解释了环境中的耐药基因如何成为临床传播的潜在“桥梁”,也是本研究的重要出发点。
02
《感染医线》:在本次ESCMID Global 2025大会上您汇报的研究(P1609)展示了核糖体突变介导鲍曼不动杆菌对奥马环素的敏感性降低。能否请您简要介绍以下该研究的主要发现?
华孝挺教授:本研究通过实验室进化方式,在奥马环素梯度浓度压力下诱导鲍曼不动杆菌标准菌株产生适应性突变,最终鉴定出rpsJ V57D和rplN c.-55T>G两种关键突变。其中,rplN突变位于基因上游启动子区域,而非基因内部。这一突变通过改变核糖体亚基及多聚核糖体分布,影响细菌生长速率与耐药性。值得注意的是,该突变还增强了菌株的氧化应激响应能力,这可能进一步解释了其耐药性演化的机制。
03
《感染医线》:研究(P1609)发现突变株的氧化应激耐受能力更强,这是否提示此类耐药菌可能在院内环境中具备更强的存活优势?这对临床防控策略有何启示?
华孝挺教授:当前院内感染防控主要包括隔离措施、手卫生规范及消毒剂使用等,部分消毒剂通过产生活性氧(ROS)发挥抑菌作用。若耐药菌对ROS的耐受能力显著增强(如本研究中突变株所示),其在消毒环境下将获得一定的生存优势,使得传统防控手段效率下降。这一现象提示,某些耐药菌可能更易在院内存活并传播,加剧感染控制难度。对此,临床需针对性优化防控策略,例如开发基于新型作用机制的消毒剂,或联合使用多重消杀手段,以更有效阻断耐药菌的定植与传播。
04
《感染医线》:您的另一项研究(E0592)介绍了医院鲍曼不动杆菌流行病学及基因组特征研究,能否请您分享一下该研究的主要成果?
华孝挺教授:本研究对浙江某医院2015至2020年间分离的184株鲍曼不动杆菌进行了系统分析,结果显示其碳青霉烯耐药率达78%,这与CHINET监测数据基本一致。鲍曼不动杆菌的主要耐药机制为携带blaOXA-23基因(93.1%),少数菌株(3.4%)携带blaNDM-1。通过基因组进化分析,菌株分为两簇:Cluster1包括ST40Pas、ST46Pas等序列型,耐药水平较低;Cluster2(72.8%)则以全球流行克隆ST2Pas为主,耐药性更高,且存在较强的种间传播以及跨时间、空间的传播,表明其具有强传播适应性。
本研究通过KL分型发现,同一ST208型鲍曼不动杆菌中存在KL2与KL7亚型的分化。KL分型由荚膜多糖合成基因簇决定,而该区域是基因组中的重组热点,易通过基因水平转移或突变发生结构变异,细菌的KL分型及荚膜多糖也会随之改变。尽管目前荚膜多糖的功能尚未得到充分明确,但其是细菌的主要毒力因子。比如,既往有研究报道过高毒力鲍曼不动杆菌,其耐药水平低,对药物敏感性良好,但其毒性较强,患者病情进展速度快,而这与荚膜多糖的改变密切相关。未来需借助基因组编辑技术,进一步明确荚膜多糖改变对血清型改变影响。
05
《感染医线》:ST208-KL2菌株在全球的流行率高于ST208-KL7,哪些基因组特征或表型优势可能驱动了ST208-KL2的广泛传播?
华孝挺教授:目前研究提示,ST208-KL2菌株的流行优势可能与其荚膜多糖特性相关。通过毒力测试(如大蜡螟和小鼠模型)及血清抗性实验,我们发现KL2型菌株较KL7型表现出更强的毒力及血清抗性。但菌株间的表型差异不仅限于KL分型区域,基因组其他位点的变异也可能协同驱动适应性演化。后续我们需要通过精准的基因组编辑技术排除其他区域变异的干扰,从而明确KL2型在毒力方面的优势。
▌参考文献:
[1] Yao Y, Hua XT. Ribosomal mutations mediated reduced omadacycline susceptibility in Acinetobacter baumannii. ESCMID Global 2025; Abstract P1609.
[2] Zhang Y, Hua XT. Epidemiological and Genomic Characteristics of Acinetobacter baumannii in a Hospital in Zhejiang, China: A Study from 2015 to 2020. ESCMID Global 2025; Abstract E0592.
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
