- 首页 > 正文
从流行病学到精准诊疗:肖永红教授深度解读2024年血流感染研究进展与临床启示
感染医线 发表时间:2025/5/15 17:19:04
编者按:血流感染是临床常见的危重症之一,其高死亡率与耐药菌的蔓延对全球公共卫生构成严峻挑战。近年来,随着分子诊断技术、新型抗菌药物及人工智能的快速发展,血流感染的诊疗策略正悄然发生改变。在近日举行的2025年天津市感染性疾病学术年会暨感染性疾病专科联盟培训班中,浙江大学医学院附属第一医院肖永红教授以“血流感染2024”为题,系统梳理了该领域的最新研究成果。肖永红教授基于BRICS十年监测数据及多项国际临床试验,深入剖析了血流感染的流行病学新发现,同时展示了超快速药敏检测(uRAST)等诊断技术的革新,还对新型抗菌药物研发以及治疗策略优化等方面进行了详尽阐述,为临床医生提供了极具价值的指导和参考。
01
流行病学新发现:性别差异与耐药菌感染风险
金黄色葡萄球菌菌血症的性别差异
一项纳入32项研究、95 469例患者的系统综述和荟萃分析研究发现,在金黄色葡萄球菌菌血症(SAB)患者中,女性相对于男性患者的死亡风险增加;同时,在30天死亡率模型中,女性性别与脓毒症引起的SAB死亡相关(HR 1.21,95%CI:1.02~1.44,P=0.03)[1]。另一项纳入7 515例成人SAB患者队列研究显示,女性患者30天死亡率(29% vs. 27%)和90天死亡率(37% vs. 36%)均高于男性;调整年龄、合并症等因素后,女性性别仍与30天(OR 1.19,95CI:1.06~1.34,P=0.003)和90天(OR 1.15,95CI:1.03~1.29,P=0.02)死亡率显著相关[2]。这一发现提示临床医生需重视女性患者的个体化治疗,尤其在脓毒症管理中需优化干预策略。
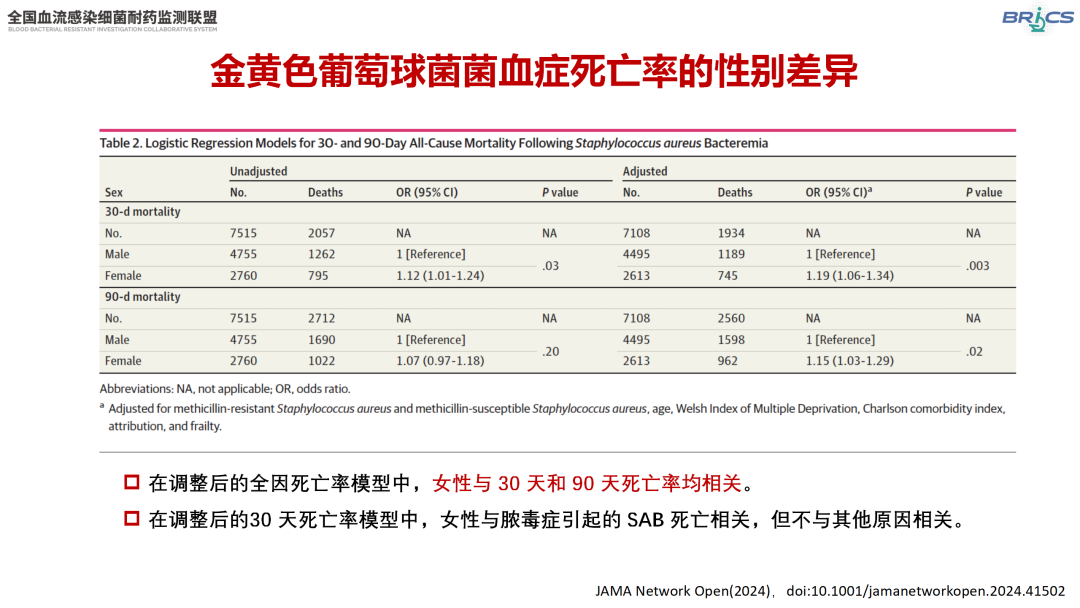
△SAB 30天和90天全因死亡率分析(引自讲者幻灯)
产碳青霉烯酶肠杆菌的感染风险
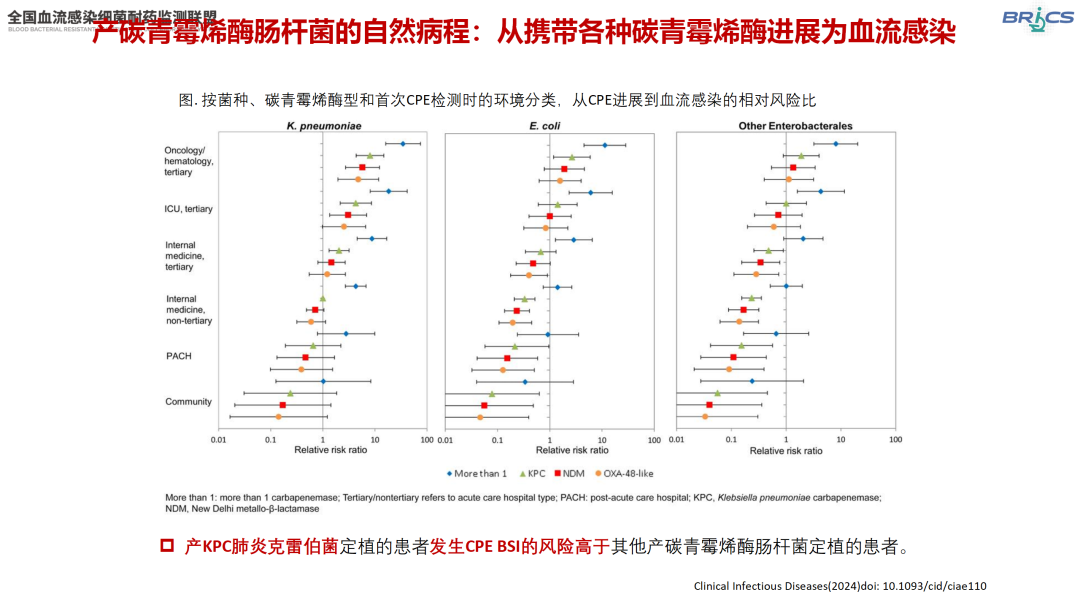
△从CPE定植进展为CPE BSI的相对风险比(引自讲者幻灯)
02
诊断技术革新:从快速药敏到纳米孔测序
无需血培养的超快速药敏检测
Nature杂志最新研究展示了一种新型超快速药敏检测(uRAST)技术[4]。该技术直接从全血中分离病原体,结合96孔芯片进行快速细菌鉴定和快速药敏检测,将传统检测时间从数天缩短至13±2.53小时。研究显示,其对大肠埃希菌和金黄色葡萄球菌的捕获效率达80%以上。这一技术不仅有望加速精准用药,更将减少广谱抗菌药物的使用,为BSI患者的早期治疗争取宝贵时间。
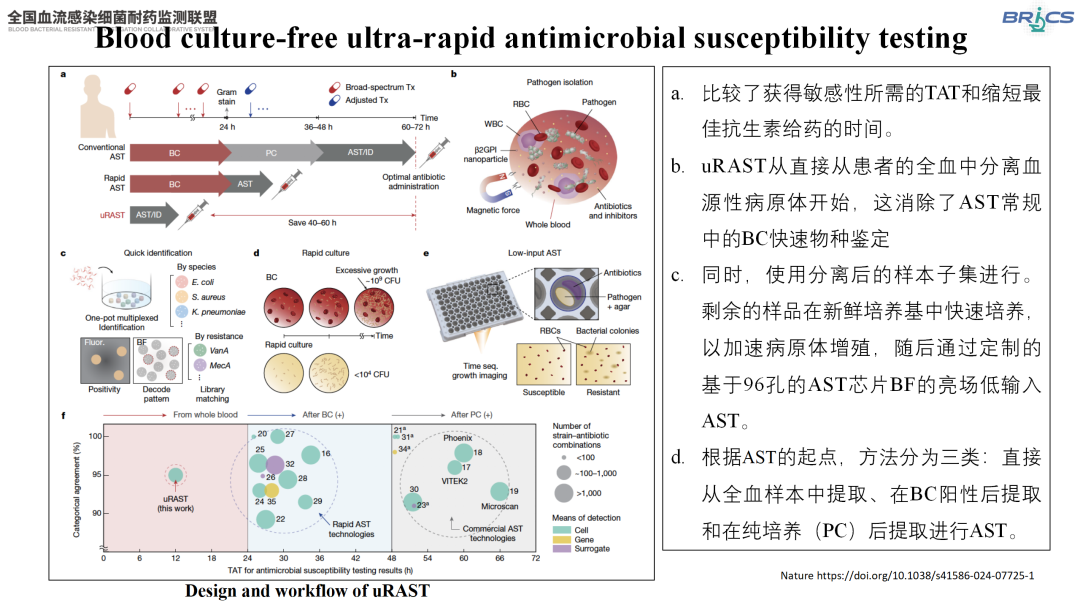
△uRAST的设计和工作流程(引自讲者幻灯)
机器学习预测脓毒症风险
德国研究者通过收集患者年龄、性别和全血细胞计数(CBC)参数(血红蛋白、血小板、平均红细胞体积、白细胞和红细胞),训练了一个增强随机森林模型,用于预测脓毒症患者入住ICU的风险[5]。该模型的预测准确性高(AUC 0.872),在外部验证中表现稳定(AUC 0.805~0.845),且CBC结合降钙素原(PCT)的模型显示出显著更高的AUC(0.857,95%CI:0.836~0.877),显著优于仅使用PCT的AUC(0.790,95%CI:0.759~0.821;P<0.001)。这一模型有望实现非ICU患者脓毒症的早期预测,缩短诊断时间,提高患者的生存率。
细菌指纹识别方法
我国研究者开发了一种通用的细菌指纹识别方法,通过结合阴离子氨基酸量子点和阳离子抗菌肽构建传感器阵列,并利用机器学习算法对三步筛选策略进行优化[6]。该方法在诊断临床尿路感染(UTI)和脓毒症方面表现出色,准确率分别达到100%和99.4%。同时,其还能够对混合比例不同的临床常见细菌株进行定量检测。这一技术为临床微生物的快速、准确检测提供了新的工具。
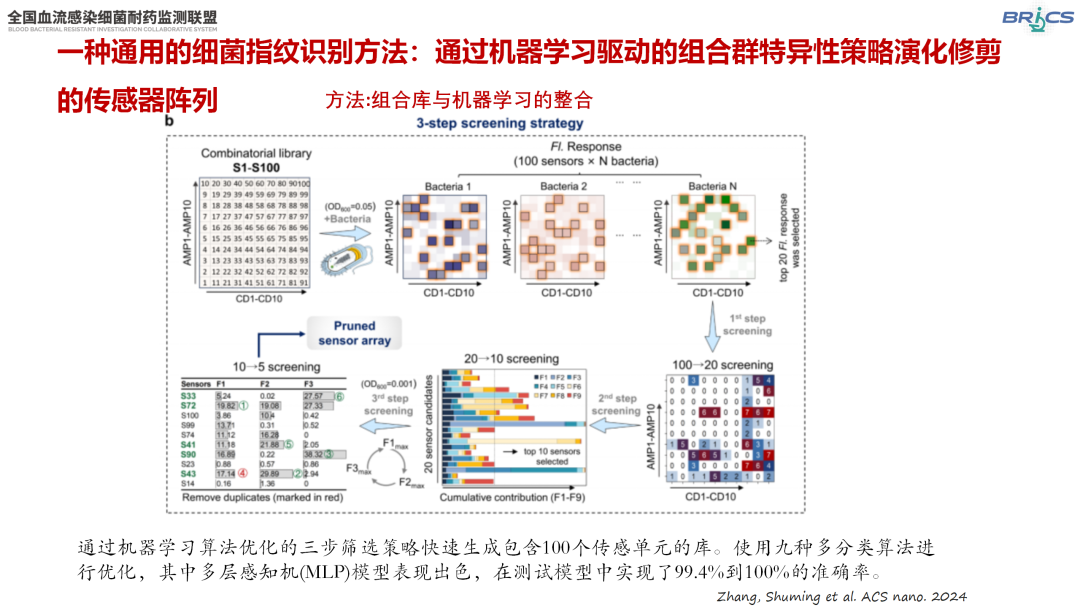
△三步筛选策略示意图以及对各种临床疾病模型的概念验证(引自讲者幻灯)
纳米孔测序技术
牛津纳米孔测序技术(ONT)以其实时分析长DNA或RNA片段的能力,在病原体鉴定和抗微生物药物耐药性预测领域展现出巨大潜力。ONT在物种鉴定上具有高分辨率,能够准确识别多种病原体。在更新ResFinder数据库后,该技术在抗菌药物敏感性预测方面的准确性和一致性也得到了显著提高,总体分类一致性(CA)超过90%,重大错误率(VME)从35.8%降至10.1%[7]。这一技术的进步有望为临床提供更快速、准确的诊断支持。
03
抗菌药物研究进展
Exebacase治疗金黄色葡萄球菌血流感染和心内膜炎
Exebacase是一种噬菌体衍生酶。在Ⅱ期临床试验中,其在治疗金黄色葡萄球菌血流感染(SABSI)和心内膜炎方面显示出了一定的治疗潜力,在预先设定的甲氧西林耐药金黄色葡萄球菌(MRSA)亚组中获得了显著更高的临床反应率(Exebacase+抗菌药物组 vs. 单独抗菌药物组:74.1% vs. 31.3%;P=0.01)[8]。然而,在Ⅲ期试验中,Exebacase联合标准抗菌药物未能达到预期的优效性治疗目标,联合组和单独抗菌治疗组MRSA感染患者的14天临床反应率分别为50.0%(32/64)和60.6%(20/33)(P=0.392)[9]。
舒巴坦/度洛巴坦治疗鲍曼不动杆菌-醋酸钙复合体感染
2024年,国家药品监督管理局(NMPA)批准了舒巴坦/度洛巴坦用于治疗由鲍曼不动杆菌-醋酸钙复合体(ABC)敏感分离株所致的医院获得性细菌性肺炎(HABP)、呼吸机相关性细菌性肺炎(VABP)。在此前进行的全球多中心、随机、对照、Ⅲ期、非劣效性ATTACK研究中,舒巴坦/度洛巴坦达到了非劣效性标准,其治疗碳青霉烯耐药ABC(CRABC)感染的28天全因死亡率不劣于黏菌素(19% vs. 32%),且肾毒性发生率更低(13% vs. 38%)[10]。
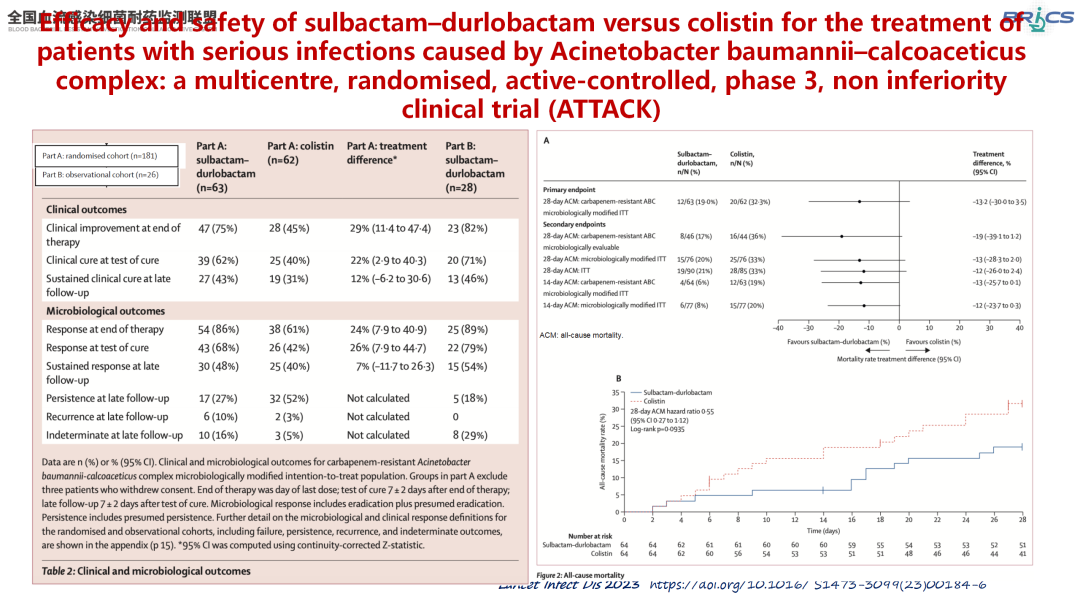
△Ⅲ期ATTACK研究主要结果(引自讲者幻灯)
头孢比罗治疗复杂性SAB
2024年,头孢比罗正式纳入国家医保目录。此前头孢比罗治疗复杂性SAB的Ⅲ期非劣效性试验显示,头孢比罗展现出与达托霉素相当的疗效,包括70天治疗成功率(69.8% vs. 68.7%)、死亡率(9.0% vs. 9.1%)、微生物学根除率(82.0% vs. 77.3%)等[11]。两组的不良事件发生率相似,头孢比罗组和达托霉素组分别有63.4%和59.1%的患者报告了不良事件,分别有18.8%和22.7%报告了严重不良事件。

△头孢比罗治疗复杂性SAB的疗效和安全性结局(引自讲者幻灯)
04
治疗策略优化
肠杆菌BSI的降级治疗
在一项开放标签、多中心、随机试验(SIMPLIFY)中,研究人员探讨了抗假单胞菌β-内酰胺类药物降级治疗肠杆菌BSI的疗效和安全性[12]。研究发现,在治疗结束后3~5天,降级治疗组的临床治愈率与继续使用广谱抗假单胞菌β-内酰胺类药物的对照组相当(90% vs. 89%)。这一研究结果为优化肠杆菌BSI的治疗策略提供了重要依据。
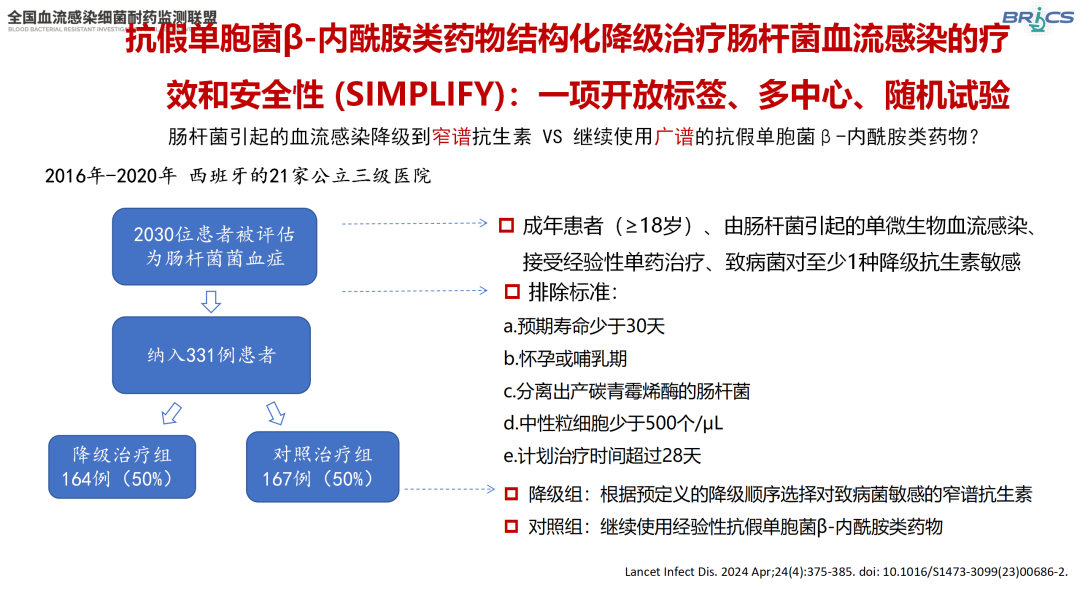
△SIMPLIFY试验研究设计(引自讲者幻灯)
口服转换疗法的新证据
针对低风险SABSI患者,国际多中心、平行、随机、对照、非劣效性SABATO研究发现,静脉治疗5~7天后转为口服抗菌药物(如复方新诺明、克林霉素或利奈唑胺)治疗的患者,其90天SABSI相关并发症发生率与持续静脉治疗组相当(13% vs. 12%)[13]。
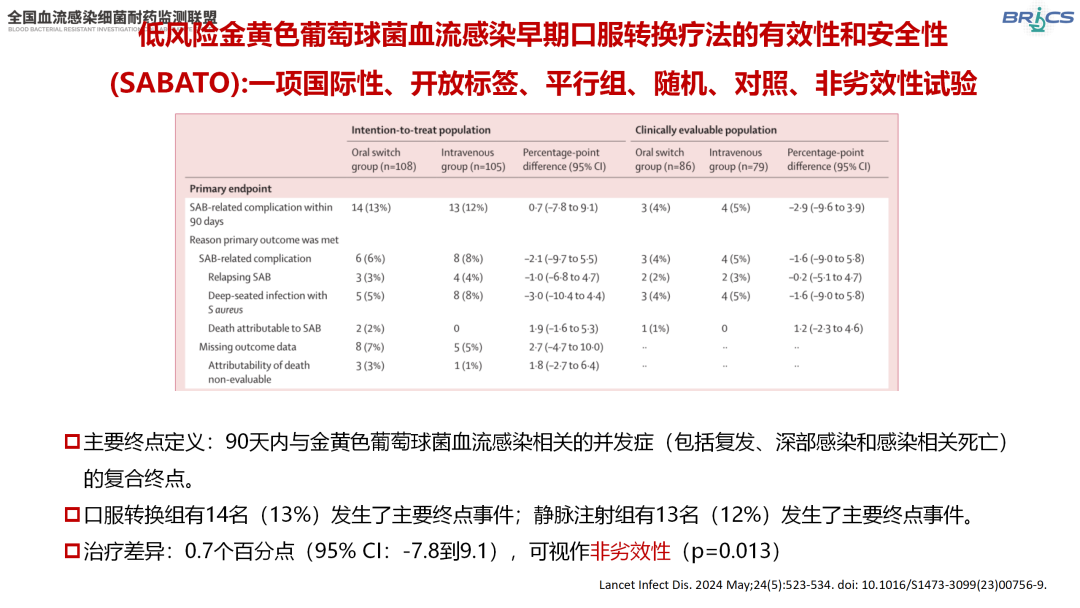
△SABATO研究意向治疗和临床可评估人群的主要结局(引自讲者幻灯)
此外,一项系统评价和meta分析纳入了38项随机对照试验和队列研究[14]。研究结果显示,早期转换为口服抗菌药物治疗不劣于持续静脉治疗,并且可以显著缩短住院时间,减少静脉治疗相关并发症及医疗费用。两项研究为优化BSI和脓毒血症的治疗方案提供了有力支持。
抗菌疗程缩短:7 vs. 14天
BALANCE研究纳入来自7个国家74家医院的3 608例BSI患者,结果显示7天组与14天组的90天死亡率(主要结局)相当(14.5% vs. 16.1%;差异-1.6%,95%CI:-4.0~0.8),复发率、住院时间等次要结局指标也获得了相似的结果[15]。这一发现挑战了传统长疗程观念,为减少抗菌药物暴露提供了重要证据。
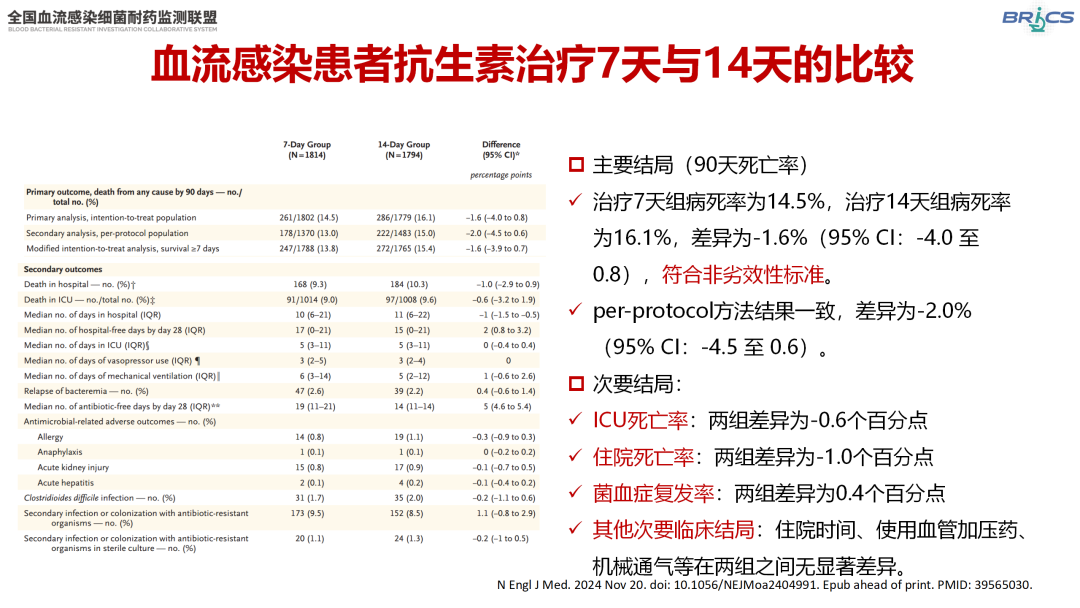
△BALANCE研究结果(引自讲者幻灯)
β-内酰胺类药物输注方式
一项回顾性队列研究发现,延长输注(EI-BL)相较于间歇输注β-内酰胺类药物(II-BL)能够显著降低患者的90天死亡率(22.4% vs. 27.8%;aOR 0.71,P=0.03),尤其是Pitt评分≥4的重症患者(38.7% vs. 55.6%;aOR 0.47,P=0.006)和感染了MIC较高病原体的患者(7.1% vs. 23.8%;aOR 0.06,P=0.02)尽管治疗相关不良事件有所增加(9% vs. 3%),但耐药性发生率并未显著上升(2.9% vs. 7.2%;P=0.35)[16]。
而BLING研究则提示,连续输注相较于间歇输注未显著降低90天死亡率(24.9% vs. 26.8%;OR 0.91,P=0.08),但可提高临床治愈率(55.7% vs. 50.0%;OR 1.26,P<0.001)[17]。
人工智能驱动的最佳抗菌药物选择
人工智能驱动的最佳抗菌药物选择(OptAB)模型整合SOFA评分、患者特征及实验室数据,动态推荐治疗方案[18]。研究结果显示,OptAB在避免抗菌药物相关副作用的同时,可使SOFA评分在18小时内下降约1个单位。这一创新技术的应用前景广阔,未来可考虑与生存分析相结合以预测个体生存概率,或可在普通病房中辅助用于脓毒症的早期识别,有望为脓毒症患者的早期诊治带来新的突破。
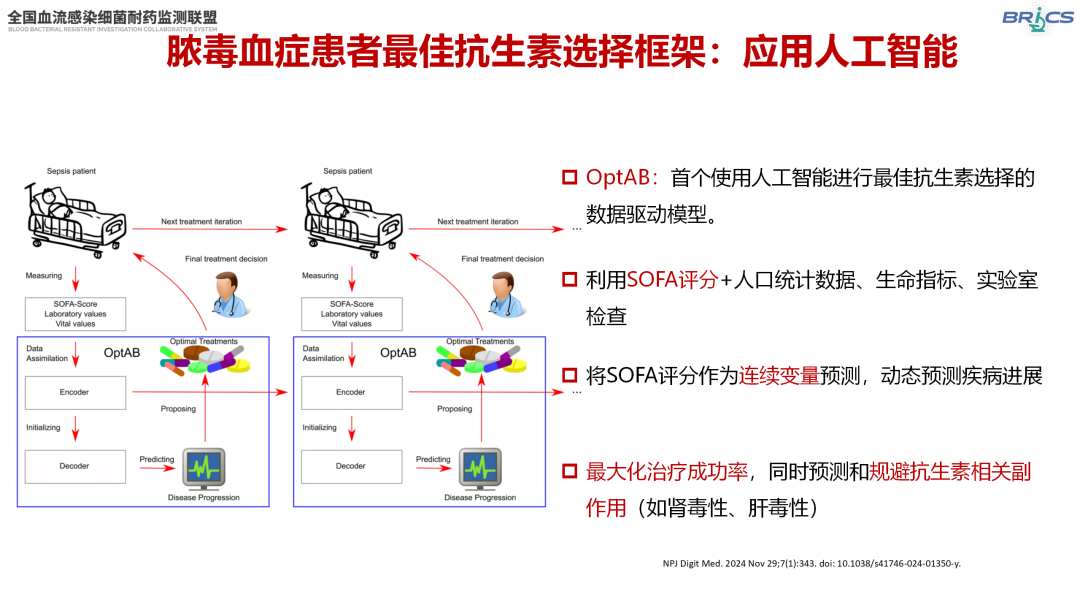
△OptAB模型概述(引自讲者幻灯)
05
总结
肖永红教授强调,未来BSI管理需以“多学科协作”为核心,通过感染、重症、药学、微生物等多学科的深度融合,将快速诊断技术、人工智能模型与个体化治疗策略系统整合,形成闭环诊疗路径。这些突破不仅为临床提供了循证依据,更标志着感染性疾病诊疗从“经验驱动”向“精准靶向”的范式转变。正如BRICS十年监测所证实的——唯有执着追求科学证据,方能破解耐药困局,挽救更多生命。未来,我们期待在这一领域看到更多的创新和突破。
参考文献
[1] Westgeest AC, Lambregts MMC, Ruffin F, et al. Female Sex and Mortality in Patients with Staphylococcus aureus Bacteremia: A Systematic Review and Meta-analysis. JAMA Netw Open. 2024;7(2):e240473. Published 2024 Feb 5. doi:10.1001/jamanetworkopen.2024.0473
[2] Carter BL, Underwood J. Sex Disparities in Staphylococcus aureus Bacteremia Mortality. JAMA Netw Open. 2024;7(10):e2441502. Published 2024 Oct 1. doi:10.1001/jamanetworkopen.2024.41502
[3] Temkin E, Solter E, Lugassy C, et al. The Natural History of Carbapenemase-Producing Enterobacterales: Progression From Carriage of Various Carbapenemases to Bloodstream Infection. Clin Infect Dis. 2024;79(1):22-29. doi:10.1093/cid/ciae110
[4] Kim TH, Kang J, Jang H, et al. Blood culture-free ultra-rapid antimicrobial susceptibility testing. Nature. 2024;632(8026):893-902. doi:10.1038/s41586-024-07725-1
[5] Steinbach D, Ahrens PC, Schmidt M, et al. Applying Machine Learning to Blood Count Data Predicts Sepsis with ICU Admission [published correction appears in Clin Chem. 2024 Aug 1;70(8):1088. doi: 10.1093/clinchem/hvae055.]. Clin Chem. 2024;70(3):506-515. doi:10.1093/clinchem/hvae001
[6] Zhang S, Stewart C, Gao X, et al. A Universal Method for Fingerprinting Multiplexed Bacteria: Evolving Pruned Sensor Arrays via Machine Learning-Driven Combinatorial Group-Specificity Strategy. ACS Nano. 2024;18(49):33452-33467. doi:10.1021/acsnano.4c10203
[7] Liu PY, Wu HC, Li YL, et al. Comprehensive pathogen identification and antimicrobial resistance prediction from positive blood cultures using nanopore sequencing technology. Genome Med. 2024;16(1):141. Published 2024 Dec 2. doi:10.1186/s13073-024-01416-2
[8] Fowler VG Jr, Das AF, Lipka-Diamond J, et al. Exebacase for patients with Staphylococcus aureus bloodstream infection and endocarditis. J Clin Invest. 2020;130(7):3750-3760. doi:10.1172/JCI136577
[9] Fowler VG Jr, Das AF, Lipka-Diamond J, et al. Exebacase in Addition to Standard-of-Care Antibiotics for Staphylococcus aureus Bloodstream Infections and Right-Sided Infective Endocarditis: A Phase 3, Superiority-Design, Placebo-Controlled, Randomized Clinical Trial (DISRUPT). Clin Infect Dis. 2024;78(6):1473-1481. doi:10.1093/cid/ciae043
[10] Kaye KS, Shorr AF, Wunderink RG, et al. Efficacy and safety of sulbactam-durlobactam versus colistin for the treatment of patients with serious infections caused by Acinetobacter baumannii-calcoaceticus complex: a multicentre, randomised, active-controlled, phase 3, non-inferiority clinical trial (ATTACK). Lancet Infect Dis. 2023;23(9):1072-1084. doi:10.1016/S1473-3099(23)00184-6
[11] Holland TL, Cosgrove SE, Doernberg SB, et al. Ceftobiprole for Treatment of Complicated Staphylococcus aureus Bacteremia. N Engl J Med. 2023;389(15):1390-1401. doi:10.1056/NEJMoa2300220
[12] López-Cortés LE, Delgado-Valverde M, Moreno-Mellado E, et al. Efficacy and safety of a structured de-escalation from antipseudomonal β-lactams in bloodstream infections due to Enterobacterales (SIMPLIFY): an open-label, multicentre, randomised trial. Lancet Infect Dis. 2024;24(4):375-385. doi:10.1016/S1473-3099(23)00686-2
[13] Kaasch AJ, López-Cortés LE, Rodríguez-Baño J, et al. Efficacy and safety of an early oral switch in low-risk Staphylococcus aureus bloodstream infection (SABATO): an international, open-label, parallel-group, randomised, controlled, non-inferiority trial. Lancet Infect Dis. 2024;24(5):523-534. doi:10.1016/S1473-3099(23)00756-9
[14] Li Q, Zhou Q, Fan J, et al. Oral switch vs. continued intravenous antibiotic therapy in patients with bacteraemia and sepsis: a systematic review and meta-analysis. Clin Microbiol Infect. 2025;31(4):551-559. doi:10.1016/j.cmi.2024.11.035
[15] BALANCE Investigators, for the Canadian Critical Care Trials Group, the Association of Medical Microbiology and Infectious Disease Canada Clinical Research Network, the Australian and New Zealand Intensive Care Society Clinical Trials Group, and the Australasian Society for Infectious Diseases Clinical Research Network, Daneman N, Rishu A, et al. Antibiotic Treatment for 7 versus 14 Days in Patients with Bloodstream Infections. N Engl J Med. 2025;392(11):1065-1078. doi:10.1056/NEJMoa2404991
[16] Karaba SM, Cosgrove SE, Lee JH, et al. Extended-Infusion β-Lactam Therapy, Mortality, and Subsequent Antibiotic Resistance Among Hospitalized Adults With Gram-Negative Bloodstream Infections. JAMA Netw Open. 2024;7(7):e2418234. Published 2024 Jul 1. doi:10.1001/jamanetworkopen.2024.18234
[17] Dulhunty JM, Brett SJ, De Waele JJ, et al. Continuous vs Intermittent β-Lactam Antibiotic Infusions in Critically Ill Patients With Sepsis: The BLING III Randomized Clinical Trial. JAMA. 2024;332(8):629-637. doi:10.1001/jama.2024.9779
[18] Wendland P, Schenkel-Häger C, Wenningmann I, Kschischo M. An optimal antibiotic selection framework for Sepsis patients using Artificial Intelligence. NPJ Digit Med. 2024;7(1):343. Published 2024 Nov 29. doi:10.1038/s41746-024-01350-y
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。