- 首页 > 正文
深三院结核之窗丨通过竞争性crRNA实现级联信号放大的非对称CRISPR技术
感染医线 发表时间:2025/5/9 18:21:12
编者按:CRISPR技术是一种源自细菌免疫系统的基因编辑工具。它能够精准地识别和切割特定的DNA或RNA序列,就像一把“分子剪刀”。近年来,科学家们发现CRISPR技术不仅可以用于基因编辑,还能应用于核酸检测领域,为分子诊断带来了新的希望。本期“结核之窗”栏目中,卢水华教授团队将分享一项发表于Nature Communications的研究。该研究设计了一种非对称CRISPR检测,通过竞争性crRNA的非对称反式切割行为,实现了信号的级联放大。该方法无需预扩增,灵敏度高达856 aM,并具备定量检测能力,为液体活检和癌症早期诊断提供了新的解决方案。
研究简介
一、研究背景
简单、灵敏且准确的核酸检测在早期癌症诊断和传染病检测中起着关键作用。尽管基于PCR的核酸检测方法因其高灵敏度和特异性被视为金标准,但人们越来越关注开发替代检测方法,以应对快速、经济高效且易于使用的诊断工具的需求。CRISPR(成簇规律间隔短回文重复序列)-Cas(CRISPR相关蛋白)系统就是其中一种替代方法。CRISPR-Cas最初作为细菌免疫系统进化而来,现已被重新设计为一种强大的核酸检测工具。迄今为止,已经开发了多种基于CRISPR的方法,通常涉及目标核酸的预扩增步骤,随后使用CRISPR-Cas酶(如Cas12a或Cas13a)进行检测。尽管CRISPR-Cas系统在简单性和特异性方面具有优势,但大多数基于CRISPR的检测工具依赖于单独的预扩增步骤,且缺乏定量检测能力,限制了其实际应用。
CRISPR-Cas12a是一种RNA引导的DNA内切酶,可编程切割目标DNA,自发现以来已被用于基因编辑。此外,Cas12a在目标特异性识别和切割后可以诱导非目标单链DNA(ssDNA)的无差别切割,这被称为反式切割活性。由于这一特性,Cas12a被广泛应用于基于核酸的分子诊断。然而,由于目前的Cas12a检测方法仅限于检测双链DNA(dsDNA)或ssDNA,因此RNA检测需要逆转录步骤和/或额外的DNA预扩增步骤。此外,CRISPR-Cas12a通常由具有原间隔相邻基序(PAM)的dsDNA目标激活。
二、研究方法
1.非对称CRISPR检测
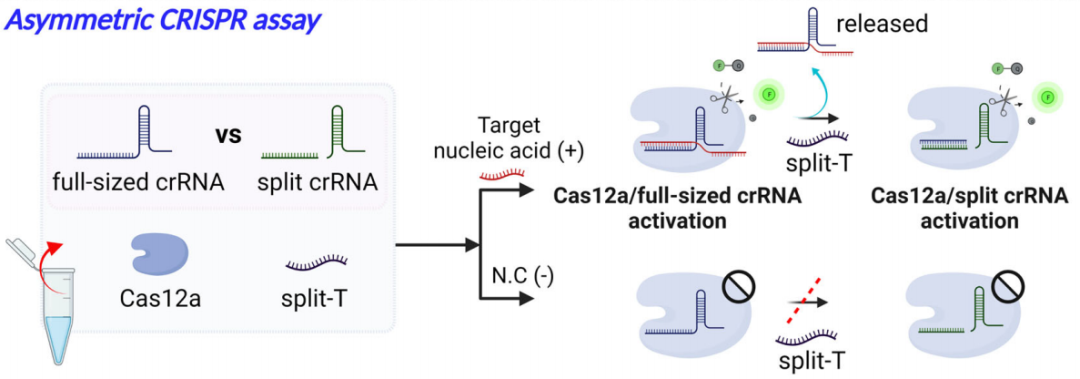
图1. 非对称CRISPR检测核酸示意图
2. 非对称CRISPR系统对DNA的检测效率
与不存在分裂crRNA和split-T时的DNA靶标检测效率相比,当添加分裂crRNA和split-T后,检测效率显著提高,非对称CRISPR检测对ssDNA靶标的检测限(LoD)为100 fM,比传统CRISPR-Cas12a检测的灵敏度高100倍。
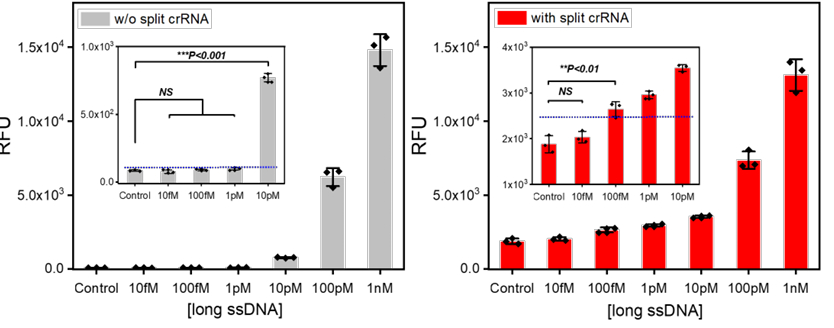
图2. 在有和没有分裂crRNA的情况下,检测ssDNA(10 fM~1 nM)1小时的荧光强度
3. 使用片段化RNA/DNA靶标实现RNA检测
crRNA的PAM近端“种子”区域严格耐受DNA序列以启动反式切割,而PAM远端区域或crRNA的3'端对RNA或DNA底物均可耐受。因此,ssRNA与crRNA的结合位置高度影响Cas12a的反式切割活性。以此为基础,研究者设计了一种通用的ssDNA activator与crRNA的种子区域互补;选择miR-19a作为目标miRNA序列,并将miRNA序列设计与靠近crRNA 3'端结合。研究者利用实时荧光信号监测不同浓度miRNA靶标的检测效果,结果显示,通过片段化DNA/RNA靶标策略可以检测到1 pM水平的miRNA。
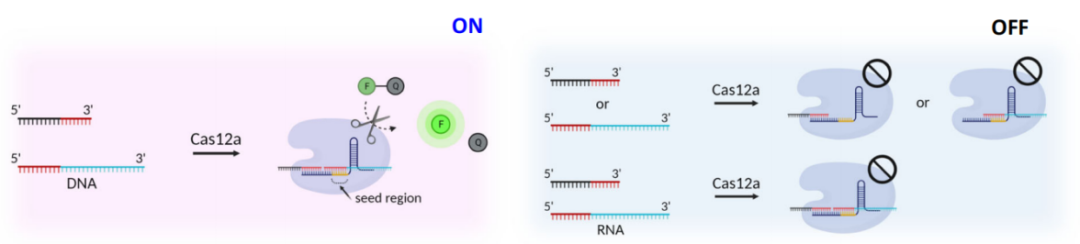
图3. 利用片段化核酸靶点进行Cas12a 的RNA检测
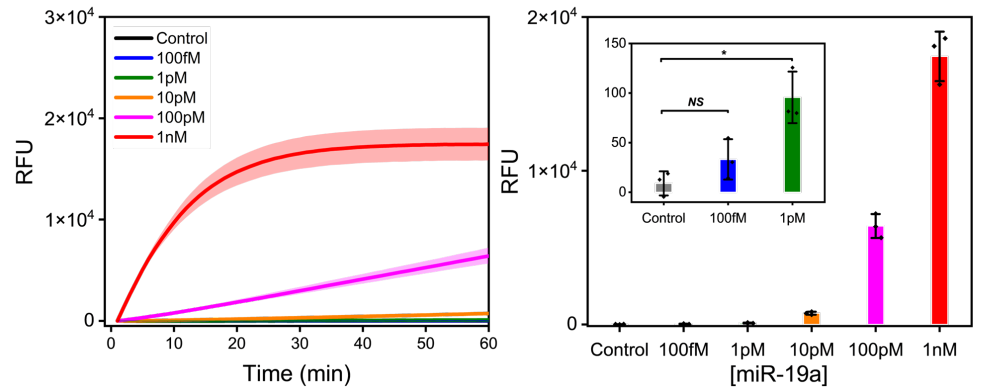
图4. 靶基因miR-19a在100 fM~1 nM范围内的实时荧光信号
4. 无扩增的miRNA定量检测
应用非对称CRISPR检测能够进一步提高Cas12a对miRNA的检测灵敏度,从而实现无扩增的miRNA检测。为了消除对额外split-T的需求,研究者将ssDNA 3'-activator同时作为分裂crRNA的靶标。完整crRNA同时结合miRNA(miRNA的红色部分,图5a)和ssDNA activator(ssDNA activator的红色部分,图5a),分裂crRNA识别ssDNA activator的一部分(DNA激活剂的蓝色部分,图5a)。对反应条件进行优化后,非对称CRISPR检测能够更加灵敏地检测出低浓度靶标,对miR-19a的检测限可达到856 aM,比传统CRISPR检测灵敏度高1 000倍,与结合预扩增步骤的CRISPR检测方法相当。
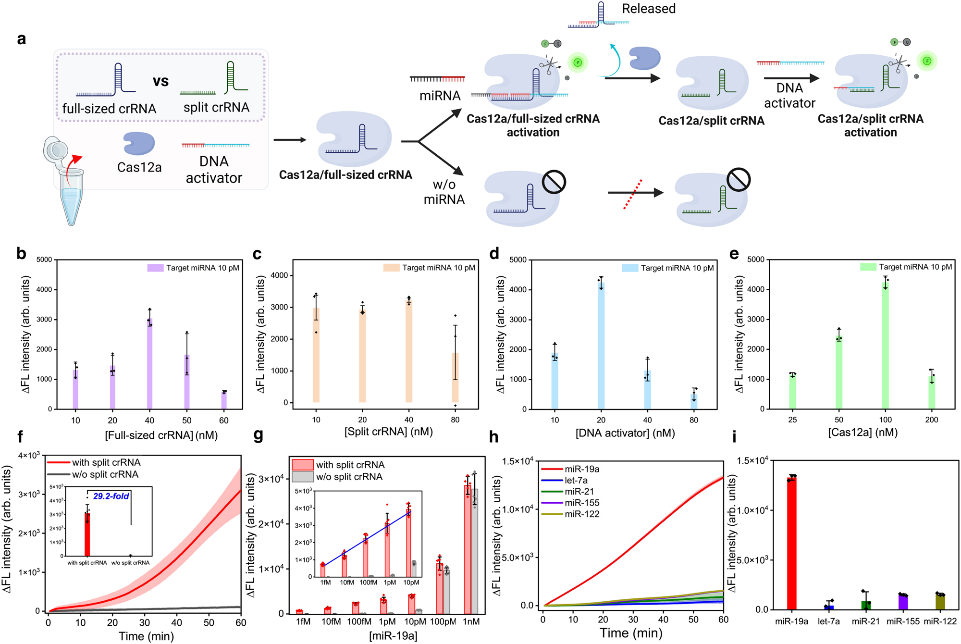
图5. 非对称CRISPR技术定量检测miRNA的优化及效果
5. 临床验证
miRNA与多种癌症的发展和进展有关。通过检测体液(如血液、尿液或唾液)中miRNA表达水平的变化,miRNA液体活检可以提供关于疾病的重要诊断和预后信息,并且比组织活检更方便且对患者更友好。研究表明miR-19a在膀胱癌患者中过表达,促进了膀胱癌的生长和转移。研究者使用非对称CRISPR检测分析了膀胱癌患者血浆样本中miR-19a的表达水平,结果证实,与健康者样本相比,膀胱癌患者样本中miR-19a的总体表达水平更高。同时与RT-qPCR的平行对比结果显示,这种检测方法与RT-qPCR的结果显示出极好的相关性。这些临床测试结果表明,非对称CRISPR方法能够简单、快速且无扩增地检测临床样本中的miRNA,并具有高灵敏度,为其临床应用提供了实证支持。
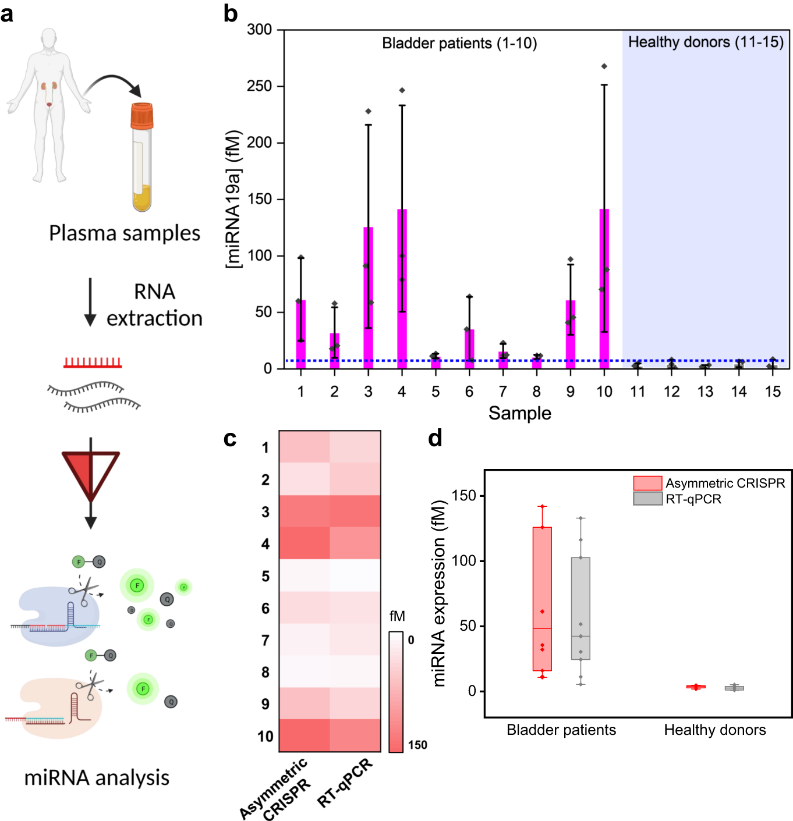
图6. 非对称CRISPR技术在临床样本中检测游离miRNA的临床应用
三、研究总结
(i)完整crRNA与Cas12a的结合亲和力高于分裂crRNA,这使得完整crRNA能够调控分裂crRNA的反应。具体而言,当两种亲和力不同的crRNA混合时,亲和力更强的crRNA引起的反式切割反应快速且占主导地位。相比之下,亲和力较弱的crRNA诱导的反应较慢,但有助于增强主导反应的灵敏度。完整crRNA和分裂crRNA之间的这种竞争反应可以提高CRISPR-Cas12a的检测灵敏度
(ii)II类V型CRISPR-Cas12a系统可以识别dsDNA和ssDNA,并表现出非特异性的ssDNA反式切割活性。RNA与crRNA的结合区域非常重要,ssDNA必须位于crRNA的5'端,这是一个在Cas12a蛋白的目标识别和切割中起关键作用的种子区域。当RNA位于crRNA的3'端并由位于crRNA5'端的DNA激活时,Cas12a可以直接识别RNA靶标,从而实现RNA的直接检测
研究点评
1.研究亮点:
(i)研究者利用竞争性crRNA的特定非对称反式切割行为,开发了一种信号放大方法,只需添加分裂crRNA及目标ssDNA即可提高CRISPR的灵敏度,这是首次报道利用具有不同CRISPR反应活性的竞争性crRNA实现信号放大的方法。
(ii)通过结合片段化DNA/RNA靶标,将非对称CRISPR检测应用于定量检测miRNA生物标志物,对目标miRNA的选择性检测限达到856 aM。与当前基于CRISPR-Cas系统的miRNA检测方法相比,这是一种使用单一CRISPR酶的一锅、一步等温信号放大方法,能够简单、灵敏且定量地检测核酸。此外,非对称CRISPR具有成本效益,每测试的材料成本估计低至0.47美元。
2.扩展和改进:
(i)为简化手动操作,该检测可进一步集成到微流控平台中,实现自动化样本制备和液体操作;
(ii)为提高检测的单核苷酸序列分辨能力,可探索和优化新型工程化CRISPR酶及crRNA;
(iii)为摆脱对昂贵荧光检测设备的依赖,可开发基于智能手机的简易检测器,用于荧光记录和信号处理;
(iv)除当前用于癌症早期诊断的miRNA检测外,非对称CRISPR检测还可进一步开发用于检测其他传染病的核酸生物标志物。
▌参考文献:
Moon J, Liu C. Asymmetric CRISPR enabling cascade signal amplification for nucleic acid detection by competitive crRNA. Nat Commun. 2023;14(1):7504. Published 2023 Nov 18. doi:10.1038/s41467-023-43389-7

更多精彩内容,请扫码订阅“深三院结核之窗”专栏

卢水华 教授
教授,主任医师,二级教授,博士生导师
国家感染性疾病临床医学研究中心副主任,深圳市第三人民医院肺病医学部主任

王颖
复旦大学病原生物学2023级硕士研究生
主要研究方向:基于CRISPR技术进行重大传染病分子诊断法的开发与应用
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
