- 首页 > 正文
深三院结核之窗丨ESCMID Global 2025结核病诊疗新突破与耐药性管理前沿研究解读
感染医线 发表时间:2025/5/9 10:19:39
编者按:世界卫生组织(WHO)数据显示,2023年全球共125万人死于结核病。继冠状病毒病(COVID-19)连续三年居首后,结核病或重新成为全球由单一传染性病原体导致死亡的首要原因。尽管标准治疗方案已广泛使用,结核性脑膜炎(TBM)死亡率仍可达40%,耐药结核的诊疗困境更亟待突破。2025年欧洲临床微生物学与感染病学会大会(ESCMID Global 2025)公布的多项研究为结核病管理带来了新的希望,包括高剂量利福平治疗TBM的Ⅲ期临床试验、宿主内结核分枝杆菌亚群驱动耐药的分子机制解析,以及靶向测序技术实现临床样本直接快速药敏检测。本期“结核之窗”栏目中,卢水华教授团队将从临床与科研角度深入解读上述研究,探讨其科学价值、临床转化潜力及未来挑战。
01
高剂量利福平治疗结核性脑膜炎:HARVEST Ⅲ期多国随机临床试验的结果
摘要号:L0017
背景
结核性脑膜炎(TBM)即使在标准治疗下死亡率仍可达到约40%,且三分之一的幸存者留下残疾。标准剂量利福平(10 mg/kg)在脑脊液(CSF)中的渗透性较差,而提高剂量可改善CSF中的药物浓度。印度尼西亚Ⅱ期试验及药代动力学-药效学模型分析表明,利福平血浆暴露量增加可提高生存率,且每日>30 mg/kg的剂量为最优选择。动物模型证实每日35 mg/kg的利福平可增强脑内杀菌活性。研究者假设,与标准治疗相比,每日35 mg/kg的利福平可降低TBM患者的死亡或残疾风险。
方法
HARVEST试验(ISRCTN15668391)是一项在印度尼西亚、南非和乌干达开展的随机、双盲、安慰剂对照Ⅲ期研究。符合条件的确诊或临床疑似TBM成人患者接受标准抗结核治疗,并按1:1随机分组,在8周强化治疗期内额外服用3~4片300 mg利福平(总量约每日35 mg/kg)或安慰剂(根据体重调整)。所有参与者均接受糖皮质激素治疗(除非存在禁忌症)。随访期为12个月,主要结局为6个月生存率,次要结局包括残疾评分(改良Rankin量表、利物浦结局量表)、神经认知结局、3~5级不良事件及12个月生存率。预设亚组分析包括MRC疾病严重程度分级、TBM共识诊断标准及HIV感染状态。
结果
2021年3月12日至2024年7月31日期间共纳入529例患者,其中29例因不符合纳入标准(如发现其他脑膜炎病因)在入组15天内退出,1例随机分配错误。最终意向治疗人群为499例,中位年龄37岁(IQR 28~45),45%(222/499)为女性,61%(304/499)合并HIV感染。43%(213/499)的患者CSF中经微生物学确诊结核分枝杆菌感染。
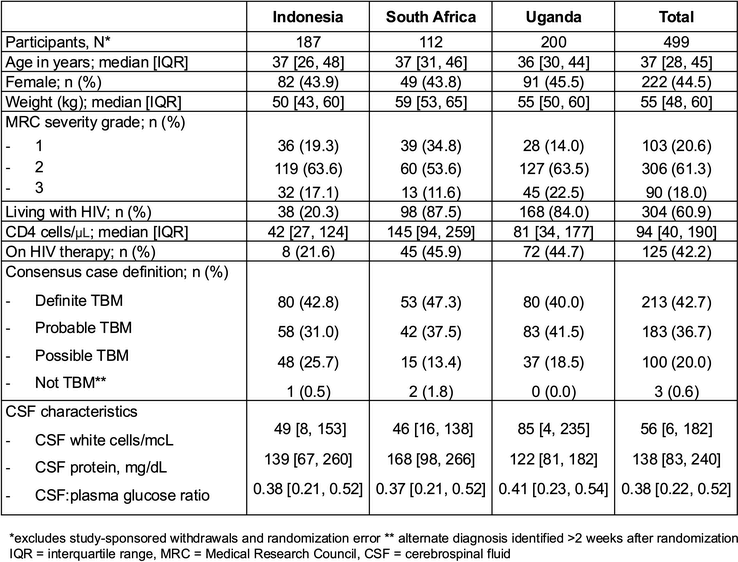
△参与者基线特征
结果显示,两组患者的6个月生存率无显著差异(HR 1.17,95%CI:0.89~1.54),高剂量利福平并未使患者获得生存获益。
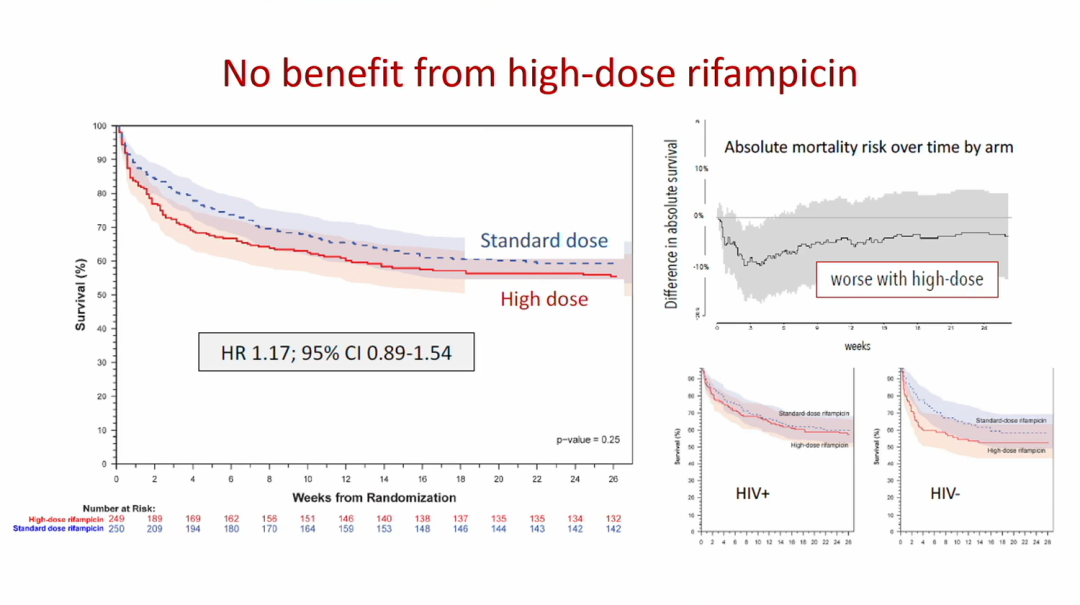
△两组总体人群的6个月生存曲线、绝对死亡风险及HIV感染者与未感染者的6个月生存曲线
亚组分析显示,没有明确的获益亚组,高剂量利福平未显著改善HIV感染者、CSF微生物学确诊TBM以及不同疾病严重程度患者的生存或残疾结局。对于CSF白细胞计数<5 cells/mm3和HIV阳性且已接受抗反转录病毒治疗(ART)的患者,高剂量利福平可能存在潜在危害。
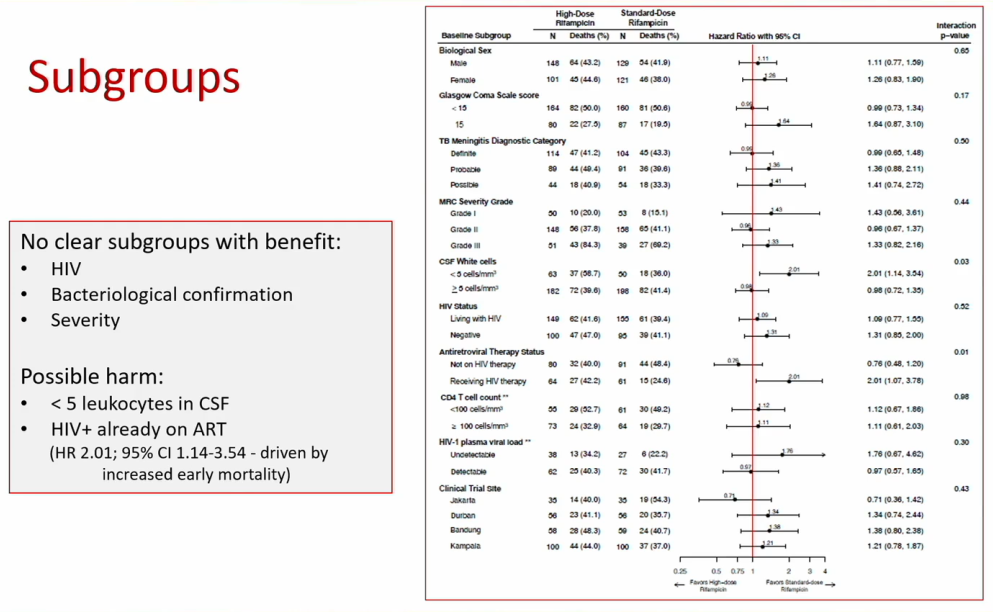
△亚组分析结果
安全性方面,高剂量组(33.7%)和标准剂量组(40.4%)均有较高比例的患者报告了不良事件,但与治疗相关的不良事件较少(6.7% vs. 4.3%)。高剂量组相较于标准剂量组,药物性肝损伤(DILI)(8.0% vs. 4.4%;P=0.09)、良性高胆红素血症(9.6% vs. 3.6%;P=)和吸入性肺炎(6.4% vs. 1.6%;P=0.006)发生率更高。
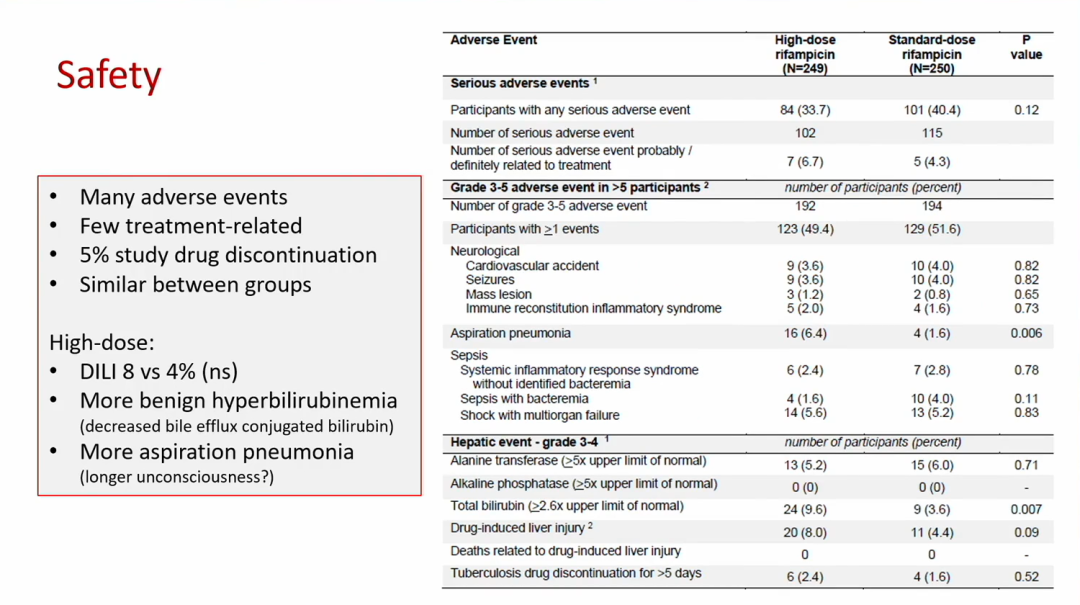
△安全性分析
专家点评
结核性脑膜炎(TBM)属于预后最差的结核病类型,经过标准方案(2HRZE/10HR)治疗的患者仍有约40%的死亡率及近1/3的致残率。在标准抗结核方案中,作为抗结核治疗基石的利福平(10 mg/kg)血脑屏障通透性较低,在血脑屏障存在炎症的情况下也只有10%~15%,无法达到最低抑菌浓度(MIC),这可能是导致疗效欠佳的重要原因。
本研究通过开展全球多中心大样本随机对照临床研究,进一步验证口服大剂量利福平(35 mg/kg)方案对于TBM的有效性及安全性,结果将为强化TBM治疗提供依据。相对于在方案中加入新药如利奈唑胺等,口服大剂量利福平方案除了可能提高有效性之外,经济性可及性方面也具有很好的优势。但大剂量利福平可能增加严重不良反应,尤其是在大剂量利福平及大剂量异烟肼联合使用的情况下,这一点需要特别关注。事实上,该研究的结果表明高剂量利福平并未使患者获得生存获益,且增加了不良反应,药物性肝损伤、良性高胆红素血症和吸入性肺炎的发生率更高。可能需要开发更创新的TBM治疗方案。
02
临床样本中的结核分枝杆菌亚群可导致利福平耐药性并阐明耐药性获得机制
摘要号:O0571
背景
抗微生物药物耐药性(AMR)的加剧要求诊断方法更精准快速。在结核分枝杆菌感染中,全基因组测序(WGS)已成为标准诊断技术,但基因型(如WGS)与表型耐药预测结果的不一致可能影响治疗和监测效果。宿主内细菌多样性,尤其是携带耐药相关等位基因的亚群存在,可能是导致此类差异的原因。
方法
本研究基于38 787份结核分枝杆菌样本,分析了次要等位基因及补偿性突变(CMs)对WGS利福平耐药预测的影响。研究人员检测了均质样本与含亚群样本中的耐药等位基因,并评估了CMs的作用。通过是否纳入次要等位基因和CMs,比较了耐药分类的灵敏度与特异度。
结果
识别样本中的次要等位基因显著提高了灵敏度,特异度略有下降。引入CMs进一步优化了耐药性预测。深入分析显示,样本可根据次要变异数量分为不同簇群,提示耐药性可能源于宿主内进化或二次感染。部分簇群与特定谱系及地理位置相关,例如印度与多谱系混合感染存在显著关联。
结论
本研究证实,评估结核分枝杆菌耐药性时需重视宿主内多样性。将耐药性次要等位基因和CMs纳入预测算法,可显著提升基因型耐药分类的准确性,从而优化治疗决策与监测策略。这写发现提出了一个关键问题,即在耐药性预测算法中,是否应该常规考虑次要等位基因和CMs。
专家点评
结核病(TB)的耐药性问题日益严峻,尤其是利福平耐药性作为多药耐药结核(MDR-TB)的核心标志,其准确检测和机制解析对临床治疗和公共卫生监测至关重要。近年来,全基因组测序(WGS)在耐药性预测中的应用逐渐普及,但其与表型药敏试验(pDST)结果的不一致性仍是一个重要挑战。结核分枝杆菌的耐药性通常由基因组中特定耐药相关基因(如ropB基因的利福平耐药决定区)的突变驱动。然而,传统WGS分析往往仅关注主效突变,忽略了宿主内存在的次要等位基因的亚群(minor alleles)以及可能增强耐药菌适应性的补偿性突变(CMs)。这可能导致基因型与表型预测的不一致,尤其是在异质性感染或混合感染的样本中。
研究团队通过分析38 787份结核分枝杆菌样本,探讨了宿主内细菌亚群(即携带耐药性次要等位基因的亚群)及补偿性突变对利福平耐药性预测的影响,揭示了耐药性获得机制的多样性,并提出了优化基因型耐药分类的潜在策略。研究结果显示,纳入次要等位基因可显著提高耐药预测的灵敏度,尽管伴随特异度的小幅下降。这一结果提示,传统WGS分析中忽略低频耐药突变可能低估耐药风险,尤其是在异质性感染或混合感染的样本中。进一步分析发现,补偿性突变(如与利福平耐药相关的基因突变)作为独立预测指标,能够进一步提高耐药预测的灵敏度。此外,样本聚类分析表明,耐药性可能通过宿主内进化或二次感染获得,且特定地理区域(如印度)与多谱系混合感染显著相关。这些发现不仅深化了对耐药机制的理解,也为精准监测提供了新视角。
本研究强调了宿主内多样性在耐药性预测中的重要性,但其临床应用仍需克服若干挑战。首先,如何定义具有临床意义的突变频率阈值仍需进一步探索。尽管一些研究将次要等位基因定义为频率≥1%,但这一阈值的设定是否适用于不同样本类型(如低生物量样本)或不同耐药基因仍需验证。其次,WGS技术在资源有限地区的普及面临成本和技术壁垒(包括数据分析能力);而生物信息学流程的标准化问题不容忽视。最后,将次要等位基因和CMs纳入临床决策需谨慎权衡灵敏度与特异度。灵敏度提升有助于早期识别耐药风险,但特异度下降可能增加假阳性风险,导致过度治疗或资源浪费。因此,需通过前瞻性研究评估低频突变对治疗结局的实际影响,以制定合理的临床阈值。
综上所述,本研究通过大规模数据分析,揭示了宿主内遗传多样性对结核分枝杆菌耐药性预测的关键作用,为优化基因型检测提供了重要方向。未来研究需进一步扩大样本的地理和临床多样性,验证次要等位基因和CMs在不同流行病学背景下的适用性。面对日益复杂的菌群多样性,在全球范围内构建大规模、地理覆盖更广的数据集,深入解析不同地区菌株谱系、耐药轨迹与流行病学特征的关系,将为构建更加精确的分子诊断体系、实现全球抗药结核控制提供数据基础。
03
利用靶向二代测序直接从临床样本中快速检测结核分枝杆菌药物敏感性
摘要号:O0575
背景
结核病(TB)仍是全球重大公共卫生挑战,耐药结核分枝杆菌的出现加剧了这一难题。目前常规方法(如基于培养的表型药敏试验[pDST]和全基因组测序[WGS]基因型药敏试验)因依赖培养步骤导致周转时间过长,可能延误最佳治疗。靶向二代测序(tNGS)可直接从临床样本中进行基因型药敏检测,为快速灵活的方法提供了新方向。
方法
本研究开发了一种基于扩增子的tNGS检测面板,包含30个扩增子,靶向与20种抗结核药物耐药相关的22个基因组区域。该方法应用于葡萄牙国家参考实验室常规诊断中收集的72份涂片阳性(0-3+)肺结核临床样本。提取DNA并进行多重PCR后,使用牛津纳米孔公司的MiniON平台对扩增子测序,并通过开源软件TB-Profiler分析。将tNGS结果与pDST及分离株的WGS数据(如有)进行比较。
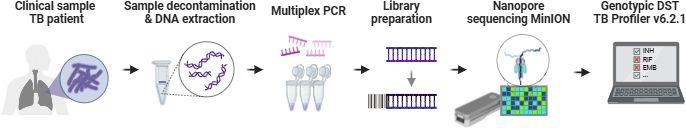
△基于tNGS的结核分枝杆菌药敏检测流程
结果
tNGS的中位扩增子成功率为90%(样本间中位数),76%的扩增子在所有位点的覆盖深度>100×。对一线药物(利福平、异烟肼、吡嗪酰胺、乙胺丁醇),tNGS与pDST的分类一致性达97%(排除不确定结果)。尽管涂片阳性程度越高测序成功率有上升趋势,但痰液样本与其他样本类型间无显著差异。未比对至结核分枝杆菌基因组的读数多源于人类DNA,表明非特异性扩增的污染细菌DNA极少且无需担心。tNGS流程可检测耐药突变和异质性耐药,与分离株WGS结果高度一致。
结论
本研究设计了一套全面的结核病药敏检测靶向测序面板,证明了tNGS直接从临床样本中快速检测的潜力。该方法无需培养,可显著缩短周转时间,为优化结核病治疗提供了新工具。
专家点评
结核病(TB)是全球公共卫生的重要挑战,而耐药性结核分枝杆菌的出现进一步加剧了这一问题的复杂性。传统的药敏检测方法,如基于培养的表型药敏试验(pDST)和基于全基因组测序(WGS)的基因型检测,因依赖耗时的培养过程(通常需数周),可能导致治疗延误。近年来,靶向二代测序(tNGS)技术因其直接从临床样本中检测耐药基因突变的潜力而受到关注。本研究通过开发一种基于扩增子的tNGS panel,结合牛津纳米孔(MiniON)测序平台,从72份涂片阳性的肺结核临床样本中检测耐药性,并与pDST及WGS结果进行对比,展示了tNGS在缩短检测周期和提高检测效率方面的显著优势。
研究团队设计的tNGS panel包含30个扩增子,覆盖22个与20种抗结核药物耐药相关的基因组区域。结果显示,该方法在扩增成功率(中位数90%)和覆盖深度(76%的扩增子>100×)方面表现稳定,对一线药物(如利福平、异烟肼)的分类一致性达到97%(排除未确定结果)。此外,tNGS能够检测耐药突变和异质性耐药,且与WGS结果高度一致。值得注意的是,研究结果展示不同样本类型(如痰液与其他样本)之间未观察到显著差异,且非特异性扩增(如人类DNA污染)极少,进一步验证了方法的特异性。这一成果表明,tNGS不仅能够绕过培养步骤,将检测周期从数周缩短至数天,还为临床提供了与现有金标准相当的可靠性,尤其在耐药结核的早期诊断中具有重要意义。
该研究验证了在真实临床样本中开展tNGS检测的可行性。相比WGS(全基因组测序)依赖培养且对数据分析要求高,tNGS因聚焦已知突变位点,数据量更小、流程更快,生物信息处理也更标准化,适合临床推广。该方法的另一大优势在于其多药联合检测能力。一次tNGS检测即可覆盖20种常见抗结核药物,尤其包括目前较难通过常规检测覆盖的新药如贝达喹啉和氯法齐明相关的耐药基因区域,这对于制定个体化治疗方案具有重要价值。同时,通过整合TB-Profiler分析结果与公开突变数据库,可实现对不同耐药突变临床意义的快速判断,推动分子检测走向“解读可用化”。
尽管如此,研究也提示了未来应用仍面临若干挑战。首先,目前技术在涂片阳性样本中成功率较高,但对涂片阴性或菌量低的样本适用性尚待进一步优化。其次,靶向扩增方案虽涵盖主流耐药位点,但对于未知突变或新型耐药机制的的情况可能未被覆盖。因此,在某些复杂病例中,tNGS仍需与pDST或WGS互为补充。此外,要实现广泛应用,还需开展更多多中心、大样本验证研究,评估该方法在不同地区、不同菌株背景下的稳定性和准确性。
综上所述,本研究为靶向测序在结核病耐药快速检测中的临床转化提供了重要证据。然而,未来研究需扩大样本多样性(包括涂片阴性、肺外结核及不同耐药谱的样本),并通过多中心合作验证其临床适用性。同时,结合动态监测耐药突变和优化成本效益,将有助于推动tNGS在资源不均背景下的实际应用。这一技术不仅为结核病诊疗提供了新工具,也为其他病原体的耐药性监测开辟了可借鉴的路径。
▌参考文献:
[1] D. Meya, R. Rovina, B. Dai, et al. High-dose rifampicin in the treatment of tuberculous meningitis: results of the HARVEST phase III multi-country randomised clinical trial. ESCMID Global 2025; Abstract L0017.
[2] V. Brunner, P. Fowler. Subpopulations in clinical samples of Mycobacterium tuberculosis can give rise to rifampicin resistance and shed light on how resistance is acquired. ESCMID Global 2025; Abstract O0571.
[3] E. Rosendal, J. Isidro, S. Carneiro, et al. Rapid drug susceptibility testing of Mycobacterium tuberculosis directly from clinical samples using targeted next-generation sequencing. ESCMID Global 2025; Abstract O0575.

更多精彩内容,请扫码订阅“深三院结核之窗”专栏

卢水华 教授
教授,主任医师,二级教授,博士生导师
国家感染性疾病临床医学研究中心副主任,深圳市第三人民医院肺病医学部主任
长期致力于TB的发病机制、疫苗与诊断技术开发、流行病学及新药临床试验等领域的研究,主持包括国家“十三五”传染病重大专项、重大新药创制项目、国家自然基金重大课题在内的国家、省部和市级科研项目12项,合计研究经费超8870万元。在NEJM、Lancet、PNAS等顶级期刊发表学术论文73篇,组织撰写指南与专家共识3篇,主编专著1部。相关成果获“中国防痨协会科学技术奖”一等奖和“上海医学科技奖”三等奖,多次被WHO指南引用。

方木通
主任医师,深圳市第三人民医院肺病一科副主任
专业特长:
难治性 NTM肺病的治疗
耐药结核病及肺外结核病的治疗
学术任职:
中国防痨协会临床专业委员会委员
中华医学会结核病分会结核性脑膜炎专业委员会委员
广东省医院协会结核病防治与管理专委会副主任委员
学术成绩:
发表专业论文20多篇,参与出版专著1部(副主编),主持及参与多项科研项目及药物临床试验。
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
