- 首页 > 正文
德国指南:ICU危重患者侵袭性肺曲霉病诊疗
感染医线 发表时间:2025/6/11 20:15:49
侵袭性肺曲霉病(Invasive Pulmonary Aspergillosis, IPA)是重症医学科(ICU)中危重病患者的一种严重并发症,其诊断和治疗一直是临床实践中的难点。日前,德国国家指南(AWMF 113-005)为ICU中IPA的诊断和治疗提供了详细的指导和建议(文末点击“阅读原文”下载全文)。

流行病学
侵袭性霉菌感染主要由曲霉菌属(Aspergillus spp.)引起。大多数感染(90%)是由烟曲霉复合种(A. fumigatus species complex)引起的,其次是黄曲霉复合种(A. flavus)、黑曲霉复合种(A. niger)和土曲霉复合种(A. terreus)。侵袭性肺曲霉病(IPA)的发病率因患者群体、地理位置的不同而有所差异,有关其基础诊断标准也一直缺乏共识。此外,当使用抗原或核酸扩增检测等间接方法时,区分定植和感染可能很困难,尤其是当无法获得组织病理学检查结果时。
在重症医学科(ICU)的危重病患者中,侵袭性肺曲霉病的发病率很可能被低估,这一点从回顾性尸检研究的结果中可以得到提示,在这些研究中,2.8%的患者患有侵袭性曲霉病,但其中只有40%的病例在生前被诊断出来。在患者死亡率数据方面也存在显著差异,因为IPA通常发生在病情严重程度显著、死亡风险已经显著增加的患者中。在比利时鲁汶的一家ICU回顾性队列研究中,共纳入了1850名患者,其中6.9%的患者有曲霉菌感染的微生物学或组织病理学证据。在这项研究中,非血液系统癌症患者的确认或可能的IPA比例为3.7%,这些患者的死亡率为90%。
侵袭性曲霉病的风险因素
近年来,人们已经确定了危重病患者中IPA的额外风险因素。除了ICU经典的危险因素外,还包括(长期)中性粒细胞减少症(<500/mm³)、异体干细胞移植后、血液系统或实体肿瘤的存在、器官移植后以及患有先天性或获得性免疫缺陷(慢性肉芽肿病、艾滋病、HIV感染伴有中性粒细胞减少症),以及慢性阻塞性肺病(COPD)、急性呼吸窘迫综合征(ARDS)、机械通气、流感和SARS-CoV-2病毒感染、肝硬化、长期糖皮质激素治疗等。下表提供了文献中描述的侵袭性曲霉病风险因素的概述。在过去,人们已经提出了许多算法和诊断标准用于IPA。为了进一步协调研究,最近已经发表了一个国际共识定义用于IPA。
往期推荐
重症患者侵袭性真菌病的诊断定义,来自FUNDICU协作组的专家共识
|
侵袭性肺曲霉病(IPA)的风险因素 |
|
ICU特定标准
|
|
实体肿瘤 |
|
慢性阻塞性肺病(COPD) |
|
(长期)中性粒细胞减少症(<500/mm³) |
|
血液系统恶性肿瘤 |
|
异基因干细胞移植 |
|
长期皮质类固醇治疗** |
|
其他免疫抑制药物(T细胞免疫抑制剂,例如:钙调磷酸酶抑制剂、肿瘤坏死因子-α抑制剂、淋巴细胞特异性单克隆抗体、钙调磷酸酶抑制剂、肿瘤坏死因子-α抑制剂、淋巴细胞特异性单克隆抗体、免疫抑制性核苷类似物) |
|
同种异体干细胞移植后的急性和慢性移植物抗宿主反应 |
|
实体器官移植,特别是肺移植 |
|
先天性免疫缺陷 |
|
急性呼吸窘迫综合征(ARDS) |
|
吸烟 |
|
酗酒 |
|
曲霉属(Aspergillus spp.)定植 |
|
环境暴露于霉菌(建筑活动、植物土壤、食物) |
诊断
指征
随着2024年3月底ICU患者侵袭性真菌感染标准的发布,已在ICU危重病患者中建立了关于IPA的(研究)定义的广泛共识。为了创造有力的证据,该指南主要是为了协调研究问题,因此非常保守,建议也因而非常严格。在临床环境中,可能需要在特殊情况下适当偏离这些建议,并且需要有充分的理由。考虑到这些方面,我们提出的诊断(和治疗)路径如下图所示。
▽临床诊断(Probable infection)
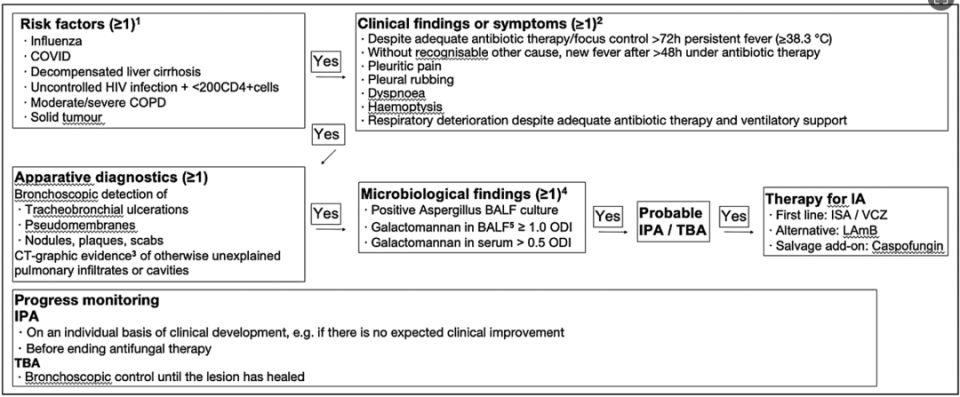
▽确诊(Proven infection)

影像学检查
近期发布了关于真菌疾病影像学诊断的建议。影像学检查对于鉴别重症患者呼吸功能恶化的原因具有重要作用。床旁检查技术,如超声或卧位胸部X光,对于真菌感染的早期发现、特征描述或监测所提供的信息不足。以下技术建议用于怀疑有或没有肺外表现的IPA。如果怀疑有血源性播散,可能需要对胸外区域进行进一步影像学检查,具体建议如下。
肺部:尽可能采用低剂量薄层CT检查。如果出现咯血,建议进行血管CT检查以调查可能的血管侵犯。对浸润的特征描述可以在一定程度上对基础病因进行分类,但不能替代微生物学诊断。如果出现新的症状、未能达到预期的改善或临床状况恶化,建议采用低剂量CT进行监测。
脑部:推荐的检查方式是使用造影剂的磁共振成像(MRI)。在急性情况下,特别是寻找出血时,应进行CT检查。如果CT检查结果无异常,且临床状况允许且无禁忌证,应增加MRI检查。
鼻窦:鼻窦侵袭性曲霉病可能症状不明显,在重症患者的临床检查中存在困难。因此,如有疑问,应进行CT或MRI检查。然而,MRI对于真菌团块侵入眼眶或大脑的可视化更为敏感。此外,对眼睛进行多次CT扫描可能会引发白内障,尤其是在年轻人中。
腹部:对于ICU患者,尽管MRI可能提供更多的信息,但由于患者难以多次屏气,其优势受到限制。因此,对于ICU患者,建议采用多期增强CT检查。
经皮CT引导活检:鉴于ICU患者病情危重,应在仔细评估风险和获益后进行活检。尽管如此,经皮CT引导活检是确认诊断的可靠方法,如果需要长期治疗和可能的二级预防,这可能优于经验性治疗。
随访:建议根据临床发展情况,在后续过程中个体化地重复影像学检查,以监测治疗反应。特别是在停止治疗之前,建议进行随访影像学检查。
支气管镜检查
ICU患者肺功能因病原体恶化的原因众多(分泌物、肺水肿、出血等)。除了其诊断作用外,支气管镜检查在ICU环境中通常也具有治疗意义。支气管镜检查期间呼吸功能恶化的风险通常较低,这就是为什么应在低阈值下对侵入性诊断进行检查,特别是在插管患者中。在气管支气管曲霉病的情况下,支气管镜检查具有直接可视化和进行针对性活检的优势。应对CT怀疑为IPA区域获得的支气管肺泡灌洗液(BALF)进行微生物培养、聚合酶链反应(PCR)和血清学检测。
培养
曲霉菌属(Aspergillus spp.)在ICU患者中,BALF培养阳性与IPA相关,在高达50%的患者中出现。此外,培养允许进行物种鉴定和表型耐药性测试,以识别唑类耐药菌株。然而,单独培养的敏感性较低,为20-50%,且无法区分定植和感染。
血清学
基于酶联免疫吸附试验(ELISA)的血清半乳甘露聚糖检测(GM试验)在中性粒细胞减少患者中显示出合理的测试性能。相比之下,在非中性粒细胞减少患者中,感染通常不是血管侵袭性的,该测试的敏感性要低得多。这就是为什么在非中性粒细胞减少的ICU患者中,半乳甘露聚糖检测应仅从呼吸道样本中进行。使用1.0 ODI截止值,一项多中心研究在ICU患者中显示出80%的敏感性和97%的特异性。床旁检测的侧流层析测定法也在ICU中进行了评估,具有类似的性能指标。
不推荐在重症监护病房中使用BALF检测β-D-葡聚糖(BDG)作为泛真菌生物标志物来诊断侵袭性肺曲霉病(IPA),因为其特异性低且存在假阳性结果。
核酸扩增技术(NAT)
已有研究描述了从血液(包括血浆、血清)和深部呼吸道样本中检测曲霉菌属(Aspergillus spp.)的分子检测方法,但目前对于这些方法在重症监护病房中的危重病患者中的益处证据尚不充分。此外,NAT无法区分定植和感染。然而,结合测序,它可以用于针对性检测cyp51A基因中与唑类耐药相关的突变(RAMs)。从BALF进行NAT的研究显示,即使在高危人群中,其敏感性和特异性也有限。然而,当PCR与检测真菌孢子活性(半乳甘露聚糖检测)相结合时,这一指标显著提高。在一项针对免疫受损患者的研究中,从血液中进行分子检测方法对于单次阳性检测结果的敏感性和特异性分别为79.2%和79.6%,而对于连续两次阳性检测结果的敏感性和特异性分别为59.6%和95.1%。
治疗
全身治疗
脂质体两性霉素B(LAmB)是ICU中治疗侵袭性肺曲霉病的另一种选择。LAmB也存在一定的肾毒性,可能会导致原有急性肾损伤的患者肾功能恶化,但通常是可逆的。当怀疑存在由当地流行病学引起的唑类耐药性时,或者当预计会发生与唑类药物相关的DDI时,也应经验性地使用LAmB作为初始治疗。其他可能的二线替代治疗选择包括泊沙康唑(PCZ)或棘白菌素类。棘白菌素类不应作为一线单药治疗使用。不过,如果别无选择,它们也可以与唑类抗真菌药物联合使用,作为挽救治疗的附加疗法。
吸入治疗
通常不推荐使用抗真菌药物的吸入疗法。尽管在某些个别情况下可能会在标签外使用,但在技术上非常复杂,尤其是在插管患者中。对于肺移植患者吻合口感染的情况,吸入治疗的证据最为充分。更多细节,请参阅德国呼吸学会关于抗菌药物吸入治疗的相关信息。
手术治疗
除了一些罕见的个别病例外,在ICU患者中手术治疗的使用是有限的。
药物相互作用
由于ICU患者不可避免地需要使用多种药物,DDI是常见问题,大约影响到30%使用抗霉菌活性抗真菌药物治疗的患者。
这些相互作用涉及代谢和清除的变化,最常由于唑类药物对细胞色素P450(CYP)的抑制作用;可能导致不良副作用的风险,以及对其他共用药物的减弱或增强作用。然而,在重症医学中,对药物相互作用进行个体化和跨学科的评估至关重要。这种评估应考虑临床背景、可获得的监测选项、潜在风险以及替代治疗的有效性。使用药物相互作用数据库作为一种筛查工具,特别是对于唑类治疗,是有益的,因为它们提供了关于剂量调整和药物相互作用管理的一般建议。下表总结了可能的药物相互作用及其对ICU常见处方药物代谢的影响。然而,这些不应被视为全面的,只能作为指导性参考。
|
药物类别 |
药物举例 |
相互作用描述 |
|
抗感染药 |
克拉霉素 |
↓代谢,↑大环内酯类(如QTc延长)的效果 |
|
利福平,利福布丁 |
↑唑类代谢,↓唑类暴露和↓唑类效果 |
|
|
化疗药物 |
环磷酰胺,异环磷酰胺,蛋白激酶抑制剂 |
↓代谢/外排,↑化疗药物的效果(如毒性) |
|
免疫抑制剂 |
钙调磷酸酶/mTOR抑制剂 |
↓代谢/外排,↑免疫抑制剂的效果和↑ 暴露 |
|
镇静剂 |
苯二氮卓类药物 |
↓代谢,↑苯二氮卓类药物的效果 |
|
镇痛药 |
阿片类药物 |
↓代谢,↑阿片类药物的效果 |
|
抗惊厥药 |
苯妥英,卡马西平 |
↓唑类代谢,↓唑类暴露和↓唑类效果 |
|
神经精神类药物 |
喹硫平,氟哌啶醇 |
↓代谢,↑神经精神类药物的效果(如QTc延长) |
|
心脏药物 |
胺碘酮,钙通道阻滞剂,地高辛,伊伐布雷定 |
↓代谢,↑心脏药物的效果(如QTc延长) |
|
HIV治疗药物 |
利托那韦,依非韦伦 |
复杂的相互作用(抑制剂/底物),可能↓唑类效果 |
|
口服抗凝药 |
口服抗Xa抑制剂,苯丙香豆素 |
↓代谢,↑抗凝药的效果 |
治疗药物监测(TDM)
伏立康唑
由于伏立康唑的消除过程是非线性的,因此其在个体内部和个体之间表现出显著的药代动力学变异性。除了药物相互作用外,细胞色素P450(CYP)2C19酶的多态性也可能导致伏立康唑浓度的波动。多项研究表明,伏立康唑血清浓度与疗效之间存在相关性。因此,根据系统综述和最近的荟萃分析,目前推荐的治疗目标范围为1-5.5 mg/L。对于患有严重感染(例如多灶性或播散性感染)、中枢神经系统受累以及由具有较高MIC的病原体引起的感染的患者,建议将目标范围提高至2-6 mg/L。超过治疗范围的伏立康唑浓度与神经毒性和肝毒性有关,一项荟萃分析确定,伏立康唑水平>6 mg/L是毒性的强预测因子。伏立康唑浓度最好在治疗的前5天内进行监测,并在调整剂量后4天重复监测。
艾沙康唑
泊沙康唑
在对接受泊沙康唑用于预防或IPA治疗的患者进行的回顾性分析中,低泊沙康唑浓度的患者更常出现突破性感染以及对治疗的反应降低。此外,在一项前瞻性研究中,泊沙康唑TDM对减少突破性感染产生了积极影响。
对于IPA的治疗,实现泊沙康唑平均浓度1.25 mg/L可改善接受泊沙康唑挽救治疗患者的反应率。在ICU患者中,多达35%的测量泊沙康唑浓度低于IPA治疗的目标范围。值得注意的是,泊沙康唑在支气管肺泡液中的浓度可达到血浆中的40倍。这一观察结果或许可以解释为什么一些研究未能证明低泊沙康唑血浆浓度与治疗失败之间存在相关性,因为尽管全身水平较低,但肺部药物渗透可能仍然足够。然而,目前可用的指南建议将泊沙康唑的谷浓度维持在>1 mg/L,以治疗IPA。为避免毒性(包括肝毒性和假性低醛固酮症的发展),正在讨论设定2或4 mg/L的上限。如果进行TDM,建议在治疗的第5-7天进行,尽管根据结果和临床背景可能需要进一步监测。
脂质体两性霉素B
除了临床前药代动力学/药效学研究外,对于ICU中患有IPA的患者,尚无明确的LAmB目标水平数据,而且由于LAmB在组织和血清中的不同动力学以及在肺组织中的积累,情况进一步复杂化。因此,目前不推荐进行TDM。
棘白菌素类
由于大多数可用数据基于念珠菌病的动物模型而非IPA,因此目前不推荐对棘白菌素类进行TDM。
▌参考文献:
Wichmann D, Hoenigl M, Koehler P, et al. Diagnosis and treatment of invasive pulmonary aspergillosis in critically ill intensive care patients: executive summary of the German national guideline (AWMF 113-005). Infection. Published online June 4, 2025. doi:10.1007/s15010-025-02572-2
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
