- 首页 > 正文
告别“无药可用”,又一BL/BLI新药在国内获批!
感染医线 发表时间:2025/7/2 11:52:41
编者按:2025年6月30日,国家药品监督管理局(NMPA)官网最新信息显示,辉瑞投资有限公司的注射用氨曲南阿维巴坦钠(以下简称:氨曲南/阿维巴坦)已正式在国内获批[1],用于治疗由革兰阴性菌引起的治疗选择有限或无替代治疗的成人复杂性腹腔内感染(cIAI),医院获得性肺炎(HAP),包括呼吸机相关性肺炎(VAP)[2]。

药物概览
氨曲南/阿维巴坦属于β-内酰胺类/β-内酰胺酶抑制剂复方制剂。其中,氨曲南为单环β-内酰胺类药物,通过抑制细菌细胞壁的合成发挥抗菌作用,其对革兰阴性菌具有良好抗菌活性,且对多种β-内酰胺酶有较好耐受性;阿维巴坦作为β-内酰胺酶抑制剂,对Ambler A类、C类和D类酶中的OXA-48酶具有抑酶活性[3]。
体外研究显示,氨曲南/阿维巴坦对所有肠杆菌目细菌表现出强大的抗菌活性(MIC90:0.25 mg/L),对多重耐药菌株、产超广谱β-内酰胺酶菌株及碳青霉烯耐药菌株保持高敏感率(>99%)和良好活性(MIC90:0.25~0.5 mg/L);值得注意的是,其对产金属β-内酰胺酶(MBL)菌株及产其他碳青霉烯酶(如KPC和OXA-48)菌株同样具有良好的抗菌活性(敏感率>99.0%,MIC90:0.5 mg/L)[4]。
REVISIT研究
REVISIT研究评估了氨曲南/阿维巴坦治疗由革兰阴性菌引起(或疑似引起)的复杂性腹腔内感染(cIAI)或医院获得性肺炎/呼吸机相关肺炎(HAP/VAP)的安全性和有效性[5]。患者以2:1的比例分配至氨曲南/阿维巴坦组(cIAI患者联用甲硝唑)或美罗培南组(联合或不联合黏菌素)。治疗疗程:cIAI为5~14天,HAP/VAP为7~14天。主要终点是意向治疗(ITT)人群在临床治愈访视时(第28天前后3天内)的临床治愈率。次要终点包括ITT人群的28天死亡率,以及ITT人群中接受研究药物治疗患者的安全性。
共筛选了461例患者。最终入组并随机分配了422例患者(氨曲南/阿维巴坦组282例,美罗培南组140例,组成ITT分析集)。最常见的基线病原体是肠杆菌目细菌(252/271,93%)。接受碳青霉烯酶检测的80株分离株中,19株(24%)呈碳青霉烯酶阳性(丝氨酸酶、金属β-内酰胺酶或二者均有)。
在临床治愈访视时,氨曲南/阿维巴坦组和美罗培南组的临床治愈率分别为68.4%(193/282)和65.7%(92/140),治疗差异为2.7%(95%CI:-6.6~12.4)。在cIAI患者中,两组经校正的临床治愈率分别为76.4%(159/208)和74.0%(77/104)。在HAP/VAP患者中,两组的治愈率则分别为45.9%(34/74)和41.7%(15/36)。
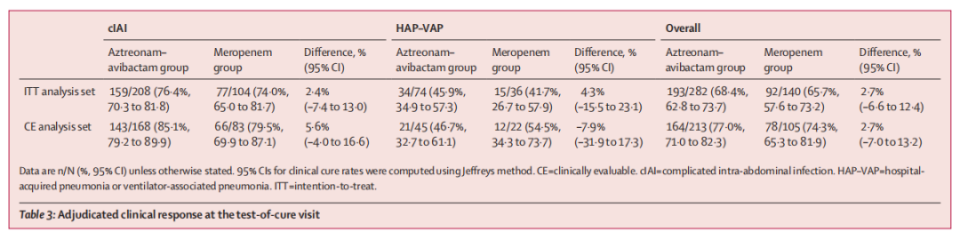
△治愈访视时的校正临床治疗反应(按感染类型)
28天全因死亡率方面,氨曲南/阿维巴坦组为4%(12/282),美罗培南组为7%(10/140);在cIAI患者中,死亡率分别为2%(4/208)和3%(3/104);在HAP/VAP患者中,死亡率分别为11%(8/74)和19%(7/36)。
氨曲南/阿维巴坦总体耐受性良好,安全性特征与已知的氨曲南单药治疗安全性特征一致。氨曲南/阿维巴坦组未发生与治疗相关的严重不良事件。
ASSEMBLE研究
ASSEMBLE研究旨在评估氨曲南/阿维巴坦对比最佳可用疗法(BAT)在治疗由产MBL革兰氏阴性菌引起的cIAI、院内肺炎(NP,包括HAP和VAP)、复杂性尿路感染(cUTI)或血流感染(BSI)中的疗效、安全性和耐受性[6]。研究纳入了15例成人住院患者,结果显示,在治愈访视时,氨曲南/阿维巴坦的临床治愈率为41.7%(5/12),BAT组为0%(0/3)。
基于上述研究成果,美国食品药品监督管理局(FDA)于当地时间2025年2月7日批准氨曲南/阿维巴坦与甲硝唑联合使用,用于治疗由敏感革兰阴性菌(大肠埃希菌、肺炎克雷伯菌、产酸克雷伯菌、阴沟肠杆菌复合体、弗氏柠檬酸杆菌复合体和黏质沙雷菌)引起的治疗药物选择有限或无替代治疗的18岁及以上患者的cIAI。
表. 美国FDA制定的氨曲南/阿维巴坦折点标准[7]
|
_ |
最低抑菌浓度 (浓度,mcg/mL) |
纸片扩散法 (直径,mm) |
||||
|
病原体 |
S |
I |
R |
S |
I |
R |
|
肠杆菌目细菌 |
≤4/4 |
8/4 |
≥16/4 |
≥21 |
18~20 |
≤17 |
S:敏感;I:中介;R:耐药
参考文献
[1] 国家药品监督管理局. 2025年06月30日药品批准证明文件送达信息. Available from: https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20250630161536179.html
[2] 辉瑞制药. 辉瑞新型抗菌药物思福诺®在华获批,用于多重耐药性感染和治疗药物选择有限的患者. Available from: https://mp.weixin.qq.com/s/xB1E8uXxQ4bWt0oT22JiFg
[3] 《β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂临床应用专家共识》编写专家组.β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)[J].中华医学杂志,2020,100(10):738-747.DOI:10.3760/cma.j.cn112137-20200202-00178.
[4] Rossolini GM, Stone G, Kantecki M, Arhin FF. In vitro activity of aztreonam/avibactam against isolates of Enterobacterales collected globally from ATLAS in 2019. J Glob Antimicrob Resist. 2022;30:214-221. doi:10.1016/j.jgar.2022.06.018
[5] Carmeli Y, Cisneros JM, Paul M, et al. Aztreonam-avibactam versus meropenem for the treatment of serious infections caused by Gram-negative bacteria (REVISIT): a descriptive, multinational, open-label, phase 3, randomised trial. Lancet Infect Dis. Published online October 7, 2024. doi:10.1016/S1473-3099(24)00499-7
[6] Efficacy, Safety, and Tolerability of ATM-AVI in the Treatment of Serious Infection Due to MBL-producing Gram-negative Bacteria. [Internet]. 2025 [cited 2025 July 1]. Available from: https://clinicaltrials.gov/study/NCT03580044
[7] U.S. FOOD & DRUG ADMINISTRATION. Aztreonam and Avibactam Injection. Available from: https://www.fda.gov/drugs/development-resources/aztreonam-and-avibactam-injection
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
