- 首页 > 正文
IDSA新冠指南更新对英夫利西单抗的建议,一文捋清重症患者的免疫调节/抗炎治疗
感染医线 发表时间:2025/8/23 9:03:47
编者按:重症或危重症COVID-19患者往往存在细胞因子风暴导致的全身炎性反应,临床可使用不同靶点的免疫调节或抗炎药物。近日,美国感染病学会(IDSA)COVID-19诊疗指南更新了英夫利西单抗在成人重症或危重型COVID-19住院患者中的应用建议[1]。
对于因重症或危重型COVID-19住院且正在接受全身性糖皮质激素治疗的患者,是否应在标准治疗基础上加用英夫利西单抗?
建议:对于正在接受全身性糖皮质激素治疗且病情严重、快速进展*或危重型**COVID-19住院成人患者,当巴瑞替尼(baricitinib)和托珠单抗(tocilizumab)不可用时,IDSA指南专家组建议使用英夫利西单抗(infliximab)而非不使用该药物(有条件推荐,证据确定性低)。
*病情严重且快速进展的定义为:在室内空气条件下血氧饱和度≤94%(包括需要辅助供氧的患者),且在全身性糖皮质激素治疗后病情仍持续恶化。
**危重型疾病定义为:需要高流量鼻导管吸氧/无创通气或有创机械通气或ECMO支持的患者。
英夫利西单抗是一种靶向肿瘤坏死因子α(TNF-α)的嵌合型单克隆抗体。TNF-α是一种主要由活化巨噬细胞、淋巴细胞和自然杀伤细胞产生的促炎细胞因子。通过中和TNF-α,英夫利西单抗能有效减轻炎症反应和免疫系统过度激活,因此被用于治疗自身免疫性和炎症性疾病。该药物已在国内外获批治疗克罗恩病、溃疡性结肠炎、类风湿关节炎、银屑病关节炎、强直性脊柱炎和斑块型银屑病等免疫性疾病。
COVID-19疫情初期,研究证实白细胞介素6(IL-6)和TNF-α水平升高是疾病严重程度和生存率的独立预测因子[2]。多项队列研究还发现,与使用非TNF-α生物制剂的患者相比,接受TNF-α抑制剂治疗的患者因COVID-19住院和发生重症的风险更低[3-4]。尽管英夫利西单抗尚未获得美国FDA批准用于COVID-19治疗,但ACTIV-1等临床试验[5]已就其管理重症COVID-19相关炎症(如细胞因子风暴)的潜在作用开展了研究。
英夫利西单抗在国内同样尚未获批COVID-19相关适应症,但在国家卫健委印发《新型冠状病毒感染诊疗方案(试行第十版)》中,英夫利西单抗或托珠单抗被推荐用于丙种球蛋白和激素治疗无好转或加重的儿童多系统炎症综合征(MIS-C)患者。
目前,已有多个不同靶点的小分子TKI或大分子单抗被用于治疗重症和危重症COVID-19患者的过度免疫反应(即“细胞因子风暴”)[6-7]。
|
药物名称 |
主要分类 |
作用靶点 |
在COVID-19治疗中的地位 |
|
托珠单抗 |
IL-6抑制剂 |
IL-6受体 |
首选/一线药物(与糖皮质激素联用) |
|
巴瑞替尼 |
JAK抑制剂 |
JAK1/JAK2 |
首选/一线药物(与糖皮质激素联用) |
|
托法替布 |
JAK抑制剂 |
JAK1/JAK3 |
替代选择(当一线药物不可用时) |
|
英夫利西单抗 |
TNF-α抑制剂 |
TNF-α |
替代选择(当一线药物不可用时) |
01
托珠单抗
使用指征与时机:
(1)托珠单抗建议用于正接受全身糖皮质激素治疗并需要吸氧、无创或有创机械通气或体外膜肺氧合(ECMO)支持的住院成年新冠感染患者。
(2)建议在入住ICU后24h内或普通病房72h内尽早应用托珠单抗。
实验室指标的监测:
(1)开始治疗前,应检查血常规及肝功能(包括中性粒细胞计数、血小板、转氨酶和总胆红素)及炎症相关指标(IL-6、CRP、铁蛋白)。
(2)治疗期间,还应监测所有患者继发感染相关风险(降钙素原、GM试验、T-spot试验等)及凝血功能。
(3)结束治疗后,应当监测继发感染相关风险指标,早期发现继发细菌、真菌、结核感染。
肾功能不全及CRRT患者的剂量调整:
(1)对于CrCL≥30 mL·min-1的患者暂无需调整托珠单抗剂量。
(2)对于CrCL<30 mL·min-1的患者是否需调整托珠单抗的剂量缺乏研究,若无替代方案必须使用时需权衡风险与获益后谨慎使用,建议按常规剂量给药,同时监测患者肾功能及药物不良反应。
(3)CRRT患者使用托珠单抗无需调整剂量。
肝功能不全患者的剂量调整:
托珠单抗在使用前应当评估肝功能,若ALT/AST>10倍正常值上限不应使用托珠单抗治疗,若无禁忌症的情况下单次使用可不调整剂量。
疗效评估:
托珠单抗治疗后的IL-6水平不能作为其疗效不佳的依据,应用托珠单抗治疗后应当根据临床症状(如氧合指数、血气分析等)及影像学变化来评估疗效。
药物相互作用:
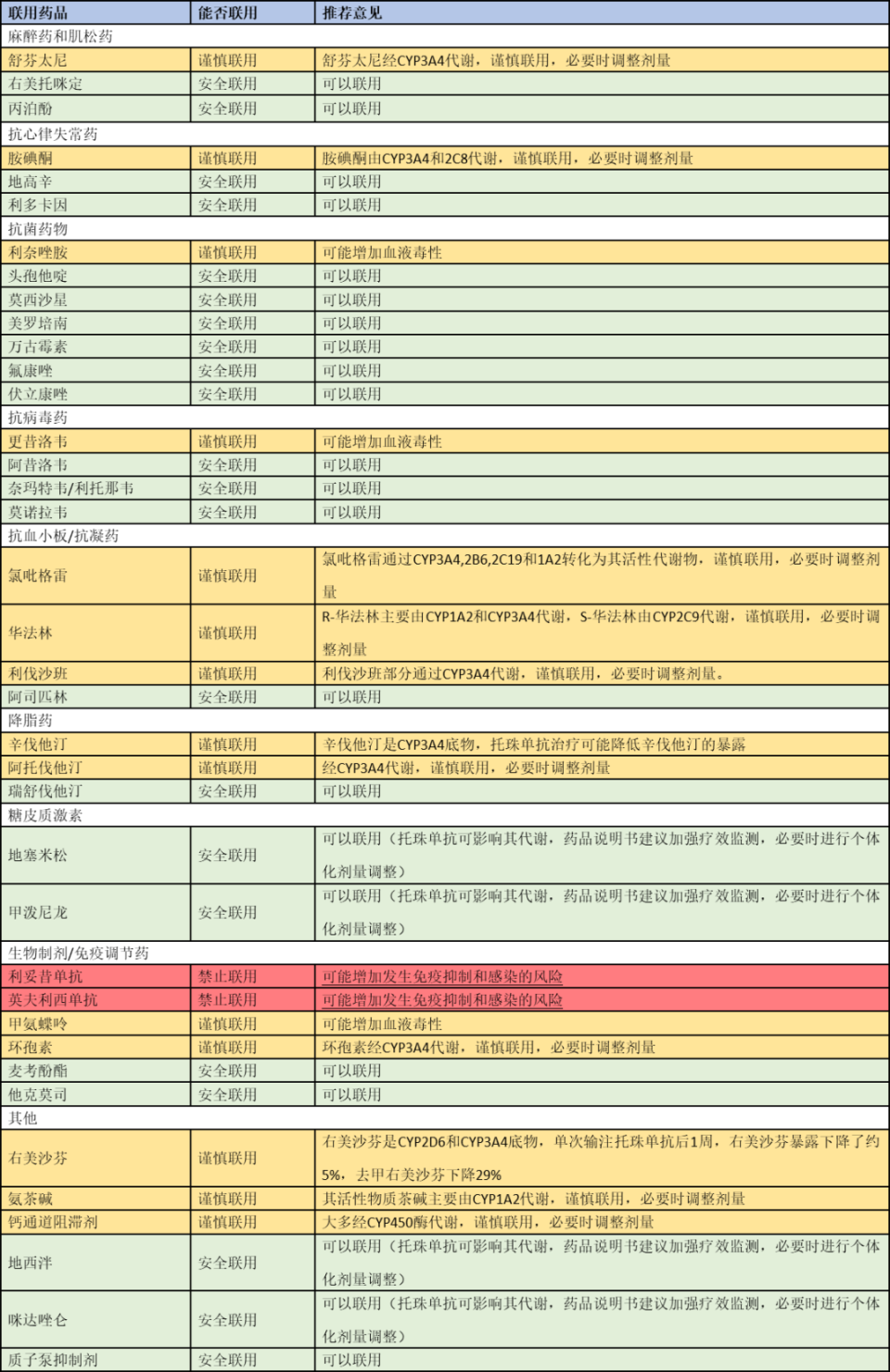
其他问题和建议:
静脉用托珠单抗短缺时可以考虑使用皮下用托珠单抗替代。
托珠单抗单次使用效果不佳的情况下,可以重复给药。累计给药次数最多为2次,单次最大剂量不超过800mg。
托珠单抗可以与激素联合应用。对于应用托珠单抗治疗效果不佳的重症或危重症COVID-19患者,可以考虑联合应用巴瑞替尼,但需密切关注两药合用可能存在的二次感染风险。不推荐托珠单抗与托法替布联合应用。
02
巴瑞替尼
使用指征与时机:
巴瑞替尼适用于需要辅助供氧、无创或有创机械通气、或ECMO的COVID-19成人住院患者。应与糖皮质激素联用。
不推荐巴瑞替尼用于以下患者:
(1)活动性结核患者;(2)绝对淋巴细胞计数(ALC)<200细胞/µL或绝对中性粒细胞计数(ANC)<500细胞/µL;(3)对于新冠感染伴有其他感染的患者应权衡利弊后使用。
使用方法:
巴瑞替尼片4mg,口服,每日一次,餐时或空腹均可,连续使用至氧合改善,最长不超过14天。用药期间应检测绝对淋巴细胞计数(ALC)与绝对中性粒细胞计数(ANC),如ALC<200细胞/µL或ANC<500细胞/µL时应终止治疗,直到恢复后继续开始使用。由于老年患者更有可能出现肾功能减退,因此在选择剂量时应更加谨慎,并对肾功能进行监测。
肝功能剂量调整:
在轻度或中度肝功能损伤的患者中无须进行剂量调整;原则上不推荐在重度肝功能损伤的患者中使用巴瑞替尼。
巴瑞替尼的国内药品说明书不推荐在肌酐清除率<30 mL/min的患者中使用,但在美国和日本的说明书中,提供了肾功能不全患者(包括eGFR<30 mL·min-1)相应的推荐用法用量。
结合国外相关说明书及巴瑞替尼的药理学特性,推荐如下:

药物相互作用:
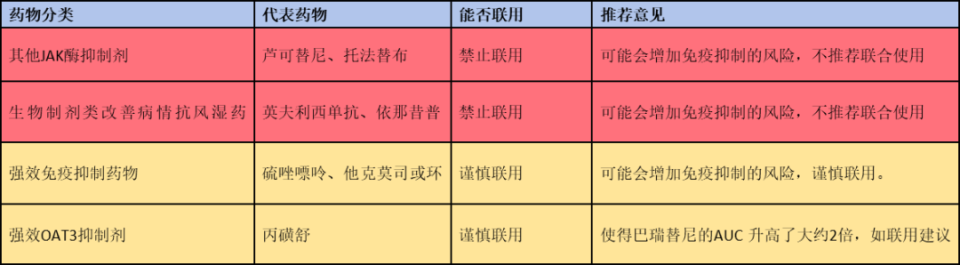
不良反应监测:
建议在巴瑞替尼使用过程中监测全血细胞计数和分类、肝肾功能及新发感染(继发细菌及真菌感染、单纯疱疹病毒、带状疱疹感染等)。加强监测凝血功能,及时评估是否出现血栓相关体征,必要时采用治疗剂量抗凝。
巴瑞替尼片在患者无法吞服的情况下,可以鼻饲给药,操作步骤:
(1)操作人员佩戴N95口罩,将4mg巴瑞替尼片放入研钵中碾碎。取50ml注射器,抽出活塞推杆,手指抵住注射器尖端,将药片粉末倒入注射器中;
(2)用注射器抽取约30mL温水,轻轻摇晃,确保药片充分分散,可以通过注射器的尖端,立即打入鼻胃管/鼻肠管。为避免管子堵塞,在给药过程中,可以保持注射器水平并摇晃;
(3)给药完成后,用至少15ml的温水进行冲管。
03
托法替布
使用指征与时机:
当托珠单抗、巴瑞替尼不可及时,托法替布可作为替代治疗方案,联合糖皮质激素用于需要吸氧的住院患者。
以下患者不推荐使用托法替布:
(1)绝对淋巴细胞计数(ALC)<500细胞/mm3,绝对中性粒细胞计数(ANC)<1000细胞/mm3,血红蛋白低于9g/dL;(2)严重活动性感染(包括局部感染);(3)严重肝功能不全。
使用方法:
托法替布片10 mg/次,每天2次,连续使用至氧合改善,最长不超过14天。用药期间建议监测血常规、肝酶及是否有继发感染。在治疗前和治疗期间推荐检测潜伏性结核病。由于老年人用药后的感染率普遍较高,因此老年人应谨慎使用。
肝肾功能损伤、透析及CRRT患者的剂量调整:

药物相互作用:
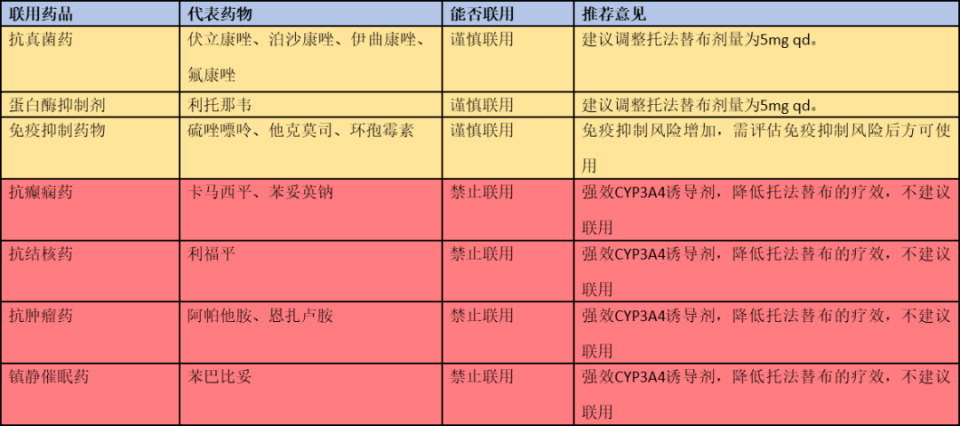
不良反应监测:
托法替布与治疗COVID-19相关的常见不良反应包括急性呼吸衰竭、感染、转氨酶增加、贫血、急性肾损伤、高血糖、淋巴瘤、肝衰竭、高钾血症等。使用托法替布期间需要监测患者肝肾功能、血常规、血糖、电解质水平和新出现感染,包括体温、CRP、PCT及培养结果等。
托法替布片在患者无法吞服的情况下,可以鼻饲给药,操作步骤:
(1)操作人员佩戴N95口罩,将10mg托法替布片放入研钵中碾碎,取50ml注射器,抽出活塞推杆,手指抵住注射器尖端,将药片粉末倒入注射器中;
(2)用注射器抽取约30mL温水,轻轻摇晃,确保药片充分分散,可以通过注射器的尖端,立即打入鼻胃管/鼻肠管。为避免管子堵塞,在给药过程中,可以保持注射器水平并摇晃;
(3)给药完成后,用至少15ml的温水进行冲管。
04
英夫利西单抗
治疗MIS-C的用药指征:
(1)英夫利西单抗适用于丙种球蛋白(IVIG)和糖皮质激素治疗24小时内无临床改善的难治性儿童多系统炎症综合征(MIS-C),或无法长期使用糖皮质激素的患儿。
(2)不建议用于伴有巨噬细胞活化综合征的MIS-C患儿。
推荐剂量:
5-10 mg/kg ivgtt,推荐使用一剂。
注射剂配置方法:
10 mL的注射用无菌水复溶每个100mg英夫利西单抗小瓶,获得10 mg/mL的浓度。复溶的溶液静置5 min,检查溶液是否有颗粒物和变色。重新配制的溶液应为无色至浅黄色和乳白色。若冻干粉未完全溶解或存在不透明颗粒、变色或其他异物颗粒,请勿使用。用无菌0.9%氯化钠注射液(不要用任何其他稀释剂稀释)将复溶的英夫利西单抗溶液的总体积稀释至250 mL。英夫利西单抗输注应在复溶和稀释后3 h内开始。输液必须使用带有过滤器(孔径为1.2 µm或更小)的输液器进行静脉内给药至少2 h。具体使用流程可参见流程图。
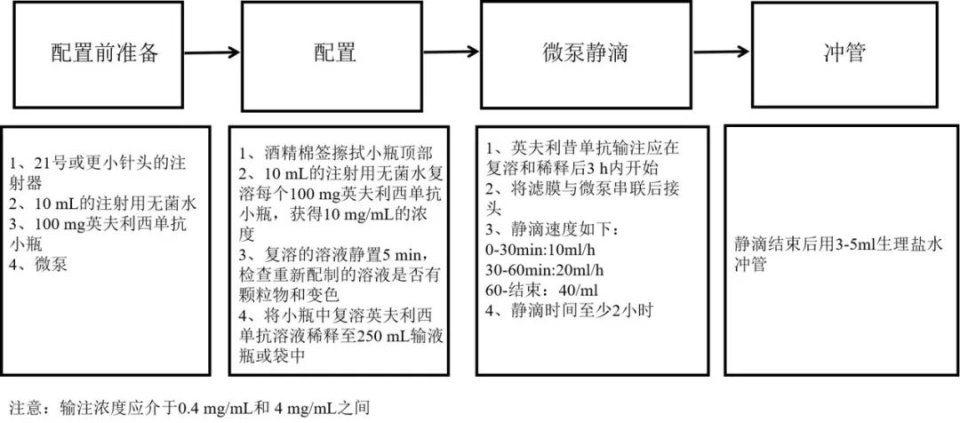
△英夫利西单抗注射剂配置流程
肝损伤风险:
英夫利西单可能导致严重的肝脏不良反应,使用前应评估肝功能情况,如患者合并黄疸和/或显著的肝酶增高(≥5倍的正常范围上限),不建议使用英夫利西单抗。
不良反应:
儿童严重不良反应的发生类型和成人相似,包括乙型肝炎病毒(HBV)再激活、充血性心力衰竭(CHF)、严重感染(包括脓毒症、机会性感染和结核病)、血清病(迟发性超敏反应)、血液系统反应、系统性红斑狼疮/狼疮样综合征、脱髓鞘性疾病、肝胆事件、淋巴瘤、肝脾T细胞淋巴瘤(HSTCL)、白血病、Merkel细胞癌、肠道或肛周脓肿(在克罗恩病中)和严重的输液反应。儿童最常见的不良反应为上呼吸道感染和咽炎、头痛。其他常见不良反应为输液反应、贫血、中性粒细胞减少症、白细胞减少症、贫血、淋巴结病、抑郁、失眠、头晕、心悸、血压改变等。
建议首次输注前筛查:
①结核(T-SPOT,PPD试验,胸部CT);②肝炎(乙肝,丙肝);③EB病毒(包括EB-IgM、EB-IgG及EB-DNA)等。用药过程中监测全血细胞计数、淋巴细胞计数、肝功能、超敏C反应蛋白、血沉等。
药物相互作用:
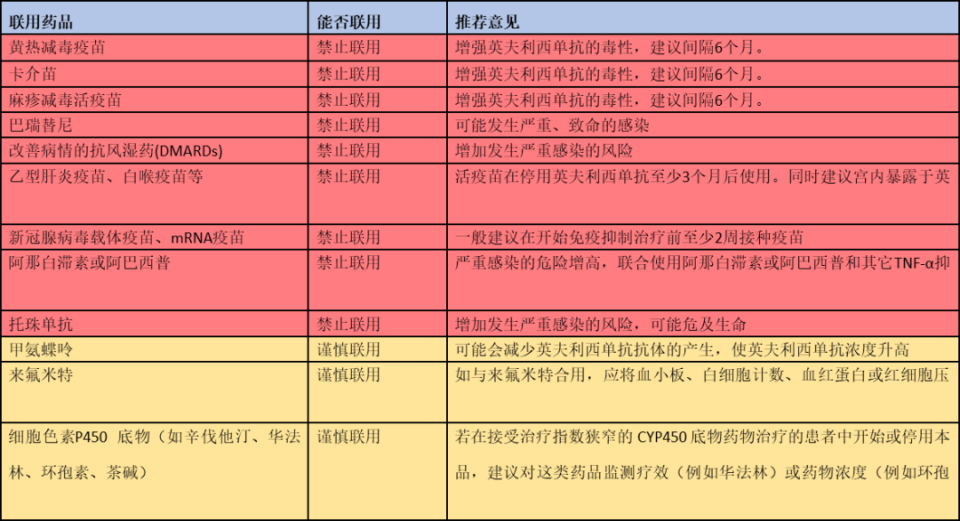
参考文献
[1] Bhimraj A, Falck-Ytter Y, Baden LR, et al. 2025 Clinical Practice Guideline Update by the Infectious Diseases Society of America on the Treatment and Management of COVID-19: Pemivibart for Pre-exposure Prophylaxis, Vilobelimab for Critical Illness, and Abatacept or Infliximab for Severe or Critical Illness. Clin Infect Dis. Published online August 4, 2025. doi:10.1093/cid/ciaf424
[2] Del Valle DM, Kim-Schulze S, Huang HH, et al. An inflammatory cytokine signature predicts COVID-19 severity and survival. Nat Med 2020; 26:1636–43.
[3] Curtis JR, Zhou X, Rubin DT, et al. Characteristics, comorbidities, and outcomes of SARS-CoV-2 infection in patients with autoimmune conditions treated with systemic therapies: a population-based study. J Rheumatol 2022; 49:320–9.
[4] Izadi Z, Brenner EJ, Mahil SK, et al. Association between tumor necrosis factor inhibitors and the risk of hospitalization or death among patients with immune-mediated inflammatory disease and COVID-19. JAMA Netw Open 2021; 4:e2129639.
[5] O’Halloran JA, Ko ER, Anstrom KJ, et al. Infliximab, cenicriviroc, or infliximab for treatment of adults hospitalized with COVID-19 pneumonia. JAMA 2023; 330:328–39.
[6] 浙江省新型冠状病毒感染临床用药建议
[7] 新型冠状病毒感染诊疗方案(试行第十版)
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
