- 首页 > 正文
《柳叶刀》子刊丨HIV感染女性宫颈癌筛查:25岁启动,每3-5年1次
感染医线 发表时间:2026/1/16 20:14:30
编者按:宫颈癌是严重威胁女性健康的公共卫生问题,在HIV感染女性中呈现更高的发病风险与更严峻的疾病负担。HIV感染会显著削弱免疫系统,导致女性更易持续感染高危型人乳头瘤病毒(HPV),其宫颈癌前病变(CIN)更不易自行消退,且进展为浸润性宫颈癌(ICC)的风险比HIV阴性女性高出六倍。因此,为这一高危群体制定科学、精准的筛查策略,是迈向世界卫生组织(WHO)提出的“消除宫颈癌”目标的关键一步。
长期以来,基于有限证据,指南建议HIV感染女性在确诊HIV并开始性生活后即启动筛查,这可能导致许多青少年很早就接受筛查和治疗,而青春期HPV感染自然清除率高,过早干预可能带来不必要的生殖健康风险(如远期早产风险)。为此,由世界卫生组织牵头的一项大规模研究应运而生。该研究通过系统文献回顾和个体患者数据荟萃分析(IPDMA),深入探究了三个核心问题:HIV感染女性应从何时开始筛查?筛查结果为阴性后,隔多久复查?治疗后,又应如何安排随访?该研究结果发表于The Lancet HIV。
宫颈癌是全球女性健康的重大威胁,2022年全球新增确诊病例约66万例,死亡35万例,其中中低收入国家(LMICs)因诊断延迟、医疗资源匮乏,死亡率显著高于高收入国家,撒哈拉以南非洲地区占全球死亡病例的五分之一。值得关注的是,HIV感染女性的宫颈癌发病风险是普通女性的6倍,其核心机制包括HPV感染持续率升高、癌前病变自然消退率降低、病变进展速度加快以及治疗后复发风险增加。随着抗逆转录病毒治疗(ART)的普及,HIV感染女性的预期寿命延长,宫颈癌已成为该人群重要的远期并发症之一,2023年全球约2100万HIV感染女性需要宫颈癌预防服务。
2020年,WHO成员国通过《加速消除宫颈癌全球战略》,设定了每10万女性宫颈癌发病率低于4例的消除目标,而筛查与治疗癌前病变是短期内降低发病率的关键措施。此前2013年WHO指南建议HIV感染女性在确诊HIV并开始性生活后即启动宫颈癌筛查,但这一建议缺乏年龄特异性数据支持。青少年和年轻女性的HPV感染多可自然清除,且消融或切除治疗的安全性数据有限,过度筛查可能增加早产等生殖健康风险。因此,亟需通过高质量研究明确HIV感染女性的最优筛查起始年龄、筛查间隔及治疗后随访策略,为指南更新提供循证依据。
研究方法
研究者对宫颈癌与HIV相关研究进行了系统文献综述,检索了MEDLINE、Embase、CENTRAL、Cochrane图书馆及临床试验注册库,检索时间范围为2012年1月1日至2019年10月13日,并补充了此前一项覆盖数据库建库至2012年7月的系统综述数据。
纳入的研究需报告原始数据,并评估感染HIV女性中与宫颈癌前病变及宫颈癌相关的一项或多项结局指标,对研究设计或研究场景无限制。排除未纳入任何HIV感染女性的研究,或仅报告HPV基因型流行率而无其他相关数据的研究。
两名研究者按年龄提取了所有报告宫颈癌筛查结果及经组织病理学证实的疾病结局的研究数据。研究分析了关于最佳筛查年龄和筛查间隔的汇总数据,在可能的情况下提供合并估计值;随后进行了个体患者数据荟萃分析(IPDMA),以分析宫颈癌及癌前病变的年龄特异性数据。研究者邀请了包含40名及以上HIV感染且合并2级及以上宫颈上皮内瘤变(CIN2+)女性的研究作者提交个体患者数据用于荟萃分析。采用随机效应模型计算不同年龄、HIV感染状态及抗逆转录病毒治疗(ART)状态下宫颈癌筛查结果的预测概率。
研究结果
(一)研究人群特征
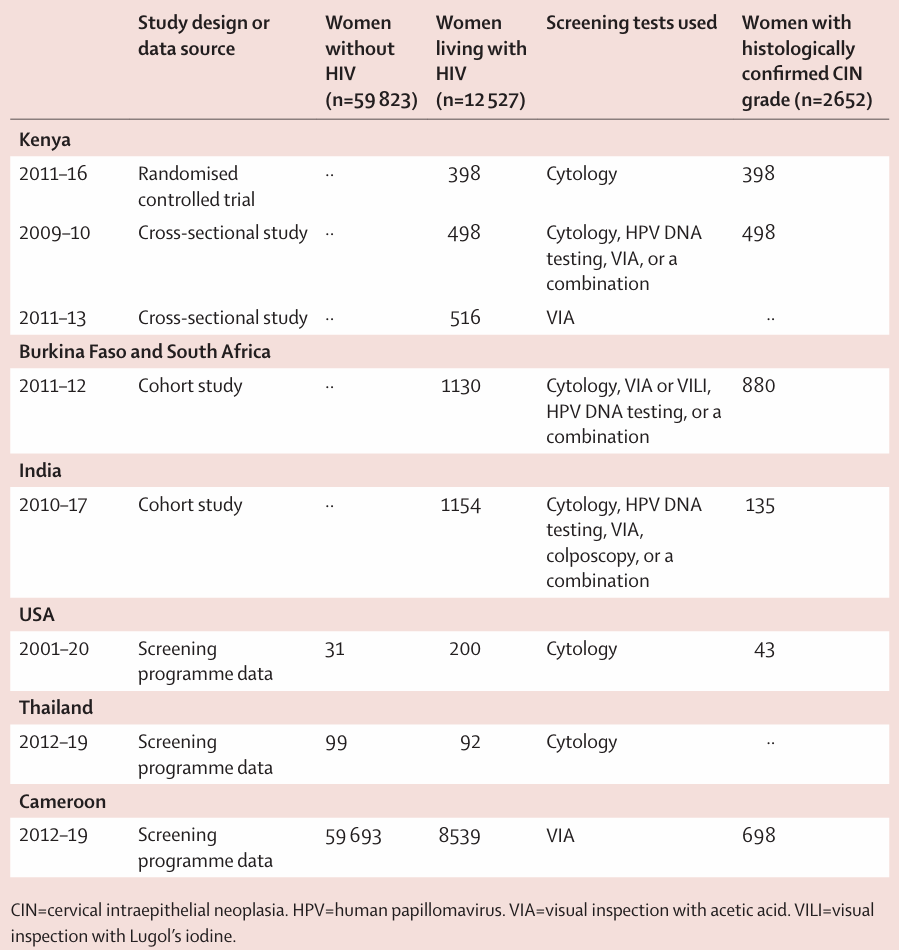
系统综述纳入34项研究,涵盖12个国家的128 732名女性,其中HIV感染女性63 790名,研究设计包括3项随机对照试验、19项前瞻性队列研究、6项回顾性队列研究、3项横断面研究和3项病例对照研究,随访时间6个月至84个月。IPDMA最终纳入72 350名女性,其中HIV感染女性12 527名(17.3%),筛查方法包括细胞学检查、HPV DNA检测、醋酸染色肉眼观察(VIA)等,2 652名女性获得组织病理学确认,其中HIV感染女性1 951名(73.6%)(表1)。
表1. HIV感染女性宫颈癌预防筛查相关个体患者数据荟萃分析纳入的按国家和年份分类的数据来源说明
CIN=宫颈上皮内瘤变;HPV=人乳头瘤病毒;VIA=醋酸染色肉眼观察法;VILI=卢戈氏碘液肉眼观察法
(二)年龄特异性病变分布
IPDMA的分析结果清晰地描绘了HIV感染女性中高级别癌前病变(CIN2/3)风险的年龄分布图谱。数据显示,宫颈高级别病变的风险呈现出明确的随年龄增长而上升的趋势。15-19岁年龄组预测概率仅为6.0%(95%CI:0.74-64.1),20-24岁升至32.4%(95%CI:8.3-72.7),25-29岁达42.1%(95%CI:16.4-80.2),30-34岁进一步升至50.3%(95%CI:16.3-80.0),45-49岁达到峰值58.1%(95%CI:17.0-81.5),50岁及以上仍维持在55.3%(95%CI:21.0-86.6)。
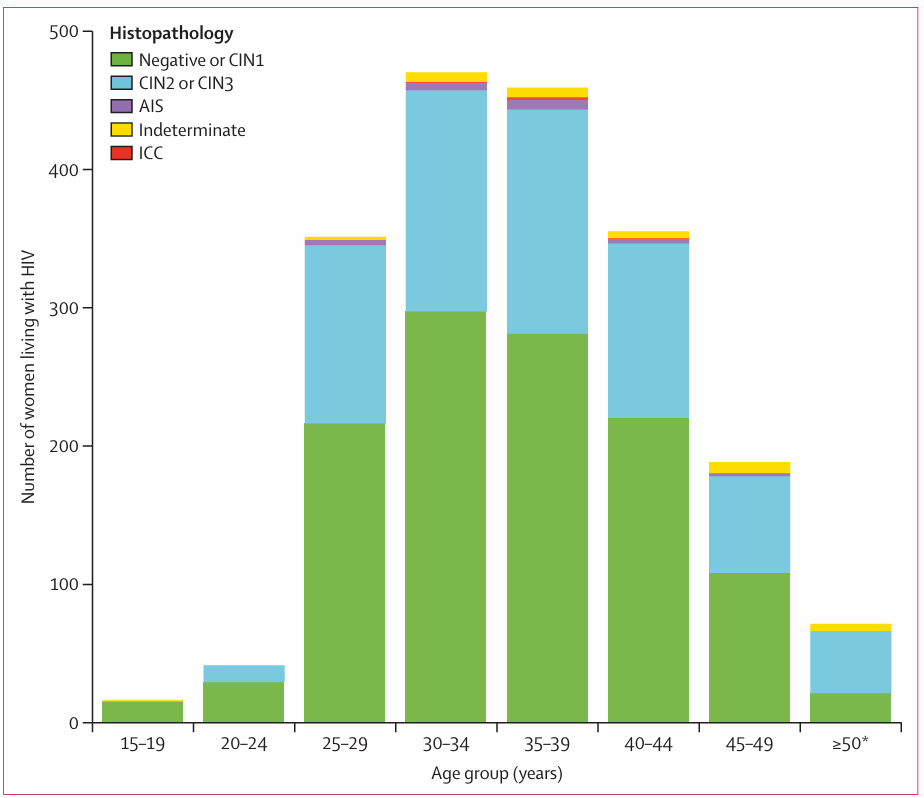
图1. 基于个体患者数据荟萃分析的HIV感染女性按年龄分层的经组织病理学证实的宫颈癌筛查结果分布
(AIS=宫颈原位腺癌;CIN=宫颈上皮内瘤变;ICC=浸润性宫颈癌。*本研究纳入的最大年龄为66岁)
浸润性宫颈癌的年龄分布特征更为明确:系统综述与IPDMA均显示,30岁以下HIV感染女性中浸润性宫颈癌罕见,发病率在30-49岁达到高峰,60岁以后逐渐下降。例如,南非一项基于全国癌症登记数据的研究显示,20-29岁HIV感染女性宫颈癌比例仅为5%,而30-50岁年龄组比例显著升高。
(三)筛查间隔相关结果
对于基线细胞学阴性且HPV阴性(双重阴性)的HIV感染女性,系统综述显示其CIN2+的累积发病率在4.2-6.4年内为0.8%-5%,12年内任何级别CIN的累积发病率高达10%。若基线细胞学阴性但HPV阳性,病变风险显著升高:1-3年病变发生率为1.0%-5.0%,4.2-6.4年升至4.2%-14.5%,12年达15.2%,其中HPV18型感染者的CIN2+发病风险(13.3%)显著高于其他高危HPV型别(4.2%-10.8%)。
(四)治疗后复发情况
HIV感染女性CIN治疗后复发风险显著高于普通人群:1年随访复发率为11%-27%,3年为3%-64%,10年高达57%。不同治疗方式的复发风险存在差异,但整体而言,HIV感染女性的复发风险是普通女性的2倍以上。例如,一项针对10 445名女性的汇总分析显示,接受环形电切术(LLETZ)、冷冻治疗或冷刀锥切术的HIV感染女性,其CIN2+复发率均显著高于HIV阴性女性,且随访时间越长,复发风险差异越明显。
(五)ART状态的影响
调整ART状态后,各年龄组HIV感染女性的CIN2+预测概率均有所降低:15-19岁组为7.0%(0.3-59.0), 年长组维持在20%-29%。这表明ART可能通过免疫重建降低HPV相关病变的进展风险,但由于研究中“全民治疗”策略实施前的数据较多,且ART长期效应的样本量有限,暂无法基于ART状态制定差异化筛查建议。
小结
本研究数据表明,HIV感染女性中CIN2和CIN3的发病风险呈明确的年龄相关性升高,45-49岁年龄组风险最高。研究结果为WHO相关建议提供了循证依据,即HIV感染女性应从25岁开始启动宫颈癌筛查,并每3-5年进行一次常规筛查。扩大筛查和治疗覆盖面对于降低宫颈癌发病率、推动宫颈癌消除进程至关重要。
▌参考文献:
Dalal S, Sundström K, Silva R, et al. Age-specific distribution of cervical precancer and cancer among women living with HIV across seven countries: a systematic review and an individual patient data meta-analysis. Lancet HIV. Published online November 27, 2025. doi:10.1016/S2352-3018(25)00198-5
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
