- 首页 > 正文
乔庐东教授丨解读IDSA复杂性尿路感染:头孢德罗、酶抑制剂复方制剂等新型抗生素的合理应用
感染医线 发表时间:2026/1/22 23:32:21
尿路感染(urinary tract infection,UTI),包括非复杂尿路感染(uncomplicated UTI,uUTI)和复杂性尿路感染(complicated UTI,cUTI),是较为常见的医院或社区获得性感染,以革兰阴性菌感染为主。2022年报道的研究显示,2019年全球有4.0461亿UTI病例,有23.679万因UTI死亡的病例;2018年美国NIS数据则显示有近四分之一的UTI病例为cUTI[2-3]。在人口老龄化背景下,UTI导致的疾病负担日趋严重,且细菌耐药率增高趋势明显,已超过既往指南的经验性抗感染治疗阈值[4-5]。此外,近年来有多项新型抗菌药物治疗尿路感染的临床研究发表。因此需要重新评估UTI的抗菌药物治疗策略。
简化cUTI定义:主要根据感染是否局限膀胱
新版指南对UTI分类的重点在于判断感染范围:若仅局限于膀胱,则定义为uUTI;若出现全身性疾病体征(如发热或菌血症)以及导尿管相关感染、肾盂肾炎的临床体征,均提示感染已超出膀胱范围,则定义为cUTI。
与既往定义有所不同的是,对于存在潜在泌尿系统异常、糖尿病或免疫功能低下的患者,不再自动归类为cUTI患者。总之,新版指南对cUTI的定义更加简化,主要侧重感染的解剖部位,即我们传统理解的上尿路和下尿路。男性前列腺炎也归为cUTI,但由于前列腺组织的特殊性对抗菌药物的药代/药效学特点有特殊的要求,所以本指南并不适用于前列腺炎。
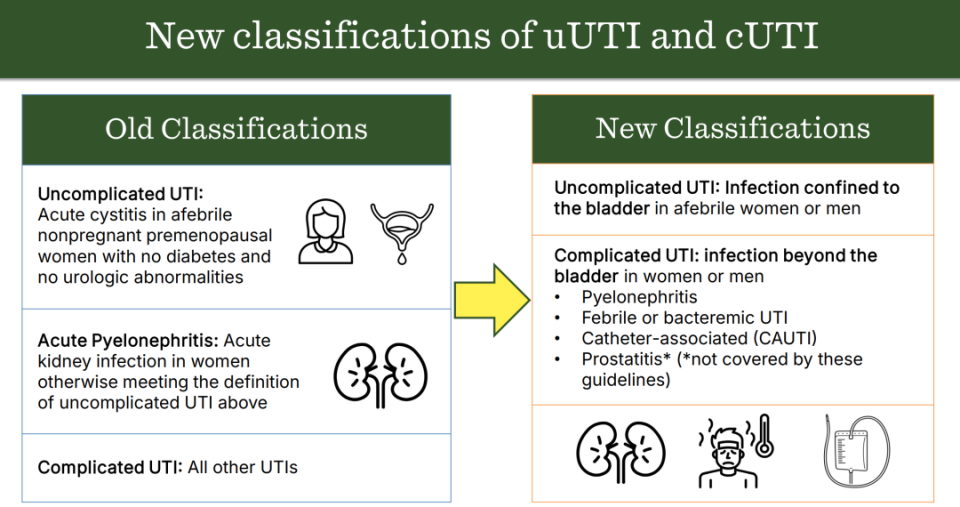
△新旧版uUTI和cUTI定义的区别
经验性治疗:“四步流程”的个体化决策
从美国各地门急诊收集到的尿路感染病原体显示,其抗菌药物耐药率已超过2010年IDSA-UTI指南经验性治疗所推荐的阈值[4-5]。例如,2010版指南建议,若当地尿路病原体对甲氧苄啶-磺胺甲噁唑的耐药率超过20%,应避免将其作为急性膀胱炎的经验性治疗用药;若社区尿路病原体对氟喹诺酮类药物的耐药率超过10%,应避免单独将其用于肾盂肾炎的经验性治疗。而相关数据显示,2018-2020年美国门诊成人尿路分离病原菌对甲氧苄啶-磺胺甲噁唑、氟喹诺酮类的耐药率已达22.4%和21.6%[7]。在UTI耐药菌威胁日趋严峻的情况下,近年来一些新型抗菌药物用于治疗UTI的随机对照试验相继报道或被批准用于临床实践。面对不断攀升的细菌耐药率以及新增的抗感染治疗药物,新版指南重新评估了指导cUTI经验性治疗选择的证据。
鉴于不同医院及不同患者间的耐药情况存在极大差异,专家组认为并不存在一种适用于所有cUTI患者经验性治疗的最佳药物。因此,新版指南并未推荐某个特定药物作为cUTI经验性治疗的首选药物,而是提出了一个“四步流程”用以对患者进行个体化决策。
1)评估病情严重程度(以初步确定经验性抗菌药物治疗的优先顺序);
2)考虑患者特有的耐药尿路病原体风险因素(以优化抗菌覆盖范围);
3)评估患者其他特定合并因素(以降低不良事件风险);
4)对于脓毒症患者,若可获取,应参考当地相关抗菌谱(以进一步提高脓毒症患者接受恰当经验性治疗的概率)。
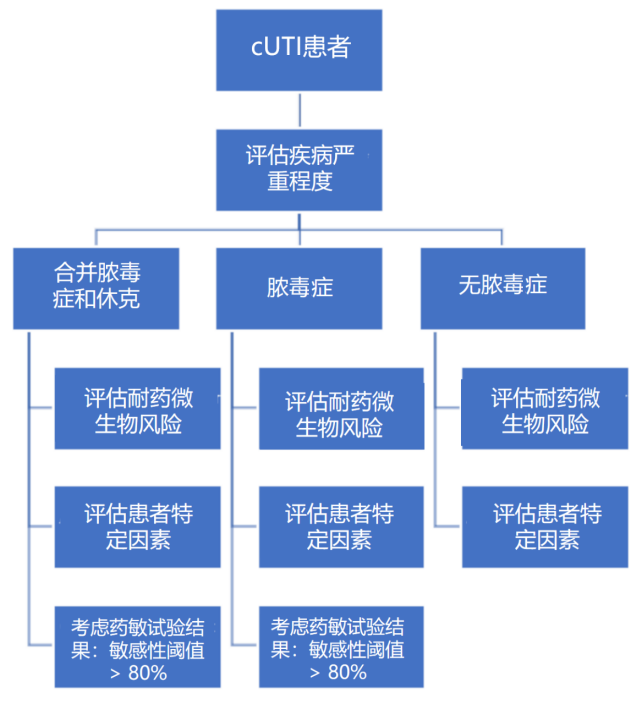
△cUTI经验性抗菌药物治疗的四步流程
新型抗菌药物:助力破解耐药菌治疗困境
在四步评估前,新版指南总结了潜在的cUTI经验性治疗的抗菌药物,包括有或无脓毒症的静脉和口服抗菌药物。值得注意的是,有一些新型抗菌药物,如新型β-内酰胺抗菌药物/β-内酰胺酶抑制剂复方制剂(BL/BLI)、新型铁载体头孢菌素头孢德罗(Cefiderocol)以及新型氨基糖苷类抗菌药物普拉佐米星(Plazomicin)。这些新型药物为个体化的cUTI经验性治疗提供了新的选择。
▽在采用四步评估前的cUTI经验性治疗的潜在抗菌药物
患者情况
|
患者情况 |
首选方案 |
替代方案 |
|
脓毒症(有或无休克) |
第三代或第四代头孢菌素、碳青霉烯类、哌拉西林-他唑巴坦、氟喹诺酮类 |
新型BL/BLI、头孢德罗(cefiderocol)、普拉佐米星(plazomicin)或较老的氨基糖苷类 |
|
无脓毒症(静脉给药) |
第三代或第四代头孢菌素、哌拉西林-他唑巴坦或氟喹诺酮类 |
碳青霉烯类、新型药物(新型BL/BLI、头孢德罗、普拉佐米星)或较老的氨基糖苷类 |
|
无脓毒症(口服给药) |
氟喹诺酮类或甲氧苄啶-磺胺甲噁唑 |
阿莫西林-克拉维酸或口服头孢菌素 |
从指南推荐的经验性治疗四步评估来看,一方面强调了cUTI合并脓毒症这类重症感染患者尽早启动经验性治疗的重要性,另一方面突出了对细菌耐药性的考量,应个体化评估患者感染耐药菌株的风险以及尽可能根据当地的抗菌谱来选择抗菌药物。尽管指南新增了新型BL/BLI、头孢德罗等新型药物的经验性治疗推荐,但在临床实践中也应基于抗菌药物的抗菌谱和细菌的耐药性等进行合理的个体化用药方案。
在已报道的多中心APEKS-cUTI研究[12]中,头孢德罗治疗cUTI显示了不劣于亚胺培南-西司他丁的疗效(主要疗效终点是抗菌药物治疗结束后7±2天的临床和微生物应答的复合终点),达到疗效终点的患者比例分别为73%和55%(调整后的差异:18.58%,95%CI:8.23%~28.92%)。近年来报道的PROVE研究,进一步在真实世界中验证了头孢德罗的疗效和安全性。2025年IDWeek大会报道该研究的多个亚组分析[13-15]则显示,相较于感染患者的挽救性治疗,尽早启动头孢德罗经验性治疗的患者临床治愈率更高,预后更好:在亚组患者中,头孢德罗经验性治疗和挽救治疗的临床治愈率分别为73.7%和54.3%,30天全因死亡率分别为14.0%和30.0%[14]。
降阶梯治疗和缩短抗菌药物治疗疗程策略的探讨
已有临床研究显示,早期由静脉转换为口服抗菌药物,以及缩短抗菌药物疗程在部分患者中具有可行性[16-17]。这种降级治疗策略成为临床合理用药、缓解耐药性发展的热点。新版指南总体上建议有或无菌血症的cUTI(包括急性肾盂肾炎)患者,若初始静脉治疗后临床改善且存在有效口服方案,则可转换为口服抗菌药物完成剩余疗程。在疗程方面,对于治疗有效的有或无菌血症的cUTI(包括急性肾盂肾炎)患者,建议氟喹诺酮的疗程不超过7天。
鉴于循证医学证据尚不充分,上述建议均为证据质量较低的条件性推荐,指南在备注中也强调,当前的临床研究证据主要是在氟喹诺酮类耐药性尚不普遍的时期对氟喹诺酮类药物进行研究所得出的。而关于cUTI缩短疗程或者口服β-内酰胺类抗菌药物治疗的证据较为有限。因此,在临床实践中有关转换口服和缩短抗菌药物疗程的问题,仍需对患者进行个体化决策,也期待未来有更多的临床研究报道,尤其是在新型BL/BLI、头孢德罗等新型药物进入临床实践后,如何把握其降阶梯转口服治疗的时机以及最佳疗程,是值得进一步探讨的问题。
参考文献
[1]Trautner, B.W. et al. Complicated Urinary Tract Infections (cUTI): Clinical Guidelines for Treatment and Management. Available from: https://www.idsociety.org/practice-guideline/complicated-urinary-tract-infections/#:~:text=Figure%201.0%3A%20Comparing%20prior%20and%20updated%20classifications%20of%20uncomplicated%20and%20complicated%20UTI
[2]Yang X, Chen H, Zheng Y, Qu S, Wang H, Yi F. Disease burden and long-term trends of urinary tract infections: A worldwide report. Front Public Health. 2022;10:888205. doi:10.3389/fpubh.2022.888205
[3]Zilberberg MD, Nathanson BH, Sulham K, Shorr AF. Descriptive Epidemiology and
Outcomes of Hospitalizations With Complicated Urinary Tract Infections in the United States,
2018. Open Forum Infect Dis. Jan 2022;9(1):ofab591. doi:10.1093/ofid/ofab591
[4]FDA Package insert for FORTAZ (ceftazidime for injection) 2007.https://www.accessdata.fda.gov/drugsatfda_docs/label/2007/050578s053,050634s020lbl.pdf
[5]Gupta K, Hooton TM, Naber KG, et al. International clinical practice guidelines for the treatment of acute uncomplicated cystitis and pyelonephritis in women: A 2010 update by the Infectious Diseases Society of America and the European Society for Microbiology and Infectious Diseases. Clin Infect Dis. 2011;52(5):e103-e120. doi:10.1093/cid/ciq257
[6]Robert H. Rubin, Eugene D. Shapiro,Vincent T. Andriole, Robert J. Davis, and Walter E. Stamm. Evaluation of New Anti-Infective Drugs for the Treatment of Urinary Tract Infection. Clinical Infectious Diseases 1992;15(Suppll):S216-27
[7]Aronin SI, Gupta V, Dunne MW, Watts JA, Yu KC. Regional Differences in Antibioticresistant Enterobacterales Urine Isolates in the United States: 2018-2020. Int J Infect Dis. Jun 2022;119:142-145. doi:10.1016/j.ijid.2022.03.052
[8]Kammineni C, Vamsi S, Basireddy SR. Surveillance of In Vitro Activity of Cefiderocol Against Carbapenem-Resistant Gram-Negative Clinical Isolates in a Tertiary Care Hospital. Cureus. 2024;16(8):e67164. Published 2024 Aug 19. doi:10.7759/cureus.67164
[9]Gill CM, Santini D, Nicolau DP; ERACE-PA Global Study Group. In vitro activity of cefiderocol against a global collection of carbapenem-resistant Pseudomonas aeruginosa with a high level of carbapenemase diversity. J Antimicrob Chemother. 2024;79(2):412-416. doi:10.1093/jac/dkad396
[10]Santerre Henriksen A, Jeannot K, Oliver A, et al. In vitro activity of cefiderocol against European Pseudomonas aeruginosa and Acinetobacter spp., including isolates resistant to meropenem and recent β-lactam/β-lactamase inhibitor combinations. Microbiol Spectr. 2024;12(4):e0383623. doi:10.1128/spectrum.03836-23
[11]Shortridge D, Streit JM, Mendes R, Castanheira M. In Vitro Activity of Cefiderocol against U.S. and European Gram-Negative Clinical Isolates Collected in 2020 as Part of the SENTRY Antimicrobial Surveillance Program. Microbiol Spectr. 2022;10(2):e0271221. doi:10.1128/spectrum.02712-21
[12]Portsmouth S , van Veenhuyzen D, Echols R, et al. Cefiderocol versus imipenem-cilastatin for the treatment of complicated urinary tract infections caused by gram-negative uropathogens: a phase 2, randomised, double-blind, non-inferiority trial. Lancet Infect Dis2018; 18:1319–28.
[13]Shields R K, et al. Outcomes of Patients Treated With Cefiderocol For Infections Caused by β-Lactam–β-Lactamase Inhibitor Non-Susceptible Bacteria: Subgroup Analysis of the PROVE Study. IDWeek 2025; Abstract 1354.
[14]Clancy C J, et al. Earlier Cefiderocol Use Was Associated with Better Outcomes for Challenging Gram-Negative Bacterial Infections: US Results From the Global Observational PROVE Study. IDWeek 2025; Abstract 1353.
[15]Drwiega E, et al. Clinical Outcomes of Cefiderocol for Treatment of Bloodstream Infections Caused by Gram-Negative Bacteria: Subgroup Analysis of the PROVE Study. IDWeek 2025; Abstract 1352.
[16]Harvey EJ, Hand K, Weston D, Ashiru-Oredope D. Development of National Antimicrobial Intravenous-to-Oral Switch Criteria and Decision Aid. J Clin Med. 2023 Mar 7;12(6):2086.
[17]McAteer J, Lee JH, Cosgrove SE, et al. Defining the Optimal Duration of Therapy for Hospitalized Patients With Complicated Urinary Tract Infections and Associated Bacteremia. Clin Infect Dis. 2023;76(9):1604-1612. doi:10.1093/cid/ciad009

乔庐东 教授
首都医科大学附属北京同仁医院
泌尿外科、主任医师、博士
国家卫健委抗菌药物专委会感染工作组委员
中华医学会泌尿外科学分会感染与炎症学组副组长
北京医学会泌尿外科学分会第12届委员
北京医学会泌尿外科学分会感染学组副组长
华北结石病防治基地委员
参编国内多篇尿路感染相关指南和共识
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
