- 首页 > 正文
全外显子组测序解锁重症细菌感染遗传真相,精准诊断新路径来了
感染医线 发表时间:2026/1/8 20:20:36
编者按:严重细菌感染(SBI)是全球公共卫生的重要挑战,其发病率和死亡率居高不下。近年来,遗传因素在SBI易感性和严重性中的作用日益受到关注。传统研究多采用候选基因策略,而新一代测序技术(NGS)尤其是全外显子组测序(WES)的应用,为无偏倚地探索遗传因素提供了新途径。一项发表于The Journal of Infectious Diseases的系统综述梳理了12项采用WES技术研究既往健康SBI患者遗传因素的研究,分析了WES的诊断效能、遗传关联发现及方法学特征,探讨了该技术在SBI遗传机制研究中的应用价值与未来方向,为临床诊断和治疗提供参考。

严重细菌感染的公共卫生负担
SBI涵盖败血症、化脓性脑膜炎、重症肺炎等多种致命性疾病,是全球范围内导致死亡的主要原因之一。据统计,2017年全球败血症病例达3300万例,死亡人数超600万,其中5岁以下儿童死亡约290万例。即使在医疗资源充足的地区,SBI仍面临诊断延迟、治疗反应不佳等问题,其高死亡率和后遗症风险对公共卫生体系构成持续挑战。深入探究SBI的发病机制,尤其是遗传层面的易感因素,对于优化预防策略、开发新型治疗靶点、改善患者预后至关重要。
SBI的遗传易感性研究现状
个体对细菌感染的反应存在显著差异,除解剖结构异常、获得性免疫缺陷(如HIV感染、免疫抑制剂使用)等已知因素外,先天性免疫缺陷(IEI)及其他遗传变异被证实是SBI的重要易感因素。免疫系统中信号传导、病原体识别、补体激活等通路的基因缺陷,可能导致机体对细菌侵袭的防御能力下降,进而引发严重感染。
以往的SBI遗传研究多采用候选基因法,即针对已知与免疫功能相关的少数基因进行分析。该方法虽在已知基因的变异发现中成效显著,但无法识别未被报道的新致病基因,极大限制了对SBI遗传机制的全面理解。随着NGS技术的发展,WES作为无靶向方法,可全面捕获基因组编码区的遗传变异,为发现SBI相关新基因和通路提供了强大工具。
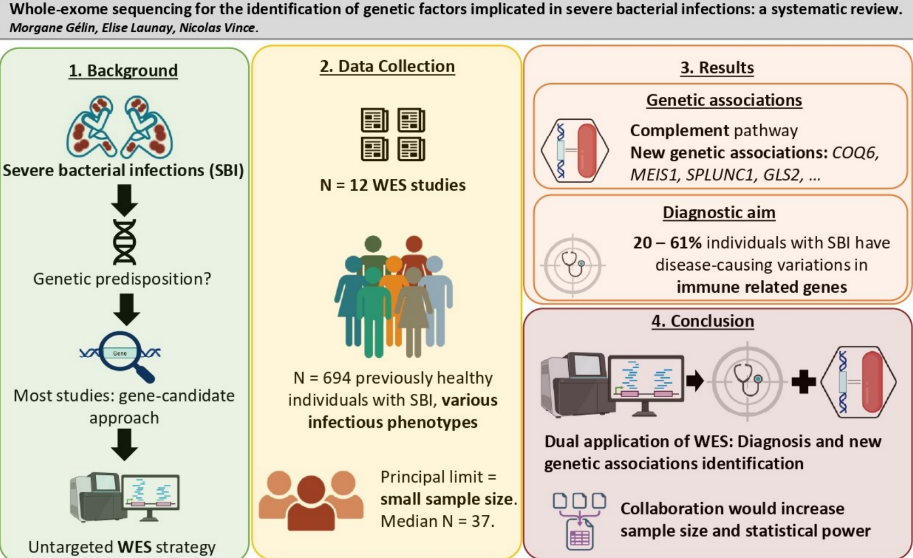
(文章图形摘要)
研究方法
本研究纳入采用WES技术分析既往健康SBI患者的相关研究,排除非细菌感染研究及包含已知遗传疾病或免疫功能异常患者的研究。研究团队评估了证据体的确定性并检测了偏倚风险,同时根据患者的感染表型对纳入研究进行分组,以呈现其主要共同特征并比较研究结果。
研究结果
纳入研究的基本特征
纳入研究的患者涵盖儿童和成人,其中8项研究聚焦儿童SBI,4项针对成人患者。感染表型具有多样性,包括多细菌所致脓毒症(4项研究)、铜绿假单胞菌感染(2项研究)、肺炎链球菌感染(2项研究),以及金黄色葡萄球菌菌血症、暴发性紫癜、复发性伤寒等特定感染类型(各1项研究)。样本量差异较大,排除验证队列后,病例数范围为2-401例(中位数37例),WES检测病例数中位数为27例。
6项研究采用前瞻性设计,1项为回顾性研究,2项采用混合设计,3项为病例报告。9项研究设置了对照人群,包括轻度感染患者、院内外显子数据库人群或公共数据库人群(如1000基因组计划),对照人群规模为32-140000余人(中位数472人)。4项研究进行了家族分析,基于遗传模式(常染色体显性/隐性)筛选变异位点。
WES检测会产生大量遗传变异数据,纳入研究采用了多样化的变异筛选策略,包括基于次要等位基因频率(MAF)的过滤(如MAF<1%或0.5%)、功能预测工具(SIFT、PolyPhen-2、CADD等)、通路富集分析(GSEA)、负担测试等。质量控制方面,所有研究均报告了目标区域测序覆盖度验证,仅1项研究未描述基因分型质量控制方法;6项研究存在批次效应风险,仅1项通过统计分析进行校正。
WES的诊断效能
在聚焦先天性免疫缺陷(IEI)相关基因分析的7项研究中,42%(156/372)的既往健康SBI患者携带IEI基因的潜在致病变异。其中两项专门评估WES诊断效能的研究显示,分别有20%和61%的SBI患者存在IEI基因变异,差异可能源于基因panel选择(240个细菌感染相关PID基因 vs. 430个IEI基因)和变异致病性注释标准的不同。3例病例报告均通过WES成功识别了与患者临床表型相符的IEI基因变异,证实了WES在罕见病例诊断中的价值。
遗传关联发现
补体系统是与SBI关联最密切的生物学通路,3项研究(涉及378例患者)均证实补体通路基因变异与SBI易感性相关,包括C9、CR3/CR4复合物相关基因等。IRAK4基因变异在2例病例报告中被发现,分别与铜绿假单胞菌脓毒症和复发性严重感染相关,该基因是先天性免疫信号传导的关键分子。
研究识别了多个未被既往SBI研究报道的新基因,包括COQ6(与肺炎链球菌急性下呼吸道感染相关)、GLS2(与复杂性金黄色葡萄球菌菌血症相关)、SPLUNC1(与侵袭性脑膜炎球菌病相关)等。这些基因涉及辅酶合成、代谢调控、细菌黏附抑制等功能,为揭示SBI的新型病理机制提供了线索。
结果验证与偏倚风险
4项研究通过独立队列进行了结果验证,1项采用不同对照人群进行伪验证,7项研究开展了功能实验(如蛋白表达分析、补体活性检测、细胞侵袭实验)验证变异的致病性。偏倚风险方面,6项研究存在潜在报告偏倚(未完整报道正负结果),4项存在选择偏倚(患者入选标准严格),仅4/9项采用非亲属对照的研究进行了遗传背景匹配,其余存在人群分层偏倚风险。所有研究均假设变异完全外显,可能高估了遗传因素的致病作用。
结论
本系统综述通过对12项采用WES技术的研究进行分析,证实了WES在既往健康SBI患者遗传因素识别中的重要价值:不仅能为42%的患者提供潜在的IEI基因诊断,还发现了多个新的SBI易感基因和补体通路这一核心关联通路,突破了传统候选基因法的局限性。尽管现有研究存在样本量小、方法学异质性高、验证不足等问题,但仍为SBI的遗传机制研究提供了关键线索。
随着测序技术的普及和多中心合作的推进,WES有望成为SBI,尤其是严重或复发性SBI患者的常规遗传检测工具,为精准诊断、个体化治疗和遗传咨询提供支撑。未来需通过标准化流程、大规模队列和深入的功能验证,进一步揭示SBI的遗传基础,为降低疾病负担提供新的科学依据。
▌参考文献:
Gélin M, Launay É, Vince N. Whole-exome sequencing for the identification of genetic factors implicated in severe bacterial infections: a systematic review. J Infect Dis. Published online January 7, 2026. doi:10.1093/infdis/jiag006
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
