- 首页 > 正文
2026 CRPA指南发布丨周华教授:聚焦精准抗感染,规范化头孢德罗等新型抗菌药物临床应用
感染医线 发表时间:2026/3/31 17:17:42
在医院获得性感染中,铜绿假单胞菌(PA)始终是棘手的对手。当其披上“碳青霉烯耐药”(CRPA)的铠甲,临床常陷入“无药可用”的困境。
2026年2月,《碳青霉烯耐药铜绿假单胞菌感染诊治指南(2026版)》正式发布。该指南基于循证医学证据,系统阐述了CRPA的流行病学特征、快速诊断技术、耐药机制检测以及个体化治疗策略等关键问题,并为新型抗菌药物的临床应用提供了规范指导。
指南领航:CRPA诊疗新纪元与治疗困局
01.
明确耐药定义,直面治疗困境[1]
2026版指南在既往共识基础上,明确并重申了关键耐药菌的定义,为临床精准识别高危患者提供了标准:
- 碳青霉烯耐药铜绿假单胞菌(CRPA):指对碳青霉烯类抗生素耐药的铜绿假单胞菌;
- 难治性耐药铜绿假单胞菌(DTR-PA):指对哌拉西林‑他唑巴坦、头孢他啶、头孢吡肟、氨曲南、亚胺培南、美罗培南、左氧氟沙星和环丙沙星均耐药的铜绿假单胞菌,CRPA包含DTR-PA。
02.
关键诊疗推荐意见:
基于现有证据,指南针对诊断优化与治疗策略提出了以下具体推荐:
- 碳青霉烯酶检测:建议实施碳青霉烯酶表型或基因型检测,以早期指导用药,特别是对于重症患者。(低把握度证据,弱推荐)
- 联合药敏试验:建议对CRPA进行联合药敏试验(首选棋盘法),以确保治疗方案的最佳效果。(低把握度证据,弱推荐)
- 治疗药物监测(TDM):建议在使用多种抗菌药物(包括新型药物)治疗CRPA感染时,尤其是重症或需要长疗程治疗的患者,应尽可能进行抗菌药物TDM。(低把握度证据,弱推荐)
- 联合治疗策略:建议CRPA感染的重症患者采用敏感抗菌药物联合治疗。对于CRPA、DTRPA引起的医院获得性肺炎、呼吸机相关肺炎和血流感染即使单药敏感也应实施联合治疗方案。(低把握度证据,条件性推荐)
03.
CRPA治疗的现实困境
当前,CRPA感染正面临耐药机制复杂化与检出率攀升的双重挑战。CRPA耐药机制复杂多样,包括产碳青霉烯酶(如VIM、IMP、NDM等金属酶及KPC等丝氨酸酶)、外膜孔蛋白缺失以及主动外排泵过表达等[2]。与此同时,国内监测数据显示难治性菌株增长迅猛:一项涵盖7480例铜绿假单胞菌血流感染的7年回顾性研究显示,DTR-PA检出率从5%升至15%,CRPA更是从26%激增至47%[3]。
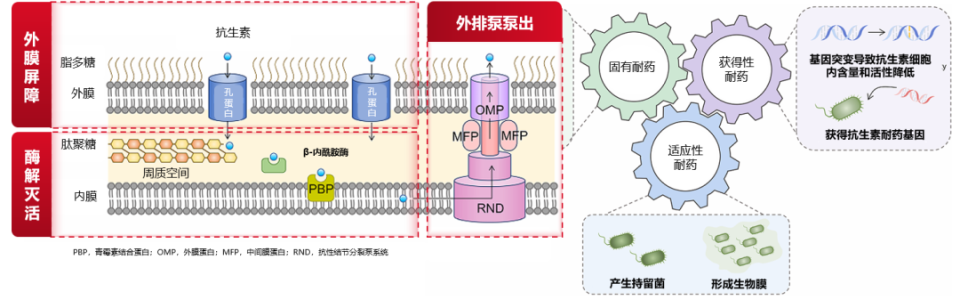
铜绿假单胞菌的耐药机制示意图[2]
伴随着耐药菌株检出率的显著上升,临床也面临着极高的死亡风险与治疗难度。一项基于血液科患者10年回顾性队列研究数据显示[4],CRPA血流感染患者的28天死亡率高达38.2%,显著高于敏感菌株(12.2%,P<0.001),死亡风险增加3倍以上,且初始不恰当治疗超56%。高致死率与高治疗失败率的现状,提示现有治疗手段在应对复杂耐药菌时的局限性。
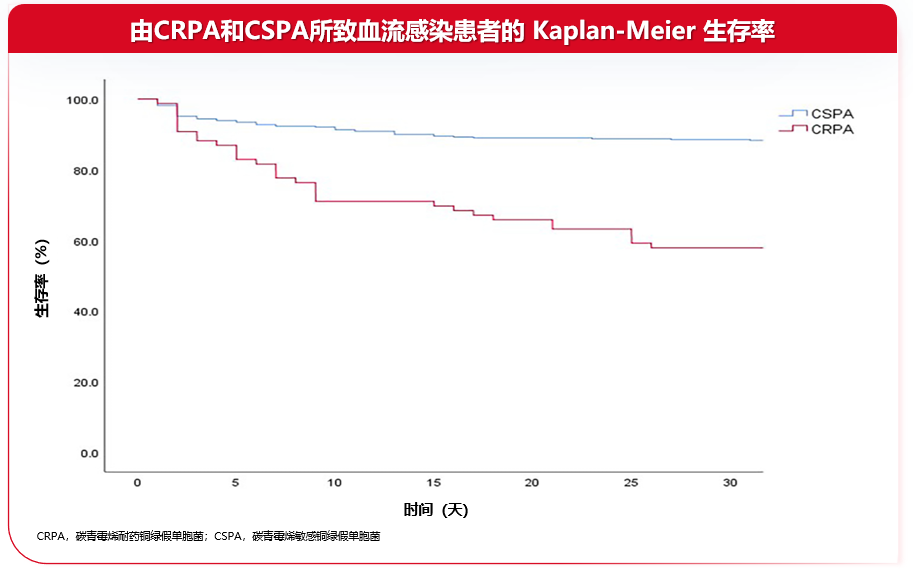
面对如此复杂的耐药形势与紧迫的治疗需求,具有独特“铁载体”转运机制的头孢德罗,凭借其能绕过多种耐药屏障的特性,为完善抗CRPA治疗武器库、解决复杂临床难题提供了新的选择。
头孢德罗的独特“特洛伊木马
01.
头孢德罗的作用机制
头孢德罗(Cefiderocol)是一种具有独特“铁载体”结构的新型头孢菌素,其药理特性主要源于以下两个关键机制[5-7]:
- 铁载体介导的主动转运:头孢德罗作为一种新型铁载体头孢菌素,在C-3侧链上连接了一个儿茶酚基团,这一结构使其能够与铁离子形成螯合物,并通过细菌的铁转运系统被主动运输进入细菌细胞 。
- 对多种β-内酰胺酶高度稳定:进入菌体后,头孢德罗对A类(KPC)、B类(金属酶,如VIM/IMP/NDM)、C类(AmpC)及D类(OXA)酶均保持稳定。
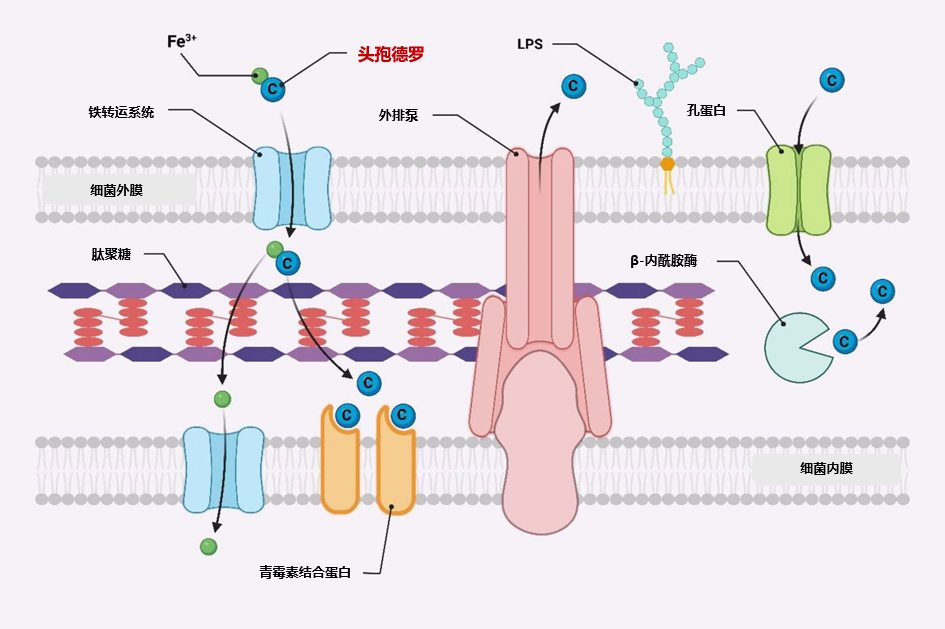
头孢德罗作用机制示意图[8]
02.
头孢德罗的PK/PD特征及组织分布
头孢德罗的几何平均分布容积(±SD)为18.0(±3.36)L。血浆蛋白结合率为40%至60%,主要与白蛋白结合。需机械通气的肺炎患者在稳态下接受头孢德罗2 g(或根据肾功能调整的等效剂量)3小时输注后,在输注结束时,头孢德罗在上皮细胞衬液中的浓度为3.1至20.7 mg/L,输注结束后2小时为7.2至15.9 mg/L[9]。
头孢德罗的终末消除半衰期为2至3小时。其代谢程度极低,单次1小时输注1g(批准推荐剂量的0.5倍)放射性标记头孢德罗后,代谢产物占比不足10%,90.6%以原形经尿液排泄[9]。
头孢德罗的杀菌效应主要取决于游离药物浓度高于最低抑菌浓度的时间(%fT>MIC)。一项纳入516名受试者(包括健康受试者及肺炎、菌血症/败血症、复杂性尿路感染患者)的PK/PD分析显示[10],头孢德罗的%fT > MIC在大多数患者中达到100%。蒙特卡洛模拟进一步证实,标准剂量方案(2 g q8h,3小时输注)对MIC≤4 μg/mL的革兰阴性菌,在所有感染部位和肾功能分组中均实现超过90%的目标达成概率。
体外抗菌活性:全球监测与中国数据
理论上的机制优势,是否转化为实际的抗菌活性?多项大规模体外监测研究给出了肯定的答案。
01.
全球监测数据
ERACE-PA研究[11]:该研究有报道头孢德罗对来自全球12个中心的806株CRPA菌株(含200余株产碳青霉烯酶菌株)的体外敏感性。结果显示,依据CLSI和EUCAST标准,头孢德罗的整体敏感率分别高达98%和95%。无论菌株是否产酶或产何种类型酶(如VIM、IMP、NDM、 KPC等),头孢德罗均保持了较高的敏感性。
按头孢德罗最低抑菌浓度(MIC)分布的菌株比例
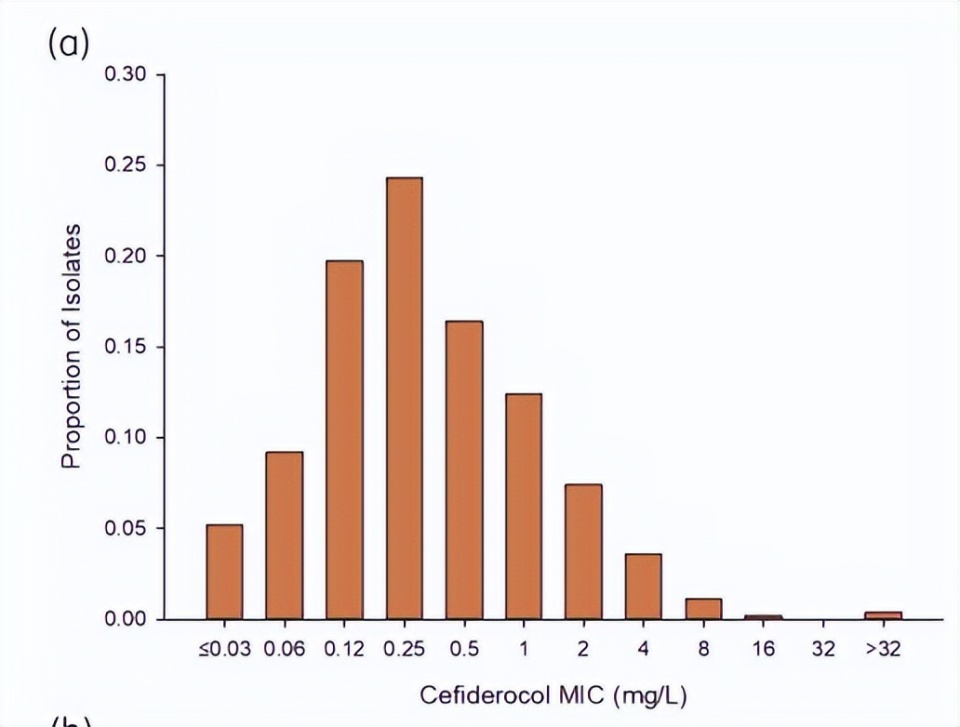
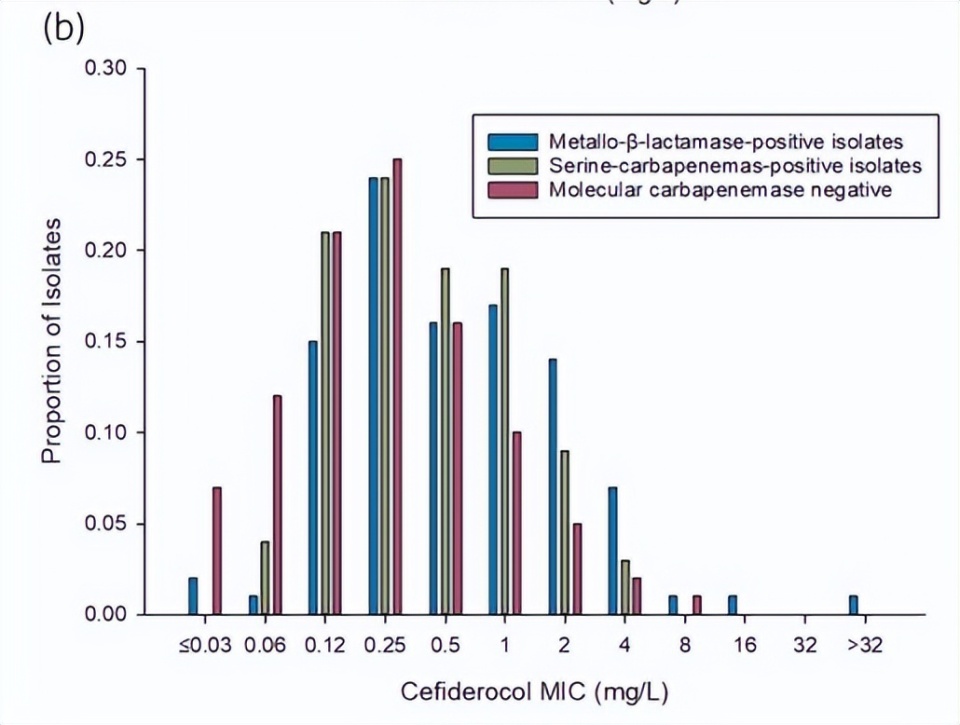
(a) 所有纳入菌株按头孢德罗 MIC 的分布比例(MIC₅₀:0.25 mg/L;MIC₉₀:2 mg/L;依据 CLSI 标准,敏感率为 98%;依据 EUCAST 标准,敏感率为 95%)。
(b) 按分子碳青霉烯酶检测结果分组的菌株,头孢德罗 MIC 分布比例:①产金属 β- 内酰胺酶(MBL)阳性菌株:MIC₅₀:0.5 mg/L;MIC₉₀:4 mg/L;依据 CLSI 标准,敏感率为 97%;依据 EUCAST 标准,敏感率为 89%;②产丝氨酸碳青霉烯酶阳性菌株:MIC₅₀:0.5 mg/L;MIC₉₀:2 mg/L;依据 CLSI 标准,敏感率为 100%;依据 EUCAST 标准,敏感率为 97%;③ 分子检测碳青霉烯酶阴性菌株:MIC₅₀:0.25 mg/L;MIC₉₀:1 mg/L;依据 CLSI 标准,敏感率为 99%;依据 EUCAST 标准,敏感率为 96%。
SIDERO与SENTRY研究[12,13]:SIDERO研究中,头孢德罗对7700株铜绿假单胞菌的敏感率达99.9%(MIC≤4 mg/L),且对美罗培南、头孢他啶/阿维巴坦等药物不敏感的菌株,头孢德罗敏感率仍超过99%。
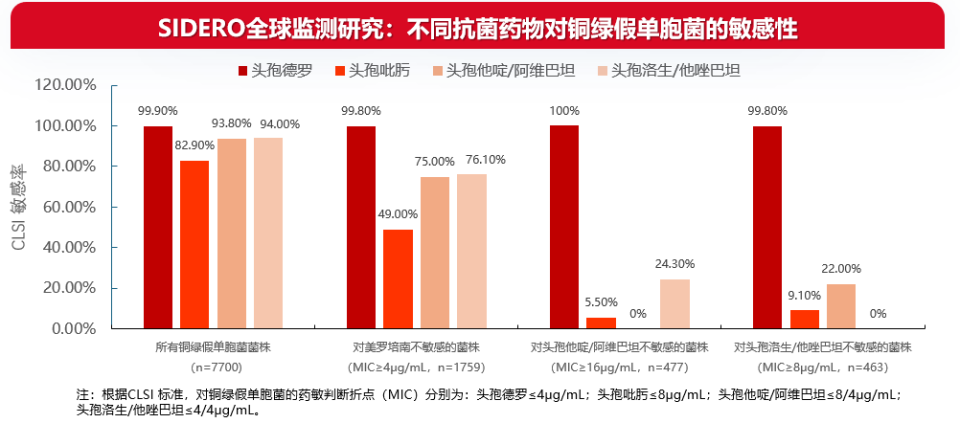
SENTRY项目对2020-2024年美欧地区数据的分析显示,头孢德罗对铜绿假单胞菌的敏感率五年间维持在98.8%-100%;即使在碳青霉烯不敏感亚群中,敏感率也保持在95.3%-100%,显示出良好的稳定性。
02.
中国本土数据
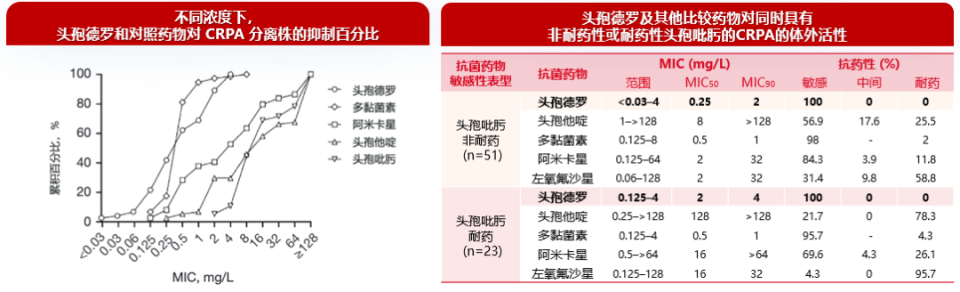
一项涵盖北京四家三甲医院的研究显示[14],头孢德罗对74株CRPA的抑制率达100%(MIC ≤4 mg/L),MIC₅₀和MIC₉₀分别为0.5 mg/L和4 mg/L。
03.
对DTR-PA的体外活性
一项针对难治菌株的研究进一步验证了头孢德罗的抗菌活性[15]。在对88株难治性铜绿假单胞菌(DTR-PA)的检测中,96.6%的菌株对头孢德罗敏感(MIC≤4μg/mL);MIC中位值仅0.5μg/mL。
综合上述全球及本土监测数据,头孢德罗在体外对CRPA及DTR-PA菌株显示出良好的抗菌活性和较高的敏感率,为临床应对复杂耐药菌感染提供了重要的体外药理学依据。
临床疗效:从关键RCT到真实世界研究
体外抗菌活性需通过临床研究进一步验证其治疗效果。多项随机对照试验(RCT)及真实世界研究评估了头孢德罗在治疗碳青霉烯耐药铜绿假单胞菌(CRPA)感染中的疗效与安全性。
01.
CREDIBLE-CR研究[16]
CREDIBLE-CR是一项随机、开放标签、多中心的III期研究,旨在评估头孢德罗对比最佳可用疗法(BAT)治疗碳青霉烯耐药革兰阴性菌感染的疗效。在118例碳青霉烯耐药菌感染患者中,铜绿假单胞菌(PA)是第三常见病原体,占比19%(22/118),分布于各感染部位。按感染部位分析,在包含PA患者的各亚组中,头孢德罗均展现出与最佳可用疗法(BAT)相当的疗效。
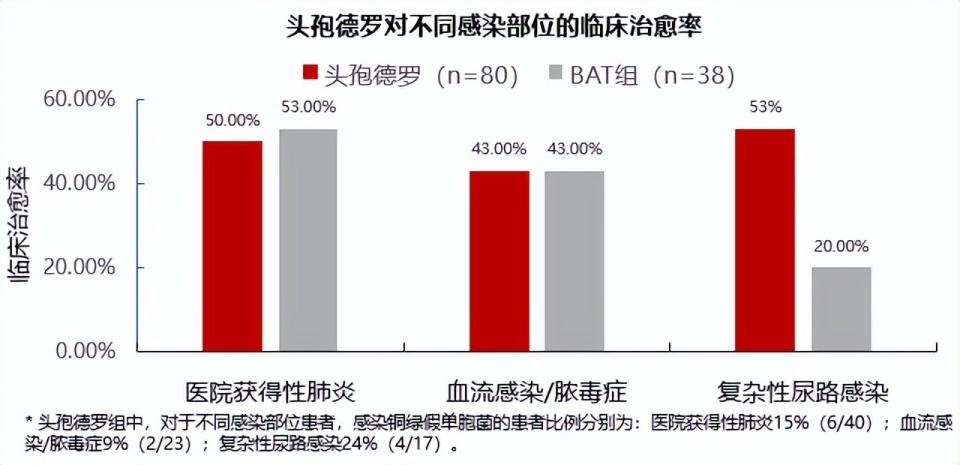
更值得关注的是,在产金属β-内酰胺酶的感染亚组(包含铜绿假单胞菌感染)中,头孢德罗组临床治愈率达75%,高于BAT组的29%,印证了其对金属酶菌株的独特优势。
02.
真实世界研究
除随机对照试验外,多项真实世界研究进一步提供了头孢德罗在常规临床实践中的数据支持。
PERSEUS研究是在西班牙开展的大规模回顾性真实世界研究[17],研究纳入261例革兰阴性菌感染患者,其中174例为CRPA感染,结果显示,使用头孢德罗治疗CRPA感染患者,实现高治愈率和低死亡率。

即使是对头孢洛生/他唑巴坦或头孢他啶/阿维巴坦耐药的患者,头孢德罗依然保持了80%左右的临床治愈率。
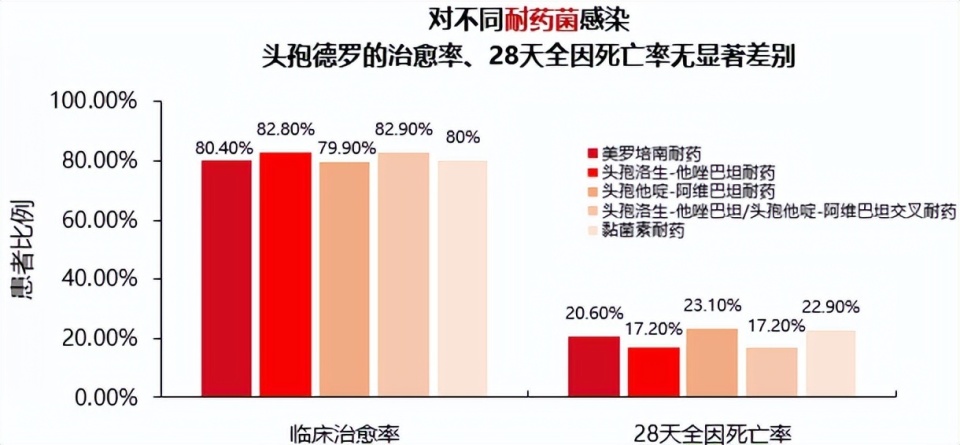
此外,头孢德罗单药治疗的临床治愈率高于联合治疗,且死亡率更低。作为一线治疗使用时,临床治愈率高于非一线使用。
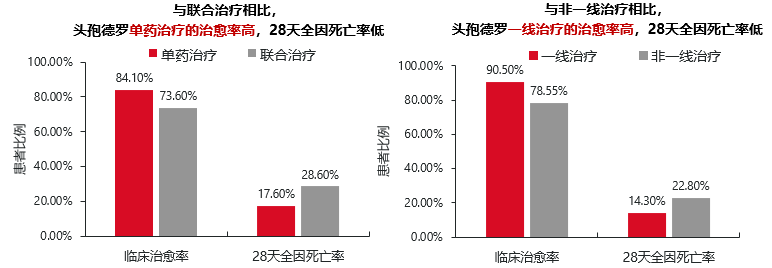
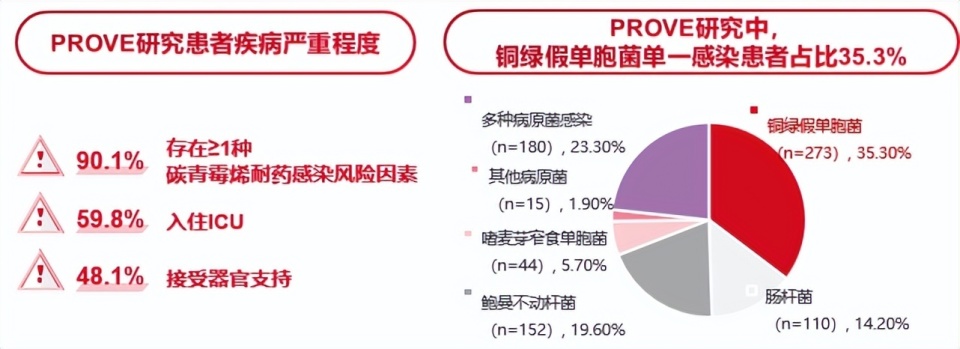
PROVE研究是一项国际多中心回顾性真实世界研究[18],系统评估了头孢德罗在常规临床实践中的有效性与安全性。中期分析纳入774例住院患者, 患者病情危重,感染部位以呼吸道为主。结果显示:
- 整体人群中,头孢德罗临床治愈率64%,30天院内死亡率24.3%。
- 针对铜绿假单胞菌单一感染和包含铜绿假单胞菌的混合感染患者,头孢德罗均实现65%以上的临床治愈率。
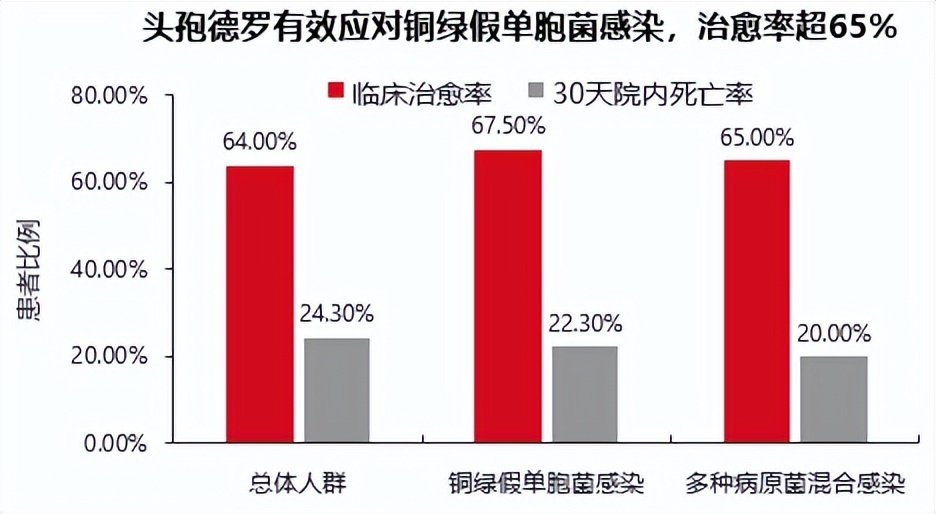
PROVE研究与PERSEUS研究的结果相互印证,为头孢德罗在CRPA治疗中的价值提供了真实世界证据。
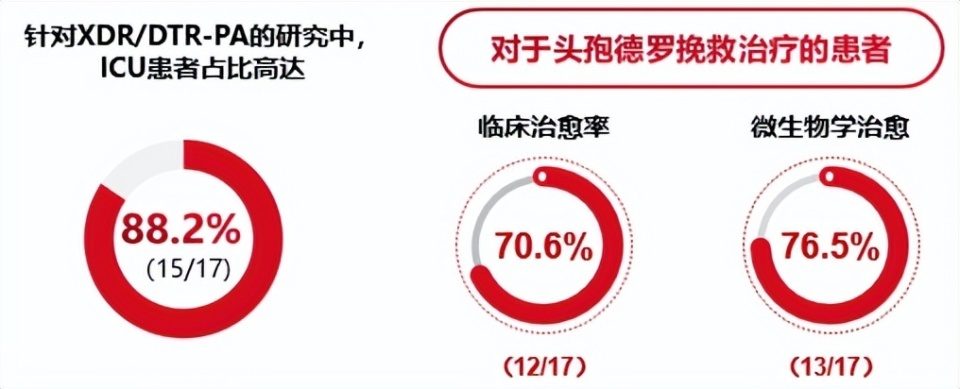
此外,意大利的一项针对XDR/DTR-PA的研究显示[19],在无其他治疗选择的重症患者中,头孢德罗挽救治疗的临床治愈率达70.6%,微生物学治愈率达76.5%。
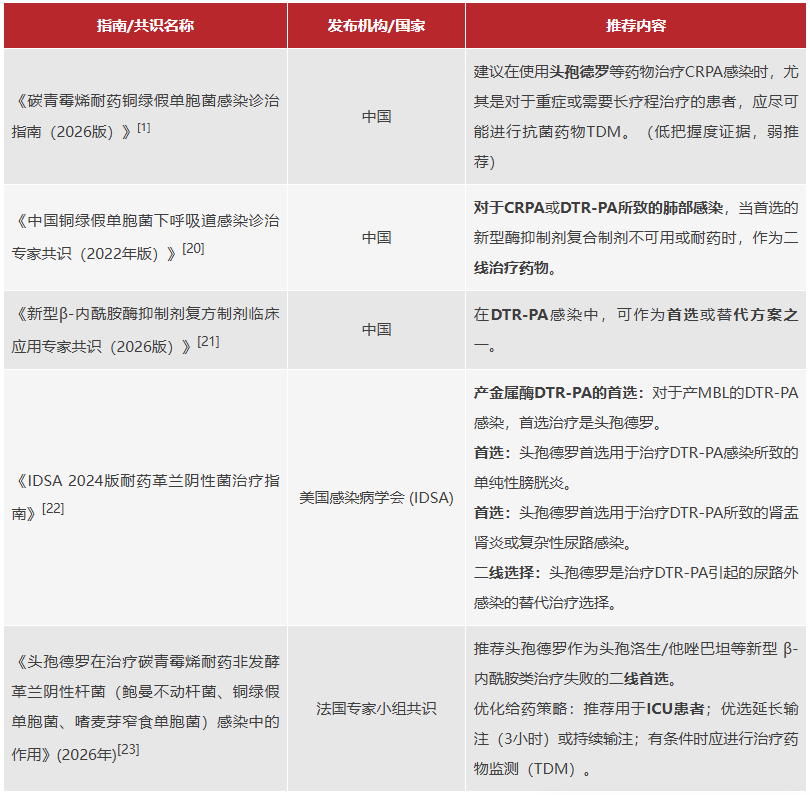
指南推荐:国内外共识的“不约而同”
基于头孢德罗的体外和临床数据,国内外指南也逐步将头孢德罗纳入相应治疗推荐中,为其在 CRPA 治疗中的应用提供了规范依据。
结语
随着《碳青霉烯耐药铜绿假单胞菌感染诊治指南(2026版)》的发布,国内CRPA及DTR-PA诊疗策略进一步规范。面对铜绿假单胞菌多重耐药机制复杂的临床现状,引入新机制抗菌药物成为重要途径。
循证数据显示,头孢德罗对CRPA保持较高体外敏感率,并且在产金属酶菌株及其他新型酶抑制剂耐药菌株感染中均显示出明确的临床疗效。基于上述证据,国内2026版指南及IDSA等国际共识已将其列为CRPA及DTR-PA感染的首选或替代方案,并建议重症患者通过延长输注及治疗药物监测优化给药。
参考文献
[1]. 中华医学会细菌感染与耐药防治分会, 等. 碳青霉烯耐药铜绿假单胞菌感染诊治指南(2026版)[J]. 中华医学杂志,2026,106(07):601-617.
[2]. Yang J, et al. Crit Rev Microbiol. 2025 Sep;51(5):841-859.
[3]. Dong L, et al. Infect Drug Resist. 2025 Feb 18;18-979-991.
[4]. Yuan F, et al. J Glob Antimicrob Resist. 2024 Jun;37:150-156.
[5]. Ito A, et al. Antimicrob Agents Chemother. 2017 Dec 21;62(1):e01454-17.
[6]. Zhanel GG, et al. Drugs. 2019 Feb;79(3):271-289.
[7]. Sato T, Yamawaki K. Clin Infect Dis. 2019 Nov 13;69(Suppl 7):S538-S543.
[8]. Roustaye Gourabi MJ, et al. Curr Microbiol. 2025 Nov 18;83(1):25.
[9]. 注射用硫酸甲苯磺酸头孢德罗说明书,国家药品监督管理局,核准日期:2026年1月5日.
[10]. Kawaguchi N, et al. Antimicrob Agents Chemother. 2021 Feb 17;65(3)e01437-20.
[11]. Gill CM, et al. J Antimicrob Chemother. 2024 Feb 1;79(2)412-416.
[12]. Karlowsky JA, et al. Antimicrob Agents Chemother. 2023 Jun 15;67(6):e0042723.
[13]. Yoshinori Yamano, et al. Open Forum Infectious Diseases, Volume 13, Issue Supplement_1, January 2026, ofaf695.1413.
[14]. Wang Y, et al. Ann Transl Med. 2022 Mar;10(5):261.
[15]. Alexander J, et al. Open Forum Infect Dis. 2023 Nov 27;10(Suppl 2):ofad500.2356.
[16]. Bassetti M, et al. Lancet Infect Dis. 2021;21(2)226-240.
[17]. Torre-Cisneros J, et al. Eur J Clin Microbiol Infect Dis. 2025 Jun;44(6):1375-1390.
[18]. Clancy C, et al. Poster presented at IDWeek 2024.
[19]. Meschiari M, et al. JAC Antimicrob Resist. 2021 Dec 11;3(4):dlab188.
[20]. 中华医学会呼吸病学分会感染学组. 中国铜绿假单胞菌下呼吸道感染诊治专家共识(2022年版)[J]. 中华结核和呼吸杂志,2022,45(08):739-752.
[21]. 国家传染病医学中心,等. 新型β-内酰胺酶抑制剂复方制剂临床应用专家共识[J]. 中华传染病杂志,2026, 网络预发表.
[22]. Tamma PD, et al. Clin Infect Dis. 2024 Aug 7:ciae403.
[23]. Bleibtreu A, et al. Infect Dis Ther. 2026 Jan 31. PMID 41619080.

周华 博士
浙江大学医学院附属第二医院呼吸与危重症医学科
常务副主任、呼吸内镜中心主任
主任医师、教授、博士生导师
首届国家优秀青年医师
国家“四大慢病”科技重大专项首席科学家
中华医学会细菌耐药和感染防控分会委员
中华医学会呼吸病学分会感染学组委员
中华医学会内科学分会青年委员
中国抗癌协会呼吸肿瘤分会常委
中国医药教育协会感染性疾病委员会常委
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
