- 首页 > 正文
徐郑丽教授:亚胺西瑞在危重症碳青霉烯耐药菌感染及高危患者治疗中的应用价值
感染医线 发表时间:2026/4/29 17:16:18
编者按:当前细菌耐药性问题日趋严峻,碳青霉烯耐药菌所致危重症感染成为临床治疗难题,其高死亡率、窄治疗窗的特点对治疗策略和药物选择提出了更高要求。在第九届北京血栓与止血会议暨第七届北京血液肿瘤与免疫高峰论坛上,北京大学人民医院徐郑丽教授在主题报告中,阐述了危重症感染的核心治疗原则,系统介绍了经典药物亚胺培南的临床价值,并深入讲解升级制剂亚胺西瑞在危重症碳青霉烯耐药菌感染及高危患者治疗中的优势,为临床规范化治疗提供重要参考。
01
抗感染治疗核心原则与危重症感染的治疗需求
抗感染治疗的核心是围绕患者病情,结合病原菌特征和抗菌药物特性制定方案,需综合评估患者感染危重程度、部位、既往感染史,以及药物抗菌谱、活性、组织浓度和安全性等因素。
危重症感染患者死亡风险高,治疗窗口唯一,脓毒症、VAP、腹腔感染的28/30天死亡率分别达32%、19%、16%[1-3],且脓毒性休克患者出现复发或持续低血压后,每延迟1小时使用抗菌药物,死亡风险增加12%[4]。针对危重症感染患者需要 “重拳猛击”的治疗策略,塔拉戈纳策略应运而生[5],即初始选用广谱抗生素全覆盖致病菌,48~72h后根据药敏结果降阶梯治疗,以减少广谱抗生素的使用、降低耐药菌产生的风险[6]。该策略可使重症感染患者临床治愈率从42.7%提升至57.9%,ICU住院时间缩短2天[7]。
多项权威指南均推荐该策略,2019 ESICM、ESCMID重症患者降阶梯共识中,除了难治性高死亡风险患者外,推荐在确定病原菌培养结果的24h内对重症患者进行降阶梯治疗[8];且针对危重HAP/VAP、脓毒症/脓毒性休克、重症复杂性尿路感染、重度腹腔感染等,均将亚胺培南等碳青霉烯类作为初始经验性治疗的重要选择[9-12]。
原研亚胺培南拥有超30年临床应用经验,是“重拳猛击”策略的核心药物,其采用超临界流体制备工艺,几乎无颗粒污染,治疗院内感染的临床有效率达65.0%,显著高于仿制药的58.7%[13]。
亚胺培南具备广谱抗菌、快速杀菌、强效杀菌三大核心特性。
广谱抗菌:亚胺培南可覆盖院内常见病原菌,包括需氧G-/G+菌、厌氧G-/G+菌,对大肠埃希菌、肺炎克雷伯菌、铜绿假单胞菌等均有活性[14]。
表1.亚胺培南的抗菌谱
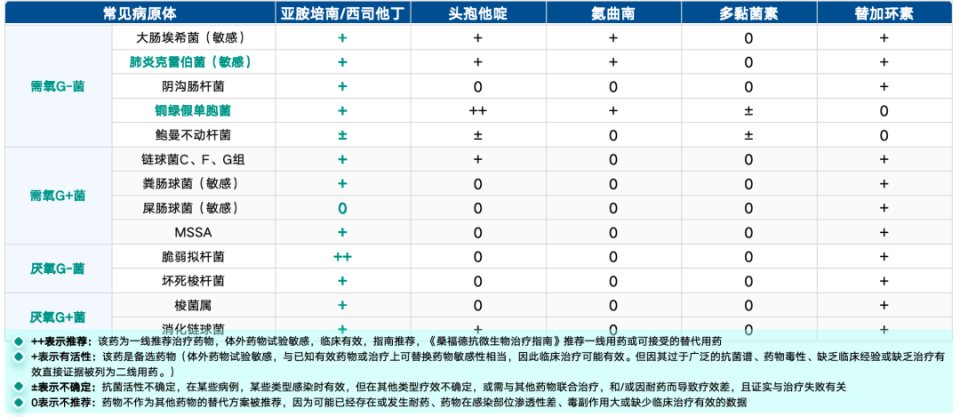
(引自讲者会议幻灯)
快速杀菌:亚胺培南对肺炎克雷伯菌及铜绿假单胞菌杀菌速度作用更快,1小时内可使铜绿假单胞菌浓度降低98.2%[15],3小时内使肺炎克雷伯菌浓度降低2.5log10,速度显著优于头孢他啶等[16]。
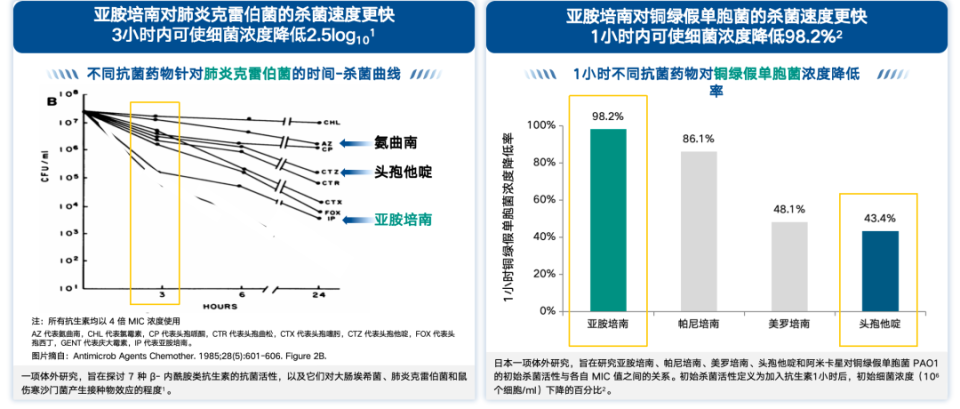
图1. 亚胺培南对肺炎克雷伯菌及铜绿假单胞菌杀菌速度(引自讲者会议幻灯)
强效杀菌:亚胺培南对肺炎克雷伯菌及铜绿假单胞菌杀菌作用更强,24小时内可完全杀灭肺炎克雷伯菌,对铜绿假单胞菌的杀菌作用为受试抗假单胞菌药物中最强[17-18]。
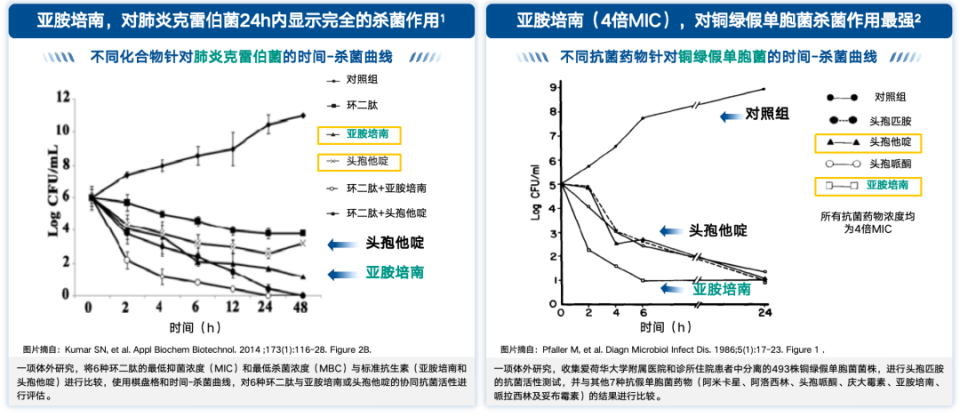
图2. 亚胺培南对肺炎克雷伯菌及铜绿假单胞菌杀菌作用
(引自讲者会议幻灯)
02
亚胺西瑞——危重症碳青霉烯耐药菌感染及高危患者治疗的升级之选
碳青霉烯耐药菌危重症感染的治疗困境
对于危重症感染患者,一旦疑似或明确碳青霉烯耐药菌感染,死亡风险更高。研究显示碳青霉烯耐药的危重症感染(如脓毒症)患者的ICU死亡率、院内死亡率分别达26.7%、32.3%,显著高于抗生素敏感患者[19]。碳青霉烯耐药菌危重症感染患者治疗需求更迫切。碳青霉烯类耐药的肠杆菌科细菌(CRE)感染进展迅速,病情凶险,治疗窗口仅有96小时,而明确病原菌感染需要52小时[20],且不恰当经验性治疗会使CRE脓毒症患者30天死亡风险增加2.48倍[21]。因此,此类患者亟需抗菌谱更广、杀菌速度更快、活性更强的药物,以提高首次治疗恰当率,快速控制感染。
亚胺西瑞的组方与优势
近年来,部分革兰氏阴性菌(尤其是铜绿假单胞菌与肺炎克雷伯菌)分别进化出了由C类 β- 内酰胺酶(如 ampC 酶)和 A 类 β- 内酰胺酶(如 KPC-2 酶)介导的亚胺培南耐药机制。恢复这类抗生素抗菌活性的一种策略是在药物中添加 β- 内酰胺酶抑制剂(BLI)。
亚胺西瑞为亚胺培南/西司他丁/瑞来巴坦固定复方制剂。其中瑞来巴坦是专为亚胺培南定制的新型β-内酰胺酶抑制剂,在阿维巴坦结构上优化升级,可抑制A/C类碳青霉烯酶,对D类酶有部分活性[22-24]。三者PK/PD协同良好,联用时药代动力学无相互影响,最大血浆浓度均在输注30分钟时达到,呈剂量依赖性增加[25],可在体内同步发挥作用。
瑞来巴坦拥有三重抗耐药机制:抑酶作用更稳定,不易从细菌细胞流出,不易受基因突变影响,可显著恢复并提升亚胺培南的抗菌活性,对KPC阳性肠杆菌的敏感率从3.7%提升至96.3%,对亚胺培南不敏感铜绿假单胞菌的敏感率达85.0%[26];同时可增强亚胺培南对敏感菌的活性,使产AmpC肠杆菌科细菌的MIC众数从0.5μg/mL降至0.25μg/mL[27]。
亚胺西瑞抗菌性能升级
1. 抗菌谱与抑酶谱升级:在注射用亚胺培南西司他丁钠抗菌谱基础上,增加对CRE/CRPA的覆盖;KPC酶突变亚型覆盖更全。
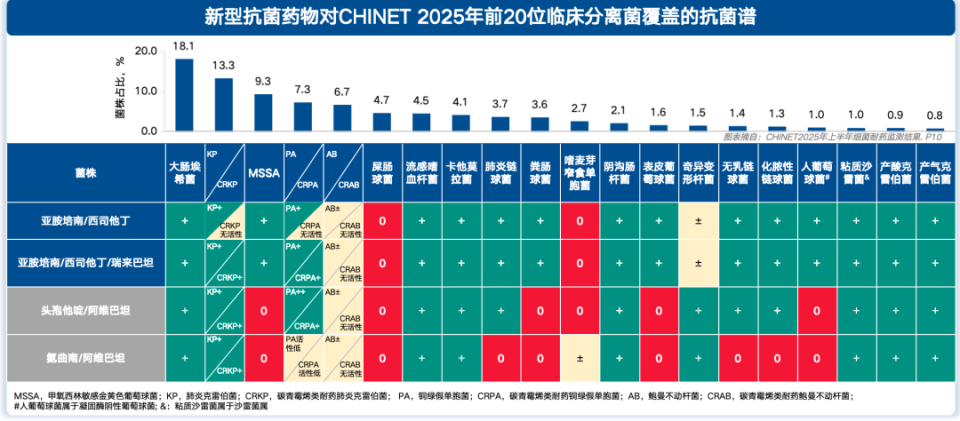
图3.新型抗菌药物对CHINET 2025年前20位临床分离菌覆盖的抗菌谱(引自讲者会议幻灯)
表2. 亚胺西瑞KPC酶抑酶谱
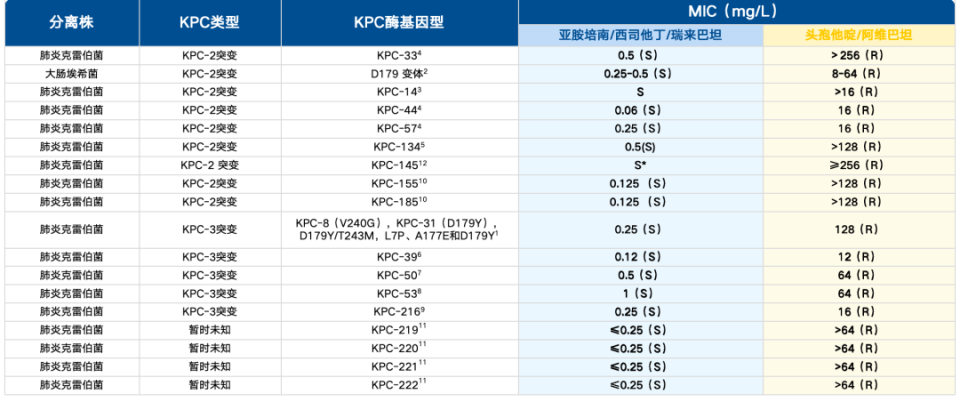
(引自讲者会议幻灯)
2. 杀菌速度升级:依托亚胺培南优异的外膜穿透能力,其对肺炎克雷伯菌的穿透速度比美罗培南快7倍以上,比氨曲南和头孢他啶至少快150倍;对铜绿假单胞菌穿透速度比美罗培南快约2倍,比头孢他啶快14倍[28-29];1倍MIC亚胺西瑞8小时内可杀灭99.9%的产KPC-CRKP菌株,且效果持续24小时,联合氨曲南时4小时即可杀灭产KPC+NDM的CRKP菌株[30-31]。
2. 杀菌强度升级:对CR-hvKP、CRPA的敏感率分别达92.5%、85.4%;接种物效应发生率仅26.3%,显著低于头孢他啶/阿维巴坦的52.6%[32-33];在肺部、腹腔、尿液等感染部位穿透率高,满足重症感染治疗需求,肺上皮衬液/血浆渗透比达55.2%,腹腔渗透率82%[34-35];且亚胺培南成分可显著降低细菌内毒素释放,减少炎症过度激活风险[36]。
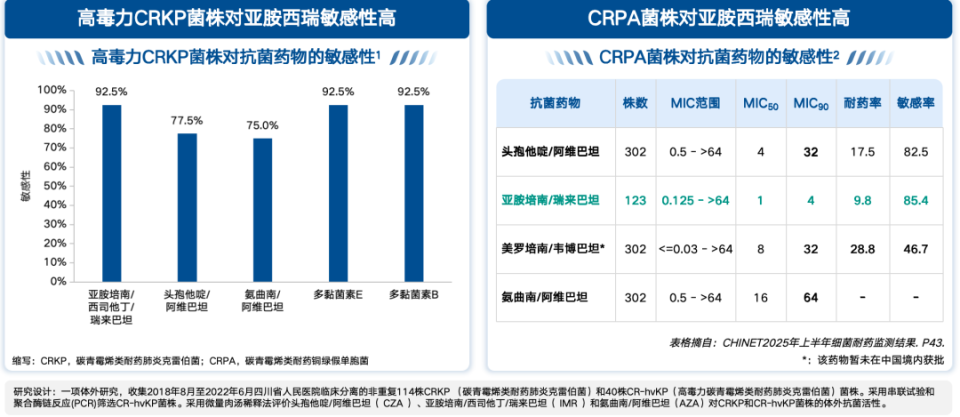
图4. CRKP、CRPA菌株对抗菌药物的敏感性
(引自讲者会议幻灯)
表3. 新型抗菌药物在肺部、腹腔、尿液等常见感染部位的渗透率
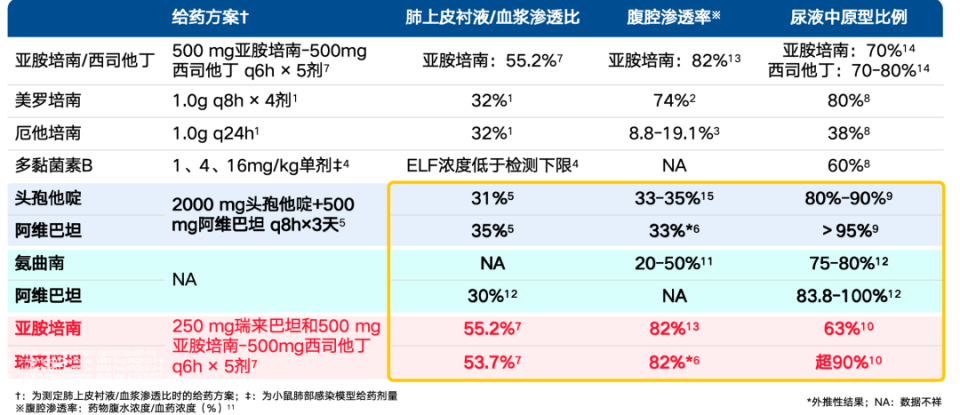
(引自讲者会议幻灯)
亚胺西瑞的真实世界疗效与指南推荐
多项真实世界研究证实亚胺西瑞疗效优异:2024年美国多中心研究显示,其治疗HABP/VABP、cUTI、cIAI患者的30天生存率达78.7%[37];2025年美国多中心研究显示,治疗MDRGNB感染的临床治愈率70.2%[38];2025年意大利多中心研究显示,治疗危重症MDRGNB感染的临床有效率75.9%,50%患者72h内实现临床改善,且治疗48小时后C反应蛋白、降钙素原水平显著下降[39];2025年美国真实世界研究显示,亚胺西瑞治疗MDR铜绿假单胞菌感染重症患者临床成功率良好,全因死亡率低[40]。
亚胺西瑞获国内外权威指南一线推荐:2024年美国感染病学会(IDSA)抗菌药物耐药革兰氏阴性菌感染治疗指南将其列为CRE、DTR-PA感染目标治疗首选药物之一[41];《高毒力碳青霉烯类耐药肺炎克雷伯菌感染诊治与防控专家共识(2025)》指出:对于高毒力CRKP感染可以参照CRE感染进行治疗,可依据细菌所产生的不同酶型选择敏感的药物进行治疗,一般以头孢他啶/阿维巴坦、亚胺培南/西司他丁/瑞来巴坦、美罗培南/韦博巴坦、氨曲南/阿维巴坦或头孢德罗单药治疗为主[42]。
表4.2024年IDSA抗菌药物耐药革兰氏阴性菌感染治疗指南对亚胺西瑞的推荐

表5.高毒力碳青霉烯类耐药肺炎克雷伯菌感染诊治与防控专家共识(2025)对亚胺西瑞的推荐

(引自讲者会议幻灯)
03
总结
危重症感染治疗的核心是“重拳猛击”后及时降阶梯,亚胺培南作为经典碳青霉烯类药物,凭借广谱、快速、强效的抗菌特性,成为非碳青霉烯耐药菌所致危重症感染的核心选择,其原研药的工艺和疗效优势为临床治疗提供可靠保障。
面对碳青霉烯耐药菌的临床挑战,亚胺西瑞实现了全方位升级,通过瑞来巴坦的三重抗耐药机制,恢复并提升了亚胺培南的抗菌活性,新增CRE/CRPA覆盖,杀菌速度更快、强度更强,且在肺部、腹腔等感染部位穿透率高,内毒素释放少。多项真实世界研究证实其治疗危重症碳青霉烯耐药菌感染的疗效优异,且获2024年IDSA指南、2025年中国高毒力CRKP感染专家共识一线推荐,成为危重症碳青霉烯耐药菌感染及高危患者的优选治疗方案。
临床应用中,需根据患者感染类型、病原菌特征、肾功能状况个体化选择亚胺培南或亚胺西瑞,严格遵循治疗策略,确保治疗的有效性与安全性。
参考文献
[1]. Xie J, Wang H, Kang Y et al. Crit Care Med. 2020 Mar;48(3):e209-e218.
[2]. Li Z, Yang L, Xu Q, Wu F. BMC Infect Dis. 2023 Oct 18;23(1):696.
[3]. Luo X, Li L, Ou S, et al. Front Med (Lausanne). 2022 Feb 25;9:839284.
[4]. Kumar A, et al. Crit Care Med. 2006 Jun;34(6):1589-96.
[5]. Intensive Care Med. 2003;29(6):876-883.
[6]. Med Klin Intensivmed Notfmed. 2014;109(3)156-161.
[7]. Intensive Care Med. 2020;46(7):1404-1417.
[8]. Tabah A, et al. Intensive Care Med. 2020;46(2):245-265.
[9]. 中华医学会呼吸病学分会感染学组. 中华结核和呼吸杂志. 2018, 41(4): 255-280.
[10]. 中国医师协会急诊医师分会, 中国研究型医院学会休克与脓毒症专业委员会. 临床急诊杂志. 2018, 19(9): 567-588.
[11]. 尿路感染诊断与治疗中国专家共识编写组.中华泌尿外科杂志. 2015, 36(4): 241-248.
[12]. 中华医学会外科学分会外科感染与重症医学学组, 等. 中国实用外科杂志,2020,40:(1)1-16.
[13]. Piyasirisilp S, et al. J Med Assoc Thai. 2010 Jan;93 Suppl 1:S117-25.
[14]. Gilbert DN, et al. 范洪伟主译. 桑福德抗微生物治疗指南(新译第53版). 北京:中国协和医科大学出版社. 2024.p77-78,80-84.
[15]. Antimicrob Agents Chemother. 1985;28(5):601-606.
[16]. Matsuda K, Inoue M. Jpn J Antibiot. 2000 Dec;53(12):667-71.
[17]. Kumar SN, et al. Appl Biochem Biotechnol. 2014 ;173(1):116-28.
[18]. Pfaller M, et al. Diagn Microbiol Infect Dis. 1986;5(1):17-23.
[19]. J Intensive Care Med. 2024 Sep;39(9):853-859.
[20. J Infect. 2016 Oct; 73(4) 336–345.
[21]. Antimicrob Resist Infect Control. 2024;13(1):84.
[22]. Heo YA. Drugs. 2021 Feb;81(3):377-388.
[23]. Clin Microbiol Rev. 2020 Nov 11;34(1):e00115-20.
[24]. Pharmacotherapy.2020 Apr;40(4):343-356.
[25]. Wang X, et al. Antimicrob Agents Chemother. 2021 Feb 17;65(3):e01391-20.
[26]. J Glob Antimicrob Resist. 2020 Jun:21:223-228.
[27]. BMC Microbiol. 2023 Jun 13;23(1):165
[28]. mBio. 2020;11(1):e03189-19.
[29]. Antimicrob Agents Chemother. 2023 Jun 15;67(6):e0160322.
[30]. Ann Clin Microbiol Antimicrob. 2023;22(1):107.
[31]. Front Microbiol. 2024;15:1210313.
[32]. Li D, et al. Microbiol Spectr. 2023 Dec 12;11(6):e0280623.
[33]. CHINET2025年上半年细菌耐药监测结果
[34]. Antimicrob Agents Chemother. 2018 Feb 23;62(3):e01411-17.
[35]. Chemotherapy. 2008;54(2):131-139.
[36]. 徐能武,袁建成,肖光夏,等. 中华烧伤杂志,2002,(02):28-30.
[37]. J Glob Antimicrob Resist. 2024;37:190-194.
[38]. Kaylee E Caniff,et al. Open Forum Infect Dis. 2025;12(4):ofaf112.
[39]. Pathogens. 2025;14(7):685.
[40]. Antimicrob Agents Chemother. 2025 Nov 7:e0132525.
[41]. Tamma PD, et al. Infectious Diseases Society of America 2024 Guidance on the Treatment of Antimicrobial-Resistant Gram-Negative Infections. Clin Infect Dis. 2024 Aug 7:ciae403.
[42]. 中国医师协会感染科医师分会,等. 高毒力碳青霉烯类耐药肺炎克雷伯菌感染诊治与防控专家共识.中华临床感染病杂志,2025,18(yufabiao) : 1-18.

徐郑丽 博士
北京大学人民医院血液科 副主任医师
中华医学会血液学分会第十二届委员会工作秘书
中国中西医结合学会第九届血液学专业委员会青委兼秘书
第一作者/通讯作者在 Leukemia, Science Bulletin, Haematologica等杂志发表SCI论文30余篇
主持国自然青年基金项目、北京大学临床医学+X项目等3项
中华医学科技青年科学技术奖
第十四届北京高校青年教师教学基本功比赛一等奖
入选北京市高创计划·春蕾项目
第四届北京大学优秀青年医师
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。