- 首页 > 正文
吴文娟教授:热带念珠菌耐药流行病学和进化机制
感染医线 发表时间:2026/4/8 17:24:32
编者按:念珠菌病是全球范围内最常见的侵袭性真菌病之一,其发病率与死亡率居高不下。在非白念珠菌中,热带念珠菌因其高侵袭性、易形成生物膜和快速产生耐药性而备受关注。近年来,热带念珠菌的耐药率在全球范围内呈现上升趋势,尤其在亚洲地区表现突出。与此同时,多重耐药菌株的出现及其独特的进化机制,给临床抗真菌治疗带来了全新挑战。在近日举行的中国医药教育协会真菌病专业委员会第六届学术会议暨第十四届深部真菌感染学术会议上,同济大学附属东方医院吴文娟教授带来了题为“热带念珠菌耐药流行病学和进化机制”的精彩报告,系统梳理了热带念珠菌的耐药流行病学、分子进化特征及适应性生存策略。《感染
热带念珠菌是全球范围内引起侵袭性念珠菌病的重要病原体之一,尤其在亚洲和北非地区检出率较高。近年来,随着抗真菌药物的广泛使用,热带念珠菌对唑类、多烯类甚至棘白菌素类药物的耐药性不断上升,多重耐药菌株的出现更是引起了临床和实验室的高度关注,日益重视对热带念珠菌的监测和耐药机制研究。
热带念珠菌病的耐药流行病学现状
真菌病对全球公共卫生构成了严重威胁。据2024年1月发表于《柳叶刀-感染病学》的一项研究统计[1],全球每年有超过655万人受到真菌病的威胁,其中超过375万人死亡,大约255万人(约68%)的死亡可能由真菌病直接引起。念珠菌的发病率约为8.05例/10万人,治疗后的念珠菌血症死亡率约为35%,未治疗的念珠菌血症死亡率约为90%。
热带念珠菌(C. tropicalis)是一种较为常见的念珠菌,但其全球地理分布存在差异。根据SENYTRY的全球监测数据[2],热带念珠菌在亚洲(尤其印度和巴基斯坦)的分离率最高(39.7%),其次为巴西(20.9%)和其他拉丁美洲国家(13.2%)。近年来,热带念珠菌对氟康唑的高耐药率已经引起了广泛关注,其耐药率在印度、中东等地区大于20%,我国和澳洲的耐药率也处于较高水平[3]。与此同时,对棘白菌素耐药的热带念珠菌也开始出现。
根据2025年最新发布的《全球念珠菌病诊断和管理指南:ECMM与ISHAM和ASM合作倡议》[4],临床实践中需结合本地流行病学与耐药模式灵活应用,以改善患者预后。我国CHIF-NET连续9年监测数据及其他研究[5-7]显示,热带念珠菌的氟康唑耐药率从5.7%增长至31.8%;而且我国也分离到了血流感染来源的对棘白菌素耐药的热带念珠菌,耐药率约为1.4%。这些数据提醒我们在临床诊疗中,需高度关注热带念珠菌耐药性的动态变化,研究其耐药机制以指导合理选择抗真菌药物,避免耐药情况进一步恶化。
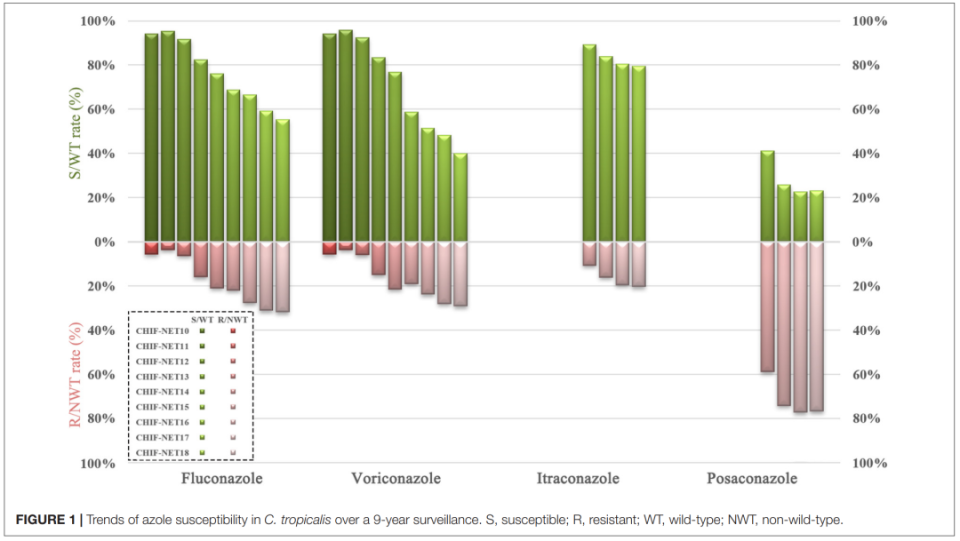
△CHIF-NET连续9年监测期间热带念珠菌的唑类耐药变化趋势(图源:参考文献[7])
热带念珠菌的耐药机制和生物学特征
热带念珠菌的抗真菌耐药性与细胞结构中的多种变化相关(见下图),如细胞壁甾醇组成改变、增大及β-1,3-葡聚糖水平变化,细胞膜上ABC转运蛋白和MFS外排泵表达增加,线粒体活性改变,细胞核内Upc2表达增加等;同时,多种基因的突变、核苷酸缺失以及FCY2杂合性缺失等基因层面变化,也通过不同途径导致了对唑类、多烯类、棘白菌素类和氟胞嘧啶等药物的耐药。
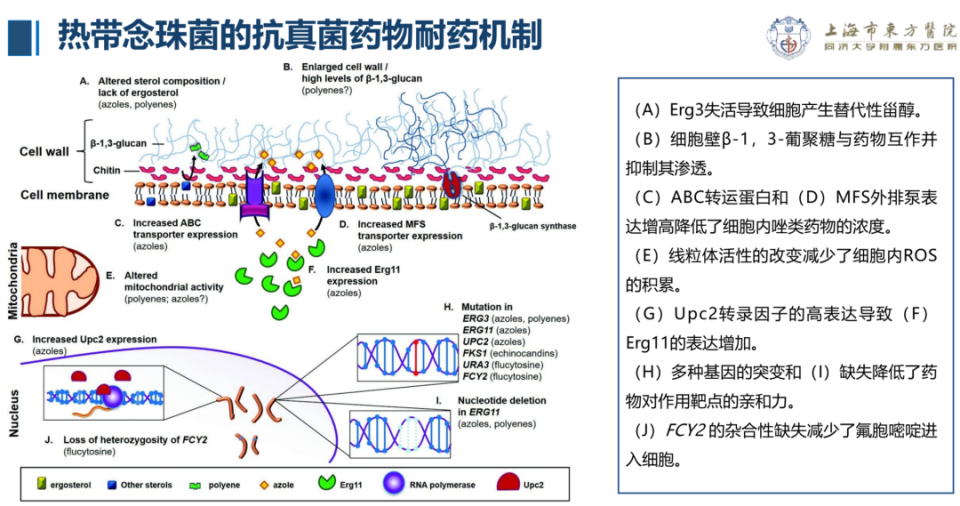
△热带念珠菌的抗真菌药物耐药机制(图源:讲者报告)
一项对热带念珠菌进行的大规模全球系统发育分析研究[8]显示,中国携带ERG11突变的高耐药群:唑类耐药群AZR的氟康唑耐药率为97.3%,近缘群AZR-ADJ的氟康唑耐药92.3%,67.9%氟康唑耐药株归属这两群并且全部携带ERG11的串联重复及关键的点突变A395T。耐药机制分析显示,AZR群ERG11基因的拷贝数和MIC正相关;AZR群Erg11的表达量与MIC值存在正相关;泛基因组分析发现在AZR群中特异的转座元件。携带ERG11突变的高耐药群须引起临床关注。
在生物学特征方面,相较于其他念珠菌,热带念珠菌具有更强的生物膜形成能力,而且对高渗环境展现出较强的适应性[2,9],这使其更容易在医院环境中传播和定植,其耐药性的演变给临床治疗带来了诸多挑战。
此外,需注意的是,有研究显示环境与临床来源的热带念珠菌具有密切关联,二者的唑类耐药率相似,唑类耐药分支的药敏表型和耐药机制相似;而且农用唑类可通过染色体倍型的可塑性诱导热带念珠菌耐药[10-11]。因此,原本用于农业的唑类药物可能间接加剧热带念珠菌耐药问题,增加临床治疗难度与不确定性。
ECIFIG热带念珠菌监测和耐药机制研究
华东地区侵袭性真菌感染协作组(Eastern China Invasive Fungi Infection Group,ECIFIG)是专注于侵袭性真菌感染监测与防控研究的区域性学术组织。它汇聚了华东地区众多医疗与科研力量,致力于从全健康角度开展多中心临床研究、监测真菌耐药趋势。
为进一步探讨MDR热带念珠菌的系统发育关系和耐药机制,通过WGS测序(n=94,MDR组30株、唑类耐药组22株,敏感组42株)和RNA-seq测序(n=50,MDR组19株、唑类耐药组21株,敏感组10株)并分析标本类型和耐药性。结果发现:(1)MDR热带念珠菌主要为DST849型,与DST225、DST506型的Azole-R都属于东亚地区临床和环境来源的热带念珠菌的主要分支CC225,表现出克隆的地域性聚集现象。(2)MDR的耐药机制较为单一,唑类包括ERG11突变和CNV,以及ERG11和CDR1高表达;棘白菌素类包括FKS1突变(S654P)等耐药机制。(3)MDR热带念珠菌通过增强生物膜形成、提高耐渗透压适应性、降低毒力,展现致病性与生存优势的平衡策略。(4)Hog1通路激活(高表达及磷酸化)可能降低DNA复制转录冲突、促进DNA损伤修复,从而增强耐药性与环境适应。
总结和展望
综上所述,热带念珠菌的抗真菌药物耐药性是一个复杂的、多因素驱动的进化过程。其主要耐药机制包括唑类相关的ERG11突变及拷贝数变异、棘白菌素相关的FKS1突变等。在进化过程中,多重耐药菌株通过增强生物膜形成、提高耐渗透压适应性、降低毒力,展现出致病性与生存优势的平衡策略。Hog1信号通路的激活在这一过程中发挥了关键作用。
面对日益严峻的真菌耐药形势,单一维度的防控策略已难以奏效。呼吁在“One Health”理念下,从环境、传播、监测、诊断、治疗和潜在干预措施等多个维度综合应对侵袭性真菌病。具体而言,应加强环境中的真菌耐药监测,控制院内传播,完善耐药监测网络,推广快速诊断技术,优化抗真菌药物使用,并积极探索新型抗真菌药物和免疫干预策略。
在精准抗真菌治疗方面,不仅依赖于正确的药物选择,更有赖于对病原体耐药机制和进化规律的深刻理解。只有在全球、区域和本地多个层面上协同努力,才能有效遏制热带念珠菌及其他耐药真菌的蔓延,改善患者的临床预后。
参考文献
[1]Denning DW. Global incidence and mortality of severe fungal disease. Lancet Infect Dis. 2024;24(7):e428-e438. doi:10.1016/S1473-3099(23)00692-8
[2]Lass-Flörl C, Kanj SS, Govender NP, Thompson GR 3rd, Ostrosky-Zeichner L, Govrins MA. Invasive candidiasis. Nat Rev Dis Primers. 2024;10(1):20. Published 2024 Mar 21. doi:10.1038/s41572-024-00503-3
[3]Oliveira JS, Pereira VS, Castelo-Branco DSCM, et al. The yeast, the antifungal, and the wardrobe: a journey into antifungal resistance mechanisms of Candida tropicalis. Can J Microbiol. 2020;66(6):377-388. doi:10.1139/cjm-2019-0531
[4]Cornely OA, Sprute R, Bassetti M, et al. Global guideline for the diagnosis and management of candidiasis: an initiative of the ECMM in cooperation with ISHAM and ASM. Lancet Infect Dis. 2025;25(5):e280-e293. doi:10.1016/S1473-3099(24)00749-7
[5]Xiao M, Chen SC, Kong F, et al. Distribution and Antifungal Susceptibility of Candida Species Causing Candidemia in China: An Update From the CHIF-NET Study. J Infect Dis. 2020;221(Suppl 2):S139-S147.
[6]Lin W, Yang Q, Lin Z, et al. Clinical and Molecular Epidemiological Characteristics of 26 Bloodstream Infection Cases Caused by Candida tropicalis. Mycopathologia. 2025;190(4):65. Published 2025 Jul 18. doi:10.1007/s11046-025-00972-4
[7]Wang Y, Fan X, Wang H, et al. Continual Decline in Azole Susceptibility Rates in Candida tropicalis Over a 9-Year Period in China. Front Microbiol. 2021;12:702839. Published 2021 Jul 9. doi:10.3389/fmicb.2021.702839
[8]Fan X, Dai RC, Zhang S, et al. Tandem gene duplications contributed to high-level azole resistance in a rapidly expanding Candida tropicalis population. Nat Commun. 2023;14(1):8369. Published 2023 Dec 15. doi:10.1038/s41467-023-43380-2
[9]Spruijtenburg B, De Carolis E, Magri C, et al. Genotyping of Candida tropicalis isolates uncovers nosocomial transmission of two lineages in Italian tertiary care hospital. J Hosp Infect. 2025;155:115-122. doi:10.1016/j.jhin.2024.10.003
[10]Hu T, Zheng Q, Cao C, et al. An agricultural triazole induces genomic instability and haploid cell formation in the human fungal pathogen Candida tropicalis. PLoS Biol. 2025;23(4):e3003062. Published 2025 Apr 1. doi:10.1371/journal.pbio.3003062
[11]Hu T, Wang S, Bing J, et al. Hotspot mutations and genomic expansion of ERG11 are major mechanisms of azole resistance in environmental and human commensal isolates of Candida tropicalis. Int J Antimicrob Agents. 2023;62(6):107010. doi:10.1016/j.ijantimicag.2023.107010



来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
