- 首页 > 正文
卢洪洲教授:HIV/AIDS功能性治愈进展及“深圳探索”
感染医线 发表时间:2026/5/10 12:57:40
编者按:在近日举行的第十一届全国艾滋病学术大会上,深圳市第三人民医院(南方科技大学第二附属医院)院长、国家感染性疾病临床医学研究中心主任卢洪洲教授系统梳理了HIV感染及艾滋病(HIV/AIDS)患者功能性治愈领域的国际前沿进展,并全面展示了其团队在该领域的系统性研究成果与战略布局。从国际最新临床试验到国内自主研发,从基础机制探索到临床转化应用,卢洪洲教授勾勒出了一幅通向艾滋病功能性治愈的清晰路线图。
近年来,HIV/AIDS功能性治愈研究在全球范围内呈现出百花齐放的态势。从广谱中和抗体到免疫调节剂,从潜伏病毒库研究到干细胞移植,从新型药物研发到精英控制者机制解析,多条技术路线同步推进,不断刷新着人们对“治愈”可能性的认知。
01
当前HIV/AIDS功能性治愈的主流策略
卢洪洲教授首先回顾了当前HIV/AIDS功能性治愈的主流策略以及近期全球重要研究进展。
单克隆抗体联合治疗
靶向于HIV病毒包膜蛋白(如gp120、gp41)或感染细胞表面CD4受体的单克隆抗体(bNABs)是近年来功能性治愈的热点,但存在疗效不确定、病毒反弹、耐药风险等挑战。2026年CROI大会报道了一项双bNABs(3BNC117-LS和10-1074-LS)的临床试验,结果显示有15人(54%)在停止ART治疗20周后仍未出现病毒反弹。双bNABs在一定程度上显示了延缓病毒反弹的潜力。
免疫调节剂疗法
通过调节机体免疫系统辅助抗病毒治疗是HIV/AIDS功能性治疗的另一大策略,在PD-1免疫检查点抑制剂基础上提高免疫调节治疗的疗效成为新的探索方向。2026年CROI大会报道的一项全球Ⅱ期随机对照试验,采用抗PD-1(budigalimab)联合抗α₄β₇整合素(trosunilimab)的策略,结果显示各组在反弹时间以及重启ART前的病毒载量峰值均无显著差异。α₄β₇整合素是淋巴细胞表面的重要黏附分子,介导淋巴细胞向肠道等组织的迁移,理论上抗α₄β₇整合能够与抗PD-1协同增强免疫作用,但该研究结果并未取得预期结果。
潜伏病毒库研究
潜伏病毒库是实现功能性治愈的核心障碍。2026年发表在《Nature》杂志上的一项研究成功分离出可不断增殖、持续产毒却不死亡的HIV潜伏库克隆(ARCs)。这些潜伏克隆平时对T细胞刺激不敏感,但在持续CTL压力下可被逐步清除。尤为重要的是,研究发现调节性T细胞来源的潜伏克隆存在可被药物逆转的免疫抗性。2026年CROI 大会报道的研究则发现其他清除潜伏病毒库的潜在策略。例如:(1)依非韦伦介导 CARD8 活化可以缩减HIV潜伏库,有6名接受依非韦伦治疗的参与者在4个月后的潜伏细胞减少了20%~50%;(2)N-803则是一种受体超激动剂,可促进NK和CD8细胞的增殖与功能,研究发现N-803可使完整HIV潜伏库一过性减少,并促使免疫细胞向干细胞样表型转化,但联合bNAbs未达到预期的 ART 中断后病毒控制效果。
干细胞移植
目前,全球已报道8例通过干细胞移植实现功能性治愈的HIV/AIDS患者,大多数患者接受的干细胞供体携带CCR5-Δ32纯合突变。 2025年《Nature》杂志报道了一例通过杂合型CCR5Δ32干细胞移植实现HIV-1持续6年缓解的案例;2024年《Nature Medicine》则报道了一例接受野生型CCR5供者移植的HIV感染者实现32个月持续病毒缓解。这些特殊的个案为扩大干细胞移植的适用范围提供了线索。
长效ART预防
近年来,随着药物递送技术取得突破性进展,众多长效ART的问世提供了新的长效预防方案。一项Ⅰ期开放研究对来那帕韦(Lenacapavir)的配方进行了升级,使其预防作用可持续长达一年。研究显示,每年一次肌肉注射与每年两次皮下注射的来那卡帕韦均能达到有效血浆浓度。这意味着,未来HIV预防可能从目前的每两个月一次注射进一步延长至每年一次,将极大提高高风险人群的依从性和预防覆盖率。
新型长效INSTIs
整合酶抑制剂(INSTIs)已成为当前ART方案的“主力军”,基于INSTIs的单片制剂虽然实现用药负担减小,当仍不能摆脱每日服药。2026年CROI大会报道的一项I期研究显示,VH-184作为第三代INSTI的应用前景可期,单次注射VH-184可维持药物体内浓度长达6至7个月,展现出每年两次给药的潜,且相较于当前常用的INSTI方案,VH-184在耐药HIV株中显示出更强的活性和更优化的耐药性特征。
精英控制者的免疫机制
精英控制者研究为理解HIV自然控制机制提供了独特窗口。2025年《Nature》杂志发表的研究揭示了CD8⁺T细胞干性在实现停药后病毒控制中的关键作用:在广谱中和抗体治疗后实现持久病毒控制的HIV感染者中,其CD8⁺T细胞在干预前即具备更强的增殖能力、干细胞样记忆表型和代谢适应性,而bNAb治疗可进一步增强这些特征。这表明,CD8⁺T细胞的干细胞样特性是实现HIV病毒血症干预后控制的前置条件。另一项发表于2025年《Nature》的研究进一步证实了这一发现。组合免疫疗法(疫苗+bNAbs+TLR9激动剂)可使70%的HIV感染者在停药后实现持续病毒控制,其作用机制在于:bNAb延缓病毒反弹,并为干细胞样CD8⁺T细胞的快速扩增争取了时间窗口。该研究在临床试验中验证了“诱导干细胞样CD8⁺T细胞”作为功能性治愈策略的可行性,为后续联合免疫治疗的设计提供了重要参考。
02
HIV/AIDS功能性治愈的“深圳探索”
近年来,作为国家感染性疾病临床医学研究中心主任,卢洪洲教授带领深三院团队在艾滋病功能性治愈领域进行了系统而深入的研究布局,形成了“学科-人才-项目-平台-成果-产品”一体化创新发展模式。
在基础机制研究方面,团队聚焦于HIV储存库这一核心障碍,系统探索了潜伏病毒的生物学特征。通过对HIV病毒整合位点检测技术的优化,特别是LTA-PCR检测技术的建立,团队实现了对潜伏库的高灵敏度监测。研究还发现,加氧环化酶(IDO)与外周血HIV活跃程度呈正相关,可作为HIV感染者免疫标志物。在潜伏激活剂方面,团队首次报道了BMS-986158促进HIV-1潜伏激活的作用,为开发新型潜伏逆转剂提供了候选分子。相关成果发表于《Clinical Infectious Diseases》《mBio》《Clinical and Translational Medicine》《Pharmaceuticals》等国际期刊。
在病毒学基础研究方面,团队针对中国5种主流HIV-1亚型(B、CRF01_AE、CRF07_BC、CRF08_BC、CRF55_01B),系统解析了gp140-CD4结合特性、Temsavir(一种新型HIV-1附着抑制剂)抑制效果及耐药机制。研究发现,B亚型gp140与CD4结合亲和力最强(KD=79 pM),而CRF重组亚型的结合力显著降低。尤为关键的是,Temsavir对B亚型的抑制率仅为35.7%。这一发现对于指导中国HIV感染者中Temsavir的临床应用具有重要意义,提示不同亚型对该药物的敏感性存在显著差异。
团队还聚焦于HBV/HIV共感染、HBV/TB共感染、免疫重建不全等特殊人群的诊疗优化:(1)作为主要研究者参与了B/T/TAF一线治疗HBV/HIV共感染的全球多中心III期ALLIANCE研究,相关研究成果发表于《The Lancet HIV》。(2)团队首次采用350和500个/μL双CD4⁺ T细胞阈值定义免疫重建不全,系统分析了其与艾滋病定义性疾病和非艾滋病定义性疾病的长期关联,填补了免疫重建不全对非艾滋病定义性疾病影响的研究空白。(3)团队利用单细胞测序技术从外周血和肺泡灌洗液两个角度绘制了HIV-1/Mtb共感染人群的单细胞图谱,鉴定出可用于HIV-1和Mtb共感染的生物标志物。(4)此外,团队还针对HIV/AIDS患者的合并症管理、行为心理学调查等方面,优化HIV/AIDS患者的全方位身心干预策略。
卢洪洲教授团队持续探索艾滋病功能性治愈新策略,从精准检测到全面评估,再到精准靶向治疗,有望在诸多领域实现更多“深圳案例”的突破。
03
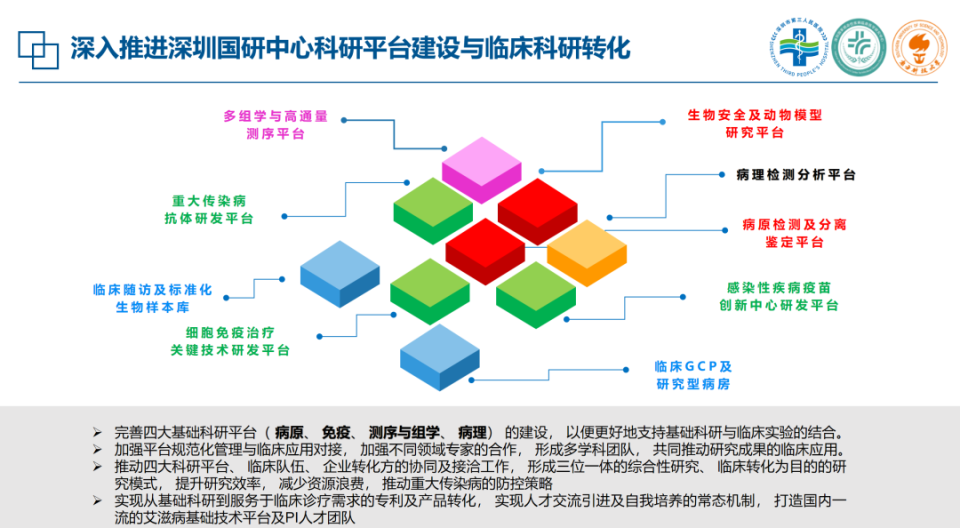
构建三位一体的综合性研究与转化模式
卢洪洲教授指出,该团队在HIV/AIDS功能性治愈的全方位探索,建立于国家感染性疾病临床医学研究中心以及深圳国研中心四大基础科研平台(病原、免疫、测序与组学、病理)的建设,形成了完整的从基础科研到临床转化的技术链条,并有力推动了四大科研平台、临床队伍、企业转化方的协同与接洽,构建了三位一体的综合性研究与转化模式。2026年1月11日,由卢洪洲教授牵头承担的“新发突发与重大传染病防控”国家科技重大专项——“功能性储存库内潜伏病毒再激活的功能性治愈临床研究”项目正式启动,直指全球医学界长期面临的重大挑战。
值得强调的是,卢洪洲教授团队的研究视野并不局限于HIV领域。在新冠疫情期间,团队发布了全球首篇新冠病毒全基因测序研究成果,揭示了临床结局相关的病毒和宿主因子,并主持了多项抗新冠病毒药物临床试验,助力小分子抗病毒药物成功上市。多项研究成果发表于NEJM、柳叶刀子刊、STTT等顶级期刊。团队因此荣膺诸多嘉奖和荣誉,如卢洪洲教授个人及团队先后荣获法国医学科学院夏邦克-杜博赛奖、荣获第十八届“药学发展奖·突出成就奖”、2025全球医疗科技创新转化奖,并收到国务院联防联控机制科研攻关组疫苗研发专班的感谢信。
在医工融合领域,卢洪洲教授团队自主研发了医疗物联网非接触式ICU监护技术,在国际顶级期刊《IEEE Internet of Things》上发表,使临床医生能够及时远程评估ICU患者的生命体征状况,推动生命监护向“非接触式”变革发展。此外,团队还牵头开展了首台国产ECMO的临床验证研究,并致力于超级细菌噬菌体精准治疗的探索。
04
总结和展望
卢洪洲教授深耕感染和传染病防治事业近40年,从临床医疗到教学科研,从基础探索到成果转化,在艾滋病、新发突发传染病防治领域取得累累硕果,入选ScholarGPS 2024年全球前0.05%顶尖科学家榜单。在南下特区后,其带领的深圳团队以“亚洲一流、世界领先”为目标,按照医疗水平国际化、环境设施现代化、医疗服务精细化、诊疗流程规范化、运营管理智慧化的标准,构建集医疗、教学、科研、预防及预警预测为一体的国家感染性疾病临床医学研究中心和国家综合性区域医疗中心。
在艾滋病功能性治愈这一全球性挑战面前,卢洪洲教授团队正以系统性的研究布局、前沿的技术平台和务实的临床转化,逐步揭开HIV潜伏病毒库的“黑色面纱”,力求实现艾滋病患者的功能性治愈乃至彻底治愈。正如卢教授在STTT发表文章时所言,“星星之火可以燎原”——每一份基础研究的突破、每一项临床试验的推进,都在为实现“红丝带”所象征的终结艾滋病流行的人类共同愿景贡献力量。

卢洪洲 教授
深圳市第三人民医院党委副书记、院长
传染和感染性疾病国家临床医学研究中心主任;南方科技大学医学院副院长、讲席教授;内科学、公共卫生管理与护理学博士生导师;美国微生物科学院fellow、深圳市首届疫情防控公共卫生专家组组长;教育部长江学者、国家百千万人才工程、“有突出贡献中青年专家”、享受国务院特殊津贴;深圳市国家级领军人才、上海领军人才;《iLABMED》主编;曾担任复旦大学附属华山医院院长助理、上海市公共卫生临床中心党委书记。入选美国斯坦福大学2021-2025年全球前2%顶尖科学家榜单及《终身科学影响力排行榜》、ScholarGPS终身与近5年全球前0.05%顶尖科学家榜单。
学术任职
世界卫生组织新发传染病临床诊治培训与研究合作中心主任;国际流感和呼吸道病毒感染学会(ISIRV)抗病毒小组(AVG)委员;国家疾病预防控制专家委员会委员,国家卫建委艾滋病、流感、埃博拉病毒病、感染病质量控制中心专家,国家新冠病毒病救治专家组与境外抗疫专家组后方支持团队成员
中国性病艾滋病防治协会学术委员会副主任委员兼艾滋病合并结核专业委员会主任委员,中华医学会感染病学分会艾滋病专业学组副组长,中华医学会热带病与寄生虫分会前任主任委员兼艾滋病学组组长,欧美同学会(中国留学人员联谊会)医师协会传染病分会主任委员,上海市医学会感染病学分会前任主任委员
广东省医学会微生态医学分会主任委员、深圳市医学会感染病分会主任委员、国家卓越期刊iLABMED主编
科研成果
先后承担国家科技重大专项(5项),国家重点研发计划(2项)、“863”、国家自然科学基金 (9项,含2项重大研究项目),美国盖茨基金、国家临床重点专科等63项科研课题
以第一作者或通讯作者在国内外发表各类论文500余篇,其中包括在Nature、New England Journal of Medicine、Lancet Microbe、Signal Transduction and Targeted Therapy等SCI期刊发表论著360篇;已主编专业书籍15部;授权专利15项
获奖荣誉
法国国家科学院“夏邦克-杜博赛”奖(2020),国家科学技术特等奖(2017),中国药学发展奖“突出成就奖”(2024)、中华医学科技奖(2021),上海市科技进步奖(2004,2009,2021),上海市医学科技奖(2016),上海市预防医学会科学技术奖(2021)、广东省优秀医药成果奖(2025)等国家及省部级科技成果奖10余项
“人民名医∙卓越建树”奖(2022),全国卫生系统先进个人、“最美援外医生”;联合国艾滋病规划署"精忠奖"等荣誉。
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
