- 首页 > 正文
唐小平教授:HIV/HBV合并感染HBV功能性治愈研究进展
感染医线 发表时间:2026/5/7 17:09:15
编者按:HIV与HBV合并感染是全球重要的公共卫生挑战,二者传播途径高度重叠、在宿主体内相互作用,显著加快肝纤维化、肝硬化及肝细胞癌的发生进程,同时削弱免疫重建效果,大幅提升不良临床结局风险。随着抗逆转录病毒治疗(ART)的广泛普及,实现HBV功能性治愈已成为改善HIV/HBV合并感染者长期预后的核心目标。2026年4月在重庆召开的第十一届艾滋病学术大会上,广州医科大学附属市八医院唐小平教授系统报告了HIV/HBV合并感染的流行特征、病毒相互作用机制、HBsAg阴转规律与预测因素,以及ART联合干扰素治疗的研究进展,为我国合并感染的精准治疗与治愈策略提供了高质量临床证据。本文基于大会报告核心内容,全面梳理HIV/HBV合并感染的诊疗现状与功能性治愈前沿成果,为临床实践、科研方向及公共卫生防控提供权威参考。
——基于第十一届艾滋病学术大会唐小平教授主题报告
01
HIV/HBV合并感染流行现状与疾病负担
1.1全球流行特征
慢性乙型肝炎与艾滋病均为危害严重的病毒性传染病,给全球带来沉重疾病负担。根据世界卫生组织(WHO)数据,截至2022年底,全球慢性HBV感染者约2.54亿[1],全球HIV感染者总数约3900万(范围3310万–4570万)[2]。在HIV感染者群体中,HBV合并感染的流行率达到7.4%[3],全球约1%的HBV感染者(约270万人)同时合并HIV感染,两类病毒的传播重叠性使合并感染成为艾滋病与病毒性肝炎防控共同关注的重点人群。
从疾病负担分布来看,全球约三分之二的HBV感染集中在少数国家。其中中国以7970万感染者、占全球31.5%的比例位居首位,印度、印度尼西亚、尼日利亚、埃塞俄比亚、孟加拉国、越南、菲律宾、巴基斯坦等国同样负担突出,提示HIV/HBV合并感染的防控工作在中高流行地区尤为关键与迫切。
1.2中国流行特征
我国HIV感染者的HBV合并感染率为11.29%,显著高于全球平均水平,且呈现明显的地域差异与传播途径差异。地域分布上,南部地区合并感染率最高(14.18%),西部地区次之(10.73%),北部地区最低(6.36%)。南部地区男性HIV感染者的HBV感染率为女性的1.29倍,性别差异突出[4]。
在传播途径方面,注射吸毒传播人群的合并感染率最高(12.76%),随后依次为异性性传播(11.32%)、血液或血液制品传播(11.22%)、传播途径不详(10.34%)、同性性传播(9.58%),母婴传播最低(2.87%)[4]。我国目前约有7500万HBV携带者,占全国总人口比例5.86%,庞大的HBV感染基数与HIV流行相叠加,使HIV/HBV合并感染成为我国传染病防治领域的重点与难点人群[5-7]。
分区域数据显示(图1),广东省HIV患者中HBV流行率为13.2%,南方地区整体为12.8%,东部地区14.5%,中部5.0%,北部6.9%,西部5.9%,母婴传播为主,病毒株以B型、C型为主[4,8-10]。与此同时,各区域HIV/HCV合并感染率同样存在明显差异,提示不同地区应当结合本地流行特点,制定差异化、精准化的防控与治疗策略。
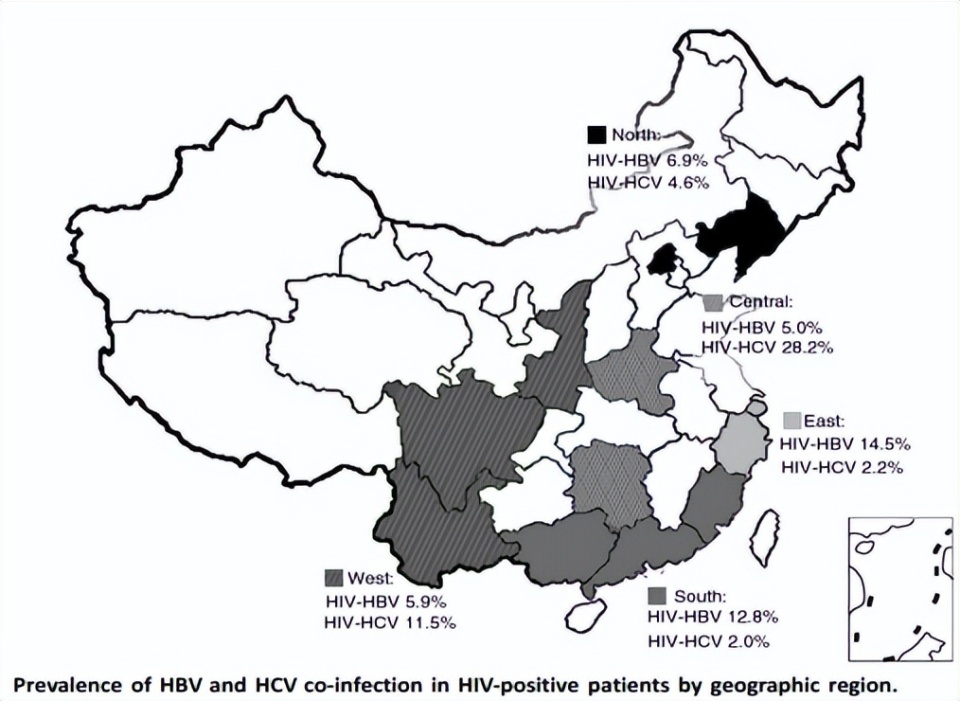
图1. 我国HIV患者中HBV流行率(来自讲者PPT)
02
HIV与HBV相互作用的临床及免疫机制
HIV与HBV在人体内形成复杂的双向相互作用,既会加速HBV相关肝病的进展,也会削弱HIV感染者的免疫重建效果,最终显著提升肝硬化、肝功能衰竭、肝细胞癌及死亡等不良临床结局的风险。
2.1HIV对HBV感染的影响
临床表现方面,HIV感染会大幅升高HBV急性感染后转为慢性感染的风险,HIV感染者急性HBV感染后进展为慢性HBV的风险比HIV阴性人群高6倍[11]。美国MACS研究(1985-2013)显示,接受ART治疗的HIV感染者合并HBV的比例显著低于未接受ART治疗者(8% vs.18%),提示及时规范的ART可在一定程度上降低合并感染风险[12]。
病毒学层面,HIV/HBV合并感染者的HBV DNA中位水平更高[13],在相当HBV DNA水平下,HIV/HBV合并感染者的HBsAg水平高于HBV单一感染者(4.29 vs. 3.94 log10 IU/mL,P = 0.016) [14]。肝病进展方面,与HBV单一感染相比,HIV/HBV合并感染者发生显著肝纤维化的风险增加约2.6倍(OR:2.61,95%CI:1.26~5.44)[15],院内死亡风险更高,且更易合并肝硬化及门脉高压相关并发症,肝病进程明显加快。
免疫机制上,HIV可引发“肠漏综合征”,造成微生物移位,进而导致肝内持续炎症与促纤维化信号激活;同时造成“促炎-抗病毒因子失衡”,IL-6、TNF-α等促炎因子升高,IFN-γ等抗病毒因子不足,TLR7、TLR9信号通路异常;此外,HBV特异性CD8+T细胞功能受损、B细胞应答下降,共同导致HBV清除障碍,病毒持续复制[16-22]。
2.2HBV对HIV感染的影响
HBV合并感染可显著延缓HIV感染者的免疫重建进程。多项队列研究证实,在相当的HIV病毒学抑制率水平下,HBV合并感染者的CD4恢复幅度更低,早期死亡风险更高[23-24]。同时,HIV/HBV合并感染会显著升高肝毒性发生风险,中国西北 4,690 例 MSM 队列显示,HIV/HBV 共感染显著增加任何级别肝毒性风险(HR 1.19)及 ≥3 级严重肝毒性风险(HR 3.16)[25]。罗马尼亚 HIV 队列研究表明,与HIV单一感染组相比,合并HBV感染组的ALT、GGT、总胆红素、淀粉酶、脂肪酶等指标异常更为常见[26]。
此外,HBV合并感染还会加重其他系统的健康负担。亚太地区多国HIV队列数据显示,HBV合并感染者的肾功能损害比例显著更高(14.8% vs. 7.6%)[27]。欧洲COHERE研究提示,在未接受和接受ART的HIV感染者中,感染HBV增加患非霍奇金淋巴瘤风险的HR分别为1.33和1.74[28]。
免疫机制方面,HBV可通过抑制TLR信号、RIG-I/MAVS通路等方式抑制I型干扰素应答,实现免疫逃逸;HBV的X蛋白(HBx)可作为核内共激活因子,与T细胞激活信号协同,超诱导HIV复制并激活HIV转录;HBV特异性CD8+T细胞高表达PD-1等抑制性受体,免疫耗竭状态更为严重,进一步削弱机体整体抗病毒免疫能力[29-34]。
03
HBV功能性治愈定义与核心临床意义
慢性乙型肝炎功能性(临床)治愈是现阶段乙肝治疗所追求的理想终点,也是HIV/HBV合并感染管理的核心目标。根据中国慢性乙型肝炎功能性(临床)治愈临床实践专家共识,其定义为:停止抗病毒治疗24周后,持续出现血清乙型肝炎表面抗原阴转(HBsAg<0.05 IU/mL)、HBV DNA低于定量下限(<10 IU/mL),伴或不伴抗-HBs出现;同时满足血清HBeAg持续阴转、ALT复常,最终实现肝组织学改善并降低HCC发生风险,肝脏中可残留cccDNA及整合HBV DNA[35]。
HBsAg阴转是降低HCC风险的最重要评估指标之一,一项台湾地区的前瞻性研究纳入11 1893名未患HCC男性,探究HBeAg以及HBsAg与HCC患病率之间的关系,结果表明HBsAg阳性人群的HCC累计发病率和HCC风险显著高于HBsAg阴性人群,实现HBsAg阴转即临床治愈后,可进一步大幅降低HCC风险[36-37]。
04
HIV/HBV合并感染者HBsAg阴转预测因素
广州医科大学附属市八医院团队针对HIV/HBV合并感染开展了一系列大样本、长期随访队列研究,系统揭示了合并感染者在ART治疗下HBsAg阴转的发生率、临床特征及关键预测因素,为临床筛选治愈优势人群提供了重要依据。
4.1HBsAg阴转预测因素
广州八院研究团队对1550例HIV/HBV合并感染者进行长期随访,平均随访时间4.7年。结果显示,共有126例(8.1%)患者实现HBsAg阴转。多因素Cox回归分析确认了三项HBsAg阴转的独立预测因子,一是基线HBsAg<1500 COI,二是ART启动后6个月内ALT升高>2倍正常值上限,三是HBV基因型为B型[38]。
国际多项队列研究一致验证(图2),基线低HBsAg水平(≤1000IU/mL)是HBsAg阴转的最强预测因素;在HBeAg阳性的参与者中,HBsAg loss与较低的基线HBV RNA水平和较高的基线HBV DNA水平有关;HBcrAg水平主要用于反映治疗期间病毒转录活性的下降趋势,预测HBsAg loss的价值不如定量HBsAg和HBV RNA。部分研究显示,基线CD4+T细胞计数≤200 cells/μL也与阴转相关,提示病毒载量、基因型与宿主免疫状态共同决定治愈概率[39-41]。
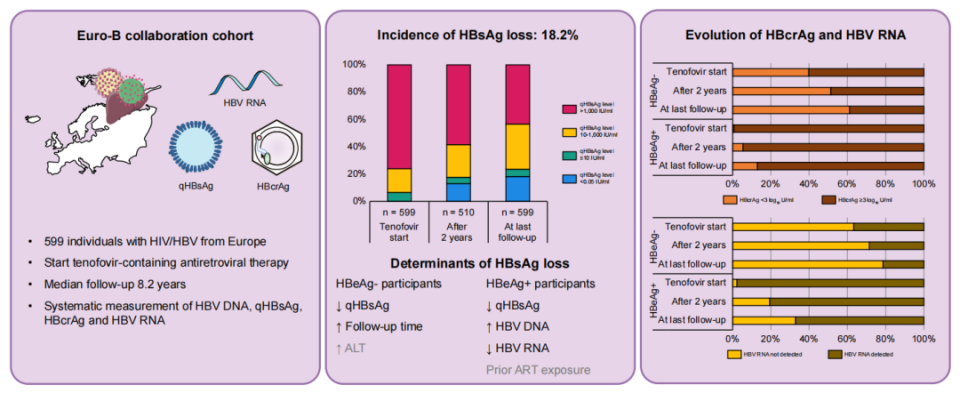
图2. HIV/HBV合并感染者HBsAg 转阴与HBV新型标志物的关系(来自讲者PPT)
HepaticFlare被定义为ART启动后12个月内,ALT升高超过正常上限5倍,且无HBV DNA或HBsAg骤升。广医八院1354例纳入分析的患者中[42],6.5%出现HepaticFlare,且多见于基线免疫功能较低但后续免疫重建增强的患者。3年、5年、10年HBsAg阴转累积发生率分别为6.4%、8.9%、12.9%,与无HepaticFlare组相比,发生HepaticFlare的患者HBsAg阴转率显著更高(13.6% vs. 6.9%,P=0.018)。不同模型的多因素分析表明, Hepatic Flare与HBsAg 转阴率独立相关,特别是在免疫功能低下、ALT正常、基线时HBV DNA和HBsAg水平较高的患者中。ART后的Hepatic Flare与HBV/HIV感染患者的HBsAg血清清除率有关。
4.2新型病毒标志物的临床价值
实现HBsAg阴转并不完全代表病毒彻底清除。广州八院研究发现,43.9%的HBsAg阴转患者pgRNA仍呈阳性,提示肝内病毒复制模板可能持续存在,仍存在病毒再激活风险。因此,在评估HIV/HBV合并感染者是否达到真正功能性治愈时,有必要联合检测pgRNA、HBcrAg等新型标志物,以更准确判断残留病毒活性,避免误判治愈状态[43]。
05
HIV/HBV合并感染治疗进展与治愈策略
5.1一线ART方案疗效与安全性
ALLIANCE研究是HIV/HBV合并感染领域的关键3期随机对照研究,对比了初治合并感染者使用B/F/TAF与DTG+F/TDF的疗效。结果显示,治疗48周时,两组HIV-1RNA抑制率相近(95.1% vs. 91%),但B/F/TAF组HBV DNA抑制率显著更优(63% vs. 43.4%)。96周时两组病毒抑制率无显著差异,但B/F/TAF组HBeAg、HBsAg消失及血清学转换率更高,肾脏与代谢安全性更佳[45]。
开放标签延展期结果显示,由DTG+F/TDF转换为B/F/TAF后,可维持高水平HIV与HBV病毒学抑制,无研究药物相关严重不良事件,无因不良事件停药;基线ALT异常者半数以上恢复正常,中位eGFR显著改善,代谢指标保持稳定,为经治患者的方案优化与转换提供了坚实依据[46]。
5.2ART联合干扰素治疗的研究进展
干扰素兼具直接抗病毒与免疫调节作用,在单一HBV感染的优势人群中,可实现30%~60%的功能性治愈率,但在HIV/HBV合并感染人群中相关研究极少[47-48]。针对这一临床空白,广州医科大学附属市八医院开展了一项前瞻性、开放性队列研究,纳入经ART≥1年、HIV-1RNA<20c/mL、HBV DNA<100IU/mL、CD4+≥200cells/μL、HBsAg<1500IU/mL的经治患者,按1:3比例分为ART联合干扰素组与单纯ART组。
结果显示,随访至48周时,ART联合干扰素组HBsAg清除率达39.1%,血清学转换率达30.4%;而单纯ART组仅2%实现HBsAg清除,无1例达到血清学转换,差异具有高度统计学意义。对于ART联合干扰素组基线资料进行多因素COX回归分析(图3),基线HBV RNA<50 拷贝/mL是发生HBsAg清除的有利因素。基线CD8+计数与HBsAg清除相关,提示免疫状态可能影响干扰素治疗效果,为临床筛选治愈优势人群提供了明确、可操作的标准。
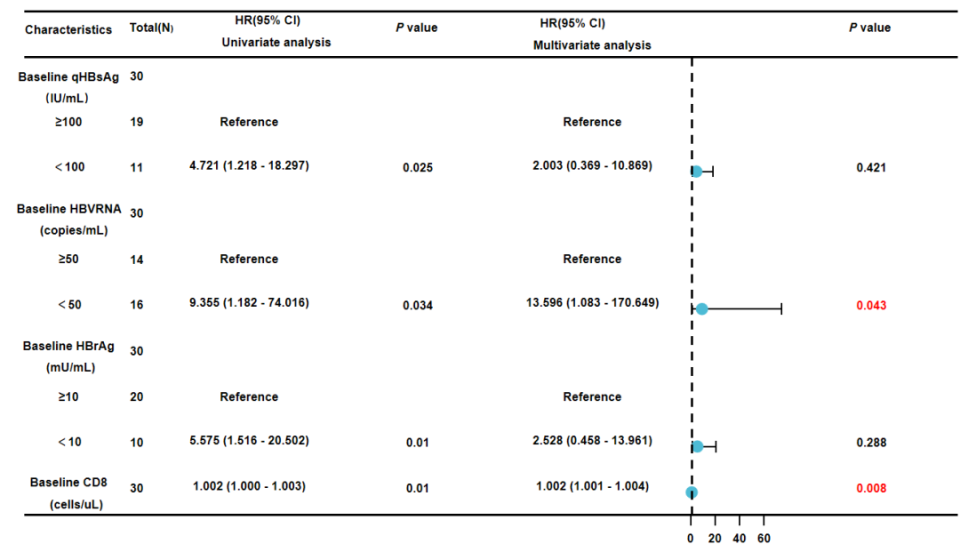
图3. HBsAg清除多因素COX回归分析(来自讲者PPT)
06
总结
HIV/HBV合并感染在我国保持较高流行率,两类病毒在体内相互作用,形成“双向恶化”效应,显著加速肝病进展、削弱免疫重建、增加肝硬化、肝细胞癌及死亡等不良结局风险。长期规范ART可实现一定比例的HBsAg阴转,基线低HBsAg水平、HBVB基因型、ART早期ALT升高及HepaticFlare是HBsAg阴转的重要预测因子,但HBsAg阴转后仍需联合检测pgRNA等新型标志物,以更准确评估残留病毒活性,判断功能性治愈状态。
ART联合干扰素治疗可显著提高HIV/HBV合并感染者的HBV功能性治愈率,48周HBsAg清除率接近40%,为临床实现治愈提供了安全、高效、可推广的路径。未来应进一步优化优势人群筛选标准、完善个体化治疗方案与疗程策略、长期评估预后及肝癌预防效果,推动HIV/HBV合并感染从单纯病毒抑制迈向功能性治愈,最终降低整体疾病负担,全面改善患者长期生存质量。
参考文献
[1] WHO. Hepatitis B fact sheet.
[2] WHO. HIV/AIDS fact sheet.
[3] Leumi Steve, et al. Clinical infectious diseases, 2020, 71 (11):2799-2806.
[4] Xie J, Han Y, Qiu Z, et al. J Int AIDS Soc, 2016,19 (1):20659.
[5] Zhao YS, Su SI, Lv CX, et al. Int J STD AIDS, 2012,23 (9):639-643.
[6] Chen X, He JM, Ding LS, et al. Arch Virol, 2013,158 (9):1889-1894.
[7] Huang SM, Cai WP, Hu FY, et al. Int J STD AIDS, 2016,27 (10):890-897.
[8] Shen YZ, Wang ZY, Qi TK, et al. HIV Med, 2013,14 (3):169-175.
[9] 曹阳,周明浩,翟祥军。中华流行病学杂志,2021,42 (2):327-334.
[10] Yu S, Yu C, Li J, et al. Virol J, 2020,17 (1):127.
[11] Rajbhandari R, et al. J Viral Hepat, 2016,23 (10):820-829.
[12] FaladeNwulia O, et al. AIDS, 2021,35 (6):991-993.
[13] Greer AE, et al. J Acquir Immune Defic Syndr, 2017,76 (4):388-393.
[14] Jaroszewicz J, et al. J Viral Hepat, 2016,23 (10):820-829.
[15] Hawkins C, et al. J Acquir Immune Defic Syndr, 2017,76 (3):298-302.
[16] Chang JJ, et al. J Virol, 2009,83 (15):7649-7658.
[17] Singh KP, et al. AIDS, 2017,31 (15):2035-2052.
[18] Ouyang J, et al. Front Immunol, 2022,12:755890.
[19] Mac PA, et al. Front Immunol, 2026,17:1789692.
[20] Kayesh MEH, et al. Int J Mol Sci, 2023,24 (11):9624.
[21] Singh KP, et al. PLoS Pathog, 2020,16 (9):e1008744.
[22] Hong F, et al. PLoS One, 2012,7 (3):e33659.
[23] Wandeler G, et al. J Infect Dis, 2013,208 (9):1454-1458.
[24] Mbae M, et al. AIDS, 2019,33 (8):1404-1406.
[25] Ma X, et al. PLoS One, 2025,20 (10):e0333371.
[26] Marin RC, et al. Pharmaceuticals (Basel), 2025,18 (5):688.
[27] Vu TT, et al. AIDS Res Ther, 2025,23 (1):14.
[28] Wang Q, et al. Ann Intern Med, 2017,166 (1):9-17.
[29] GómezGonzalo M, et al. J Biol Chem, 2001,276 (38):35435-35443.
[30] Mu Y, et al. Virus Res, 2011,156 (1-2):81-9.
[31] Sun B, et al. Hepatology, 2024,80 (3):649-663.
[32] Chen P, et al. World J Hepatol, 2025,17 (6):104533.
[33] Sausen DG, et al. Int J Mol Sci, 2022,23 (24):15973.
[34] Preechanukul A, et al. Gut, 2025.
[35] 中国慢性乙型肝炎功能性(临床)治愈临床实践专家共识。中华肝脏病杂志,2025,33 (10):977-987.
[36] Yip TC, et al. J Hepatol, 2019,70 (3):361-370.
[37] HWAIIYANG, et al. N Engl J Med, 2002,347 (3).
[38] He Y, Lin W, Li H, et al. Chin Med J (Engl), 2023,136 (22):2686-2693.
[39] Béguelin C, et al. HIV Med, 2025,26 (5):813-819.
[40] Jain MK, et al. Open Forum Infect Dis, 2021,8 (7):ofab116.
[41] Begré L, et al. JHEP Rep, 2025,8 (2):101671.
[42] Lin W, He Y, Gu F, et al. J Med Virol, 2024,96 (12):e70114.
[43] Gu F, Zeng K, Lan X, et al. J Med Virol, 2024,96 (6):e29762.
[44] Li X, Xu L, Lu L, et al. J Transl Med, 2024,22 (1):901.
[45] Avihingsanon A, et al. AIDS, 2022, OALBX0105.
[46] Avihingsanon A, et al. CROI 2025, Poster 666.
[47] Patrick Miailhes, et al. J Hepatol, 2014.
[48] Anders Boyd, et al. J Viral Hepat, 2016.

唐小平 教授
广州医科大学
二级教授、主任医师,博士生导师
广州医科大学感染病研究所所长,附属市八医院感染病学顾问、肝病首席专家,附属第一医院国家重大传染病防治基地专家委员会主任
中国性病艾滋病防治协会副会长,国家卫健委艾滋病治疗专家组副组长,广东省性病艾滋病防治协会会长,中华医学会感染病分会原常委,中华预防医学会感染病分会常委,广州市医学会会长
新世纪百千万人才工程国家级人选,国家卫健委有突出贡献中青年专家,享受国务院特殊津贴专家,广东省“特支计划”科技领军人才,广东省医学领军人才,全国先进工作者,全国优秀科技工作者
主要研究方向为艾滋病、病毒性肝炎和新突发传染病的临床诊疗与发病机制,擅长突发公共卫生事件处置,先后主持10多项国家、省部级重大课题研究,以第一或通讯作者发表SCI论文80多篇,包括在Nat Commun (5篇),NSR, eClinicalMedicine(柳叶刀子刊),J Virol,EMI 等高水平杂志发表论文,主编专著10部,获省部级科技进步奖8项
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
