- 首页 > 正文
李凌华教授:HIV低病毒血症检测助力抗病毒治疗高质量发展
感染医线 发表时间:2026/5/9 17:27:43
编者按:2026年4月17日至20日,第十一届全国艾滋病学术大会于重庆召开。随着我国艾滋病抗病毒治疗覆盖率和病毒抑制率均已达到95%,如何实现第三个95%目标中最后的“最后一公里”,成为临床关注的焦点。广州医科大学附属市八医院感染病中心李凌华教授在大会上系统阐述了HIV低病毒血症的临床界定、流行病学特征、危害机制及检测技术进展,强调高灵敏度检测在LLV早期识别和干预中的核心价值。
01
LLV:被忽视的“灰色地带”
随着抗反转录病毒治疗(ART)的进步,HIV感染者的管理已经从“生存”转向“质量”的更高要求。近年来,我国艾滋病抗病毒治疗已取得举世瞩目的成就。数据显示,中国治疗覆盖率和病毒抑制率均已达到95%[1]。然而,也有研究显示,中国仍有5.3%至38.7%的患者存在低病毒血症[2],部分地区的LLV可能被低估,如贵州的LLV检出率达33.7%。LLV是我国在实现“第三个95%”病毒学抑制率基础上,达到100%的“最后一公里”。
LLV并非严格意义的“治疗成功”,而是“未竟之志”。国际上同样面临LLV挑战的问题,是容易被忽视的“灰色地带”。肯尼亚一项纳入约80万名接受ART的HIV感染者的研究显示,LLV发生率为18.5%;在初次出现LLV的患者中,分别有13.3%和2.4%进展为病毒学失败和病毒学衰竭[3]。这一数据提示,LLV并非无害的“波动”,而是病毒学恶化的前兆。
02
LLV的临床界定:标准之争
目前,国内外不同指南对LLV的界定标准仍存在差异。为统一临床实践,中国LLV专家共识(2025版)(以下简称《共识》)推荐意见1(A1级)建议:对于接受ART至少24周,或曾达到稳定病毒学抑制的PLWH,若持续检测到(至少连续2次)HIV RNA为50-500拷贝/mL,则按照LLV进行管理[2]。
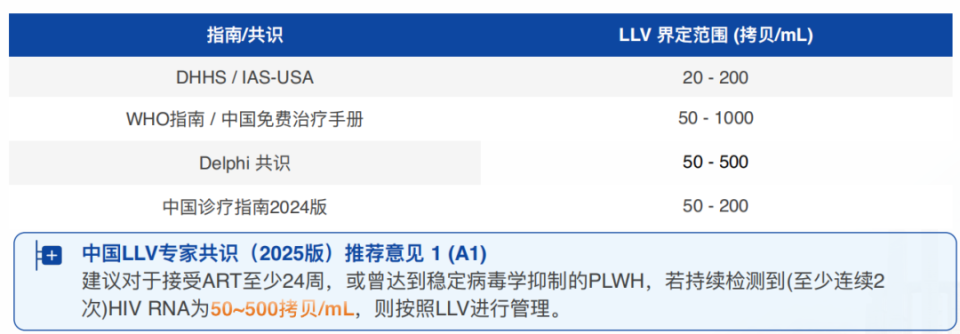
△国内外不同指南/共识对 LLV 界定范围的对比
根据病毒载量波动特征,LLV可分为两种类型:间歇性LLV(iLLV)指一次独立的LLV,且前一次和后一次病毒载量低于检出限;持续性LLV(pLLV)指至少出现连续两次LLV[4]。针对LLV的管理,《共识》建议:需评估患者的依从性、耐受性和药物不良反应、药物相互作用(A1级);LLV通常不需要改变治疗方案(B1级),但需每3个月监测1次HIV RNA,以评估是否需要调整ART方案(C1级)。
03
LLV的人群“画像”和机制探索
LLV并非偶然事件,它在特定人群中具有高发性。中国LLV专家共识(2025版)推荐意见2明确指出,以下四项是LLV发生的独立风险因素:依从性不佳、基线CD4⁺T细胞计数低、起始方案含蛋白酶抑制剂、基线病毒载量高。
其中,依从性管理的重要性值得重点强调。Meta分析数据显示,依从性不佳人群中LLV的发生率高达38.05%,提示临床需加强患者教育与随访[5]。
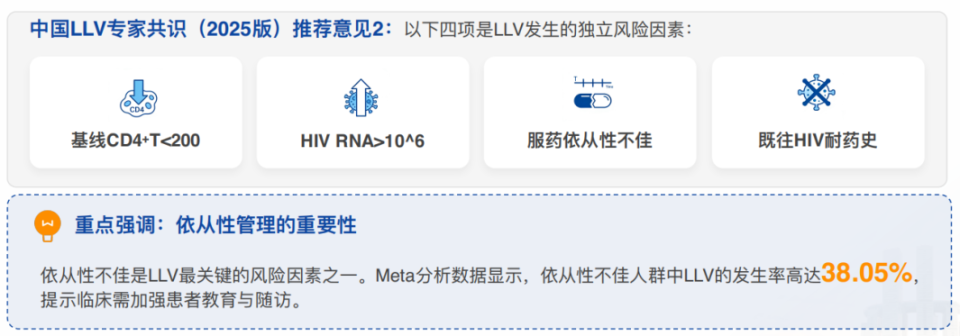
△中国LLV专家共识(2025版):LLV高危人群
河南中医药大学附属一院的荟萃研究发现,基线CD4<350细胞/μL(<200cells/μL 组OR 1.398;200~350cells/μL 组OR1.290)、基于PI的起始方案(OR 1.377)、基线VL>10⁵拷贝/mL(OR 1.567)、更换治疗方案(OR 1.883)、ART依从性差(OR 3.019)、年龄≥50岁(OR 1.293)及ART开始年龄≥50岁(OR 1.219)是LLV发生的风险因素(P值均<0.05)[6],这一结论与北京佑安医院的研究结果高度一致[7]。
广州八院的一项研究为理解LLV的起源提供了新的视角。研究提示,LLV可能源于单核细胞/巨噬细胞库的持续低水平释放,而非单纯病毒复制活跃,LLV组近全长前病毒序列的超突变率显著更高(LLV组42.35% vs 病毒学失败组8.78%,P<0.01),LLV组遗传距离也更大(0.0446 vs 0.0186,P<0.01),提示LLV具有独特的进化动力学特征[8]。这一发现意味着,LLV不仅仅是抗病毒药物压力下病毒复制的“漏网之鱼”,更可能反映了潜伏库中前病毒的特殊生物学特性。
04
“沉默杀手”:LLV的多维度临床危害
LLV的临床危害是多维度的,涉及病毒学、免疫学、代谢和死亡风险等多个层面。
病毒学失败的“前奏”
非洲博茨瓦纳一项持续超过5年的研究,纳入46,716名基于多替拉韦(DTG)的一线ART患者,结果显示,相比无LLV患者,单次LLV、确诊LLV和持续LLV患者病毒学失败的风险比分别增加至2.2(95%CI: 2.0-2.3)、3.3(95%CI: 2.5-3.3)和6.6(95%CI: 4.9-8.9)[9]。贵州一项研究进一步显示,低水平LLV组(50-199拷贝/mL)病毒学失败发生率为6.18%(366/5,920),中水平LLV组(200-399拷贝/mL)为11.79%(221/1,875),高水平LLV组(400-999拷贝/mL)为13.70%(254/1,854),三组间差异显著(χ²=127.848,P<0.001)。间歇性LLV的病毒学失败发生率为8.82%,持续性LLV为8.14%,两者无显著差异[10]。
耐药突变的“温床”
重庆公卫中心一项研究显示,LLV患者中26.32%(35/133)至少发生一个药物类别的耐药突变,15.04%(20/133)在血浆RNA中检测到耐药突变,表明存在活跃复制的耐药病毒;持续性LLV组耐药发生率略高于间歇性LLV组,在蛋白酶抑制剂组中更为明显[11]。
慢性炎症与非艾滋病定义疾病
LLV还与代谢性疾病风险增加密切相关。一项研究显示,LLV组空腹血糖“快速增加”轨迹的比例显著高于病毒抑制组(OR=2.53,95%CI: 1.53-4.16,P<0.001)。在中位随访2.4年期间,14.9%(1,297/26,097人)发展为糖尿病。糖尿病患者发生率在blips(一过性病毒波动)组和LLV组中均显著升高,LLV组的风险高于blips组(OR=1.47 vs 1.31)[12]。
死亡风险的“隐形推手”
云南德宏一项纳入7,273名HIV患者的研究发现,与病毒载量<50拷贝/mL相比,LLV 200-999拷贝/mL对应的艾滋病相关死亡风险显著升高(aHR=2.37,95%CI: 1.36-4.14)[13]。这一结论与瑞典全国观察性研究的结果一致[14]。
核心洞察:LLV并非无害的病毒波动。它是病毒学失败、耐药突变、代谢性疾病风险增加乃至死亡风险升高的明确前兆,是艾滋病治疗质量管理中不可忽视的“沉默杀手”。
05
LLV检测技术:欲善其事,先利其器
高精度检测是LLV早期识别的核心手段。检测下限(LoD)决定发现能力,定量下限(LoQ)决定定量准确性。临床上,≤20拷贝/mL被认为是LLV早期识别的金标准,精准监测是实现“U=U”(测不到=不传染)承诺的重要保障。
目前主流的高精度检测平台包括罗氏Cobas 6800/5800系统和丽珠LIVZON系统等,此类系统具备LoD和LoQ均≤20拷贝/mL、双靶标检测能力的特点。广州八院一项纳入415例样本的评估结果进一步证实,在线性范围20~2×10³拷贝/mL内,国产(LIVZON)与进口(Cobas)两系统相关性和一致性高,定量值差异平均值为0.18 Log IU/mL,95%可信区间界限为(-0.56~0.93)Log IU/mL,三个主要亚型两个平台线性相关系数均>0.93[15]。
病毒载量VL≤50拷贝/mL的阳性检出具有重要的预警价值。英国一项研究显示,治疗12个月后,在病毒载量分别为40-49拷贝/mL、RNA阳性和RNA阴性的三组患者中,后续发生病毒反弹(>50拷贝/mL)的概率分别为34.2%(95%CI: 28.1-40.3%)、11.3%(95%CI: 8.5-14.0%)和4.0%(95%CI: 2.3-5.7%),组间差异显著(P<0.0001),提示病毒载量检测越低越好[16]。荷兰一项回顾性研究同样发现,在使用三类抗病毒治疗药物的患者中,血液HIV残留病毒在1-50拷贝/mL的占比高达35%-44%,而<20拷贝/mL阳性(残留病毒1-19拷贝/mL)组占比高达25%。残留病毒1-19拷贝/mL组和20-49拷贝/mL组与后续病毒反弹显著相关,比值比分别为2.66和4.90(95%CI: 1.98-3.58和3.41-7.04)[17]。
高灵敏度检测有助于发现极低病毒载量LLV。一项采用超速离心法和血液核酸单检试剂检测HIV抗体阳性、RNA阴性样本的研究显示,超灵敏检测方案可显著提高血浆中残留病毒RNA的检出率[18]。
随检测技术升级,过往用旧平台评价治疗有效率的效果可能被高估。一项回顾性研究发现,在使用罗氏CAP/CTM(旧平台)检测病毒载量持续<50拷贝/mL的200名患者中,“Best control组”(可检出频率<25%)切换至罗氏Cobas 6800(新平台)后,病毒可检测到的比例从49%提升至58%,其中有20%患者出现一次病毒载量≥50拷贝/mL;而在“Less control组”(可检出频率≥25%)中,切换平台后病毒载量≥20拷贝/mL的比例从20%提升至46%[19]。
双靶标检测是高灵敏试剂防漏检的必要条件。一项长达13年的随访病例研究发现,经过八年的病毒抑制后,实验室于2018年6月引入pol和LTR双靶点检测试剂,病毒载量可通过LTR靶点稳定检测到,定量范围为912至11,220拷贝/mL,而基于pol单靶点检测试剂持续未检出[20]。这一案例生动地说明了单靶点检测可能导致的漏检风险。
技术要点:实现LLV的精准管理,依赖于高灵敏度(≤20拷贝/mL)的检测技术。双靶标设计(如pol+LTR)是避免因病毒变异导致漏检、确保病载结果可靠性的关键技术保障。
写在最后
接受ART的HIV感染者中,LLV多见于治疗初期及依从性不佳者,且发生率随治疗时间延长呈动态波动。LLV与病毒学失败、免疫重建不良及耐药突变累积密切相关,可增加病毒传播风险与远期死亡风险。高灵敏HIV-1病毒载量检测(检测下限≤20拷贝/mL)是实现LLV早期识别的核心手段,对优化治疗策略具有重要意义。从“生存”到“质量”,从“病毒抑制”到“完全抑制”,高灵敏度检测技术的推广应用,将成为我国实现第三个95%目标中“最后一公里”的关键助力。
参考文献
[1]张广,韩孟杰.中国艾滋病性病,2025,31(12):1297-1301.
[2]中华医学会热带病与寄生虫病分会艾滋病学组,等.中华临床感染病杂志(中英文),2025,18(1):6-18.
[3]Aoko A, et al. EClinical Medicine.2023 Aug 18;63:102166.
[4]中华医学会感染病学分会艾滋病学组, 中国疾病预防控制中心. 协和医学杂志, 2024, 15(6): 1261-1288.
[5] Zace D,et al.Sex Transm Infect, 2024, 100 (7) : 460-468.
[6]Zhang X, et al. Front Public Health. 2025 Oct 2;13:1661253.
[7]Zhao S, et al. Emerg Microbes Infect. 2025 Dec;14(1):2447613.
[8]Li J, et al. Front Microbiol. 2025 Aug 21;16:1647986.
[9]Bareng OT, et al. Viruses. 2024 May 1;16(5):720.
[10]Zheng Y, et al. Front Public Health. 2025 Jul 30;13:1535285.
[11]Zhang H, et al. Front Public Health. 2026 Feb 6;14:1753298.
[12]Tao C, et al. BMC Med. 2025 Jul 1;23(1):350.
[13]Yu H, et al. HIV Med. 2023 Jan;24(1):37-45.
[14]Elvstam O,et al.Clinical Infectious Diseases.2020. 72(12), 2079–2086.
[15]Deng X, et al. HIV Med. 2023 Feb 26.
[16]Doyle et al. The Lancet,2014:383, S44
[17]Oomen PGA, et al. J Med Virol. 2023 Oct;95(10):e29178.
[18]Coco SB, et al. J Clin Microbiol. 2025 Dec 17;63(12):e0099525.
[19]Wirden M, et al. 2022 Jul 28;77(8):2251-2256. .
[20]Sberna G, et al. Heliyon. 2024 Apr 19;10(9):e29842.

李凌华 教授
广州医科大学附属市八医院感染病中心主任,主任医师
广州医科大学教授、博士生导师
广东省杰出青年医学人才,广州市高层次卫生人才医学重点人才
中国性病艾滋病防治协会HIV合并肝病专业委员会副主任委员
中国性病艾滋病防治协会代谢性疾病专业委员会副主任委员
中华医学会感染病分会及细菌真菌与耐药防治分会委员
广东省医师协会感染科医师分会主任委员
广东省医学会细菌真菌与耐药防治分会副主任委员
曾到杜克大学、北卡罗莱纳大学做访问学者,承担国自然、国家科技部重大专项及省市课题近30项,国内外杂志发表文章160余篇
来源:《感染医线》
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
